阿爾茲海默癥(AD)與小鼠疾病模型
什么是阿爾茲海默癥?
阿爾茲海默癥(Alzheimer‘s Disease,AD )是一種常見的、但是起病隱匿的神經退行性疾病,俗稱老年癡呆。該病自1906年首次發現已經過去了100多年,很多我們所熟知的名人,例如美國前總統里根、英國前首相撒切爾夫人,以及《百年孤獨》作者加夫列爾·馬爾克斯,都在晚年罹患阿爾茲海默癥。
每年的9月21日,是“世界阿爾茲海默癥日”,全世界各個國家和地區都會通過組織一系列不同的活動,讓更多人了解并關注AD。
目前,僅有幾個可用于治療AD的藥物獲得FDA批準使用:他克林、多奈哌齊、卡巴拉汀、加蘭他敏、美金剛和美金剛多奈哌齊復方制劑,但是由于他克林會產生較強的肝臟毒性,已經退市。
這些藥物都只能在一定程度上對部分患者起到有限的作用,并不能阻止或顯著延緩病情的進一步發展。面對數量如此龐大的患者群體,各大藥企紛紛投入巨資到藥物研發中。
但是由于AD發病機制尚未明確,影響因素復雜,除了爭議中的Aducanumab(也被大家稱為aduCANumab)之外,近20年來還沒有其他真正意義上的AD治療藥物獲得FDA批準。

新藥研發一直伴隨著高風險和高收益,行業內也一直有著“雙十”的說法,即:研發一款新藥需要十年時間,花費超過十億美金。用“火葬場”來形容目前的AD藥物研發情況并不夸張,各大制藥巨頭更是接連損兵折將。
有數據顯示,全球在AD上的藥物研發投入已累計超過6000億美元,其中失敗的臨床藥物超過了300種,失敗率超過99%,而癌癥的藥物研發失敗率僅為81%。
考慮到AD疾病發展過程中涉及的多種因素,建立能夠忠實再現人類病理表型的臨床前動物模型將會更好的加速和推進AD藥物研發。
動物模型為我們更好的了解AD發病機制提供了很好的工具,可以允許我們以另外一種方式進行療法測試。
自從家族性AD(Familial Alzheimer‘s disease,FAD)突變被發現以來,許多轉基因模型都可以重現AD的某些特征。例如無脊椎動物建模(如黑腹果蠅或秀麗隱桿線蟲)具有繁育周期短等優點,但是他們的神經系統特征與人類相比差異過大。
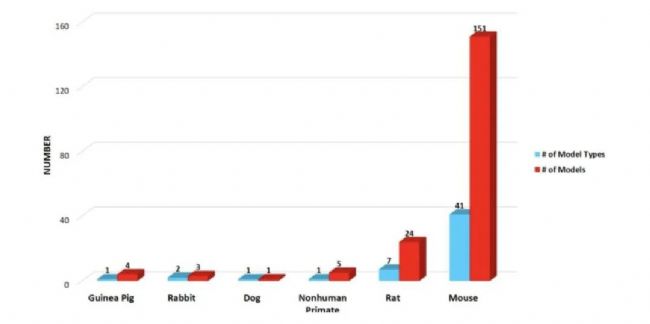
在脊椎動物中,小鼠是用來進行轉基因建模的主要物種,因為它們的繁育周期短,成本相對較低。
因此, AD小鼠模型在AD藥物研發中就顯得非常重要,也是臨床前研究中應用最多的模型[1]。對于AD研究中不同類型的小鼠模型,可以訪問Alzforum:
(https://www.alzforum.org/research-models/alzheimers-disease )進行查看。
在一項臨床前研究中,結果顯示Aducanumab給藥后
在 Tg2576 轉基因小鼠中觀察到了 Aβ 淀粉樣蛋白斑塊的減少[2]
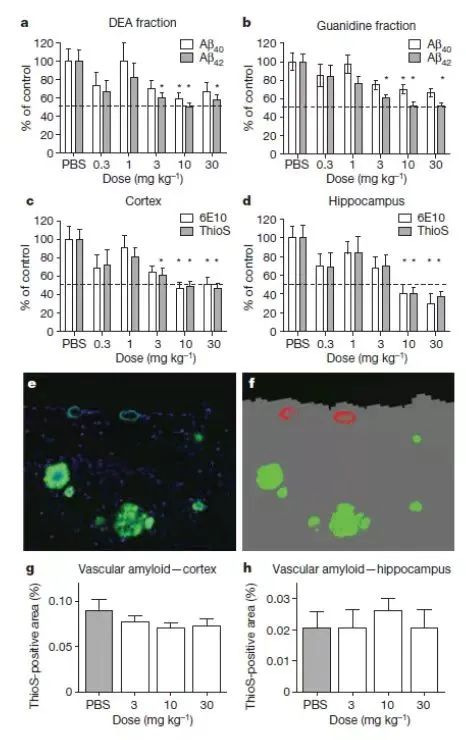 此外,在一項關于Candesartan的研究中
此外,在一項關于Candesartan的研究中
Candesartan逆轉了5XFAD小鼠海馬中的Aβ淀粉樣蛋白面積和小膠質細胞激活的情況[3]
 杰克森實驗室作為AD研究的推動者
杰克森實驗室作為AD研究的推動者
可以提供多種常見的AD小鼠模型和臨床前藥效服務

可以看到在2021年,ClinicalTrials.gov中登記注冊的臨床試驗仍然有126項。其中, 疾病修正和緩解癥狀的小分子藥物占據了大半,其他部分是疾病修正的生物療法[4]
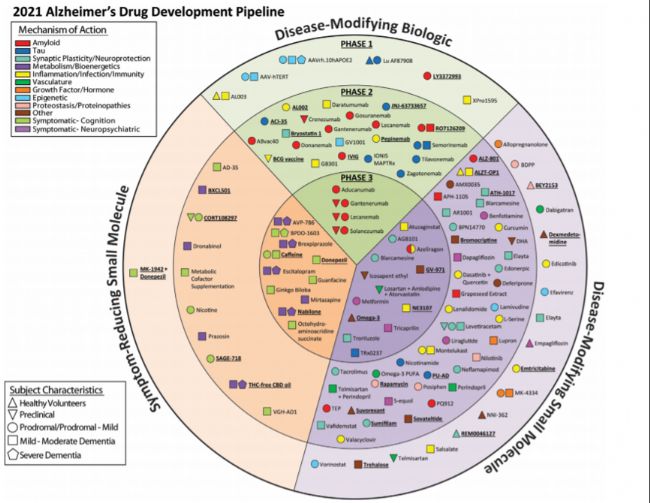
在Aducanumab獲批之后,2021年6月23日,渤健(Biogen)和衛材(Eisai)又聯合宣布, FDA授予其針對Aβ的在研抗體Lecanemab (BAN2401)突破性療法認定。
突破性療法認定旨在授予那些潛在治療嚴重疾病的藥物,促進開發新藥治療尚未滿足醫療需求的重病或威脅生命的疾病,縮短有前景的新藥的開發和審查時間。
盡管目前業界對于Aducanumab的上市仍然充滿爭議,但是它的獲批也極大地提升了大家對于AD等神經退行性疾病藥物的研發熱情。
同樣的,2021年6月24日, FDA也授予禮來制藥(LILLY)的在研新藥Donanemab治療AD突破性療法認定。同時,禮來制藥也計劃在今年晚些時候通過加速審批路徑提交其Donanemab的《生物制品許可申請》(BLA)。
由于AD發病機制復雜,發病原因至今尚未明確,所以對于尋找有效的療法依舊困難重重。而在發現真正有效的療法之前,世界各地的科研人員也正在嘗試根據不同的假說,用不同的方式尋找答案,來攻克這一世紀難題。

阿爾茲海默癥(Alzheimer‘s Disease,AD )是一種常見的、但是起病隱匿的神經退行性疾病,俗稱老年癡呆。該病自1906年首次發現已經過去了100多年,很多我們所熟知的名人,例如美國前總統里根、英國前首相撒切爾夫人,以及《百年孤獨》作者加夫列爾·馬爾克斯,都在晚年罹患阿爾茲海默癥。
每年的9月21日,是“世界阿爾茲海默癥日”,全世界各個國家和地區都會通過組織一系列不同的活動,讓更多人了解并關注AD。
AD現狀
根據2020年的一份報告,全世界大約有5000萬名AD患者。隨著老齡化趨勢的加劇,患者數量也會逐年增加。AD病程緩慢且不可逆,臨床上可表現為記憶力減退、語言功能障礙等腦功能異常和性格行為改變等,嚴重影響患者的日常生活。目前,僅有幾個可用于治療AD的藥物獲得FDA批準使用:他克林、多奈哌齊、卡巴拉汀、加蘭他敏、美金剛和美金剛多奈哌齊復方制劑,但是由于他克林會產生較強的肝臟毒性,已經退市。
這些藥物都只能在一定程度上對部分患者起到有限的作用,并不能阻止或顯著延緩病情的進一步發展。面對數量如此龐大的患者群體,各大藥企紛紛投入巨資到藥物研發中。
但是由于AD發病機制尚未明確,影響因素復雜,除了爭議中的Aducanumab(也被大家稱為aduCANumab)之外,近20年來還沒有其他真正意義上的AD治療藥物獲得FDA批準。

新藥研發一直伴隨著高風險和高收益,行業內也一直有著“雙十”的說法,即:研發一款新藥需要十年時間,花費超過十億美金。用“火葬場”來形容目前的AD藥物研發情況并不夸張,各大制藥巨頭更是接連損兵折將。
有數據顯示,全球在AD上的藥物研發投入已累計超過6000億美元,其中失敗的臨床藥物超過了300種,失敗率超過99%,而癌癥的藥物研發失敗率僅為81%。
動物模型與AD
考慮到AD疾病發展過程中涉及的多種因素,建立能夠忠實再現人類病理表型的臨床前動物模型將會更好的加速和推進AD藥物研發。
動物模型為我們更好的了解AD發病機制提供了很好的工具,可以允許我們以另外一種方式進行療法測試。
自從家族性AD(Familial Alzheimer‘s disease,FAD)突變被發現以來,許多轉基因模型都可以重現AD的某些特征。例如無脊椎動物建模(如黑腹果蠅或秀麗隱桿線蟲)具有繁育周期短等優點,但是他們的神經系統特征與人類相比差異過大。
在脊椎動物中,小鼠是用來進行轉基因建模的主要物種,因為它們的繁育周期短,成本相對較低。
因此, AD小鼠模型在AD藥物研發中就顯得非常重要,也是臨床前研究中應用最多的模型[1]。對于AD研究中不同類型的小鼠模型,可以訪問Alzforum:
(https://www.alzforum.org/research-models/alzheimers-disease )進行查看。

在一項臨床前研究中,結果顯示Aducanumab給藥后
在 Tg2576 轉基因小鼠中觀察到了 Aβ 淀粉樣蛋白斑塊的減少[2]

Candesartan逆轉了5XFAD小鼠海馬中的Aβ淀粉樣蛋白面積和小膠質細胞激活的情況[3]

可以提供多種常見的AD小鼠模型和臨床前藥效服務

愈挫愈勇的AD新藥研發
可以看到在2021年,ClinicalTrials.gov中登記注冊的臨床試驗仍然有126項。其中, 疾病修正和緩解癥狀的小分子藥物占據了大半,其他部分是疾病修正的生物療法[4]

在Aducanumab獲批之后,2021年6月23日,渤健(Biogen)和衛材(Eisai)又聯合宣布, FDA授予其針對Aβ的在研抗體Lecanemab (BAN2401)突破性療法認定。
突破性療法認定旨在授予那些潛在治療嚴重疾病的藥物,促進開發新藥治療尚未滿足醫療需求的重病或威脅生命的疾病,縮短有前景的新藥的開發和審查時間。
盡管目前業界對于Aducanumab的上市仍然充滿爭議,但是它的獲批也極大地提升了大家對于AD等神經退行性疾病藥物的研發熱情。
同樣的,2021年6月24日, FDA也授予禮來制藥(LILLY)的在研新藥Donanemab治療AD突破性療法認定。同時,禮來制藥也計劃在今年晚些時候通過加速審批路徑提交其Donanemab的《生物制品許可申請》(BLA)。
由于AD發病機制復雜,發病原因至今尚未明確,所以對于尋找有效的療法依舊困難重重。而在發現真正有效的療法之前,世界各地的科研人員也正在嘗試根據不同的假說,用不同的方式尋找答案,來攻克這一世紀難題。

Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com





