文獻解讀:南模生物模式小鼠助力揭示二甲雙胍加重腎病的新機制
2023年10月17日,浙江大學王福俤教授及閔軍霞教授共同通訊在Cell Discovery(IF=34)在線發表題為“Metformin potentiates nephrotoxicity by promoting NETosis in response to renal ferroptosis”的研究論文,該研究表明,在二甲雙胍、煙酰胺、白藜蘆醇、雷帕霉素和senolytics等長壽藥物中發現,即使在低劑量下,二甲雙胍也會加劇實驗誘導的急性腎損傷(AKI)并增加小鼠的死亡率。
南模生物為該研究提供了Tmprss6-flox和Lcn2-flox條件性敲除小鼠。

針對這一臨床重大需求,王福俤教授指導蔡昭賢博士研究生利用以上5種長壽藥物干預缺血再灌注誘發的急性腎損傷小鼠,旨在探究這些長壽神藥是否具有保護腎功能的作用。實驗結果意外發現,二甲雙胍不但沒有保護效應,反而加重了缺血再灌注導致的急性腎損傷,并且呈現明顯的劑量依賴性。在較高水平的二甲雙胍暴露下,急性腎損傷小鼠全部出現死亡。進一步研究發現,二甲雙胍腎臟毒副作用不僅在缺血再灌注引發的急性腎損傷中存在,而且存在于橫紋肌溶解導致的急性腎損傷過程中。值得注意的是,在二甲雙胍的FDA服用指南以及我國專家臨床共識中指出,以腎小球濾過率 (eGFR) 為評估指標,若患者在一定程度上伴有腎臟疾病不建議服用二甲雙胍或調整服用劑量,存在潛在腎臟副作用,但機制并不清楚。由于越來越多的非糖尿病人群服用二甲雙胍,因此,可能存在潛在風險。
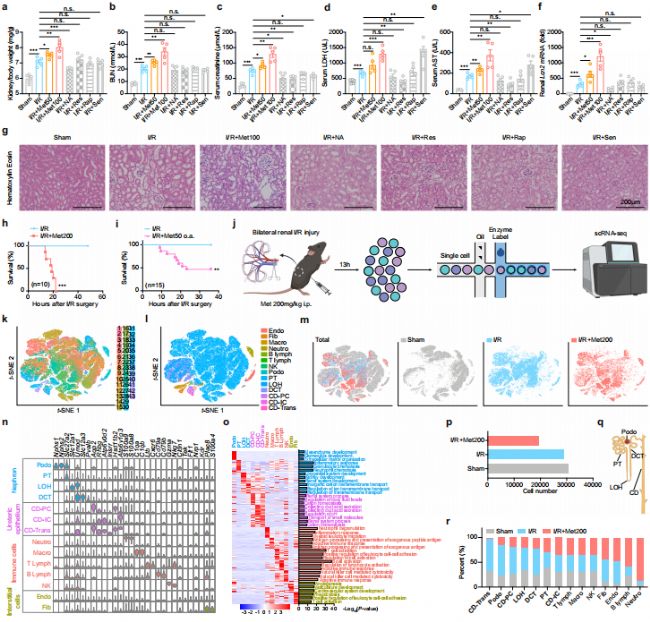
二甲雙胍劑量依賴性誘導腎臟實質細胞死亡并加重急性腎損傷
此外,從藥代動力學上來看,二甲雙胍在人體內無法被分解代謝,一般主要在肝臟富集,并以原分子形式從腎臟排出。為進一步探究二甲雙胍腎毒性的具體機制,研究團隊引進單細胞轉錄組測序技術發現,腎臟14種細胞類型中,7種腎臟實質細胞類型 (Podo / PT / LOH / CD-PC / CD-IC / CD-Trans / DCT) 在二甲雙胍的干預下數量明顯減少。由于實質細胞的特性無法在短期通過遷移來改變數量,因此研究人員提出二甲雙胍的干預可能會導致腎臟實質細胞發生死亡。
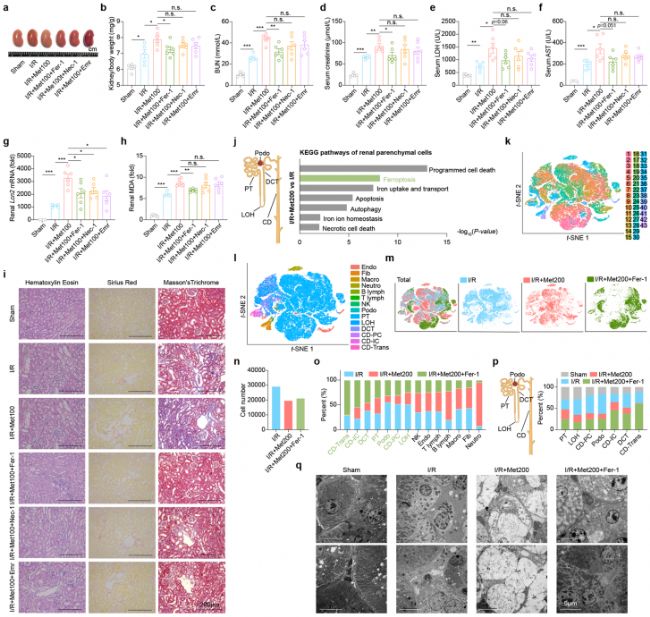
腎臟實質細胞鐵死亡為主要形式的細胞死亡是二甲雙胍腎毒性關鍵機制
研究團隊進一步揭示了具體機制,在誘導小鼠急性腎損傷(AKI)后,發現腎實質細胞發生鐵死亡等程序性細胞死亡,分泌大量的NGAL蛋白,并與循環中的二甲雙胍和游離鐵形成二甲雙胍-鐵-NGAL復合物,與中性粒細胞表面受體CXCR4結合發揮趨化作用,介導中性粒細胞浸潤至腎臟并發生NETosis(中性粒細胞對抗感染的一種機制),從而進一步加重腎損傷。最后,研究團隊證明了降低鐵水平對腎損傷具有保護作用,這支持了鐵在二甲雙胍引發的急性腎損傷(AKI)中發揮重要作用的觀點。
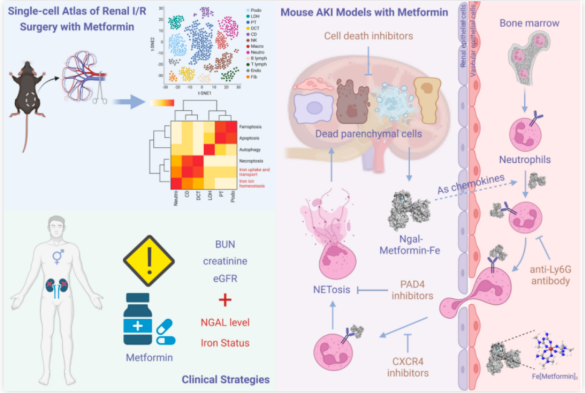
論文模式圖
總之,這項研究在小鼠體系中發現了二甲雙胍的腎臟副作用,從基礎研究的角度為二甲雙胍的臨床適用性提供了更多可靠的評估依據。從機制上,二甲雙胍與機體鐵元素的相互作用加劇了小鼠腎實質細胞的死亡,而這一過程引起了中性粒細胞NETosis的免疫反應。這一系列結果展示了細胞與細胞間的級聯反應和細胞生命活動的密切聯系,這也是該研究所取得的重要突破。在臨床角度來看,這項研究提示我們,接受二甲雙胍治療的患者除了評估其腎功能指標外,還應監測NGAL蛋白水平和鐵水平,以規避潛在的臨床腎毒性風險。
原文鏈接:https://www.nature.com/articles/s41421-023-00595-3





