文獻速遞:瑞士科學家用人類包皮成纖維細胞培育出肺類器官
來自伯爾尼大學的研究人員使用AVATAR Odyssey系統從誘導多能干細胞中獲得了復雜的多細胞肺類器官!此項研究成果由Vedat Burak Ozan和Thomas Geiser團隊在Stem Cell Reviews and Reports中發表。

誘導多能干細胞(iPSCs)可以用來做疾病建模,并促進藥物篩選,近年來已逐漸成為生物醫學領域很有前景的體外研究工具。研究人員已經可以將人iPSCs分化為肺細胞和三維肺球體或類器官。肺是一個多細胞的復雜器官,在微環境的交互影響下發育。
在本研究中,研究人員在可控的AVATAR微環境(cmO組,氧氣和壓力)中利用iPSCs制造出具備與肺泡結構復雜性相似的多細胞肺類器官。并通過SFTPC、PDPN和KRT5染色,證明存在2型和1型肺泡上皮細胞以及基底細胞。此外,cmO組中基因和蛋白表達量提高。蛋白質組學通路分析顯示,與正常培養組相比,cmO組中肺發育特異性通路上調。
此項研究中,研究人員通過使用可控的微環境,建立了一個由iPSCs衍生的多細胞肺類器官,可將其作為一種新的細胞模型,用于研究肺部健康和肺泡相關疾病。
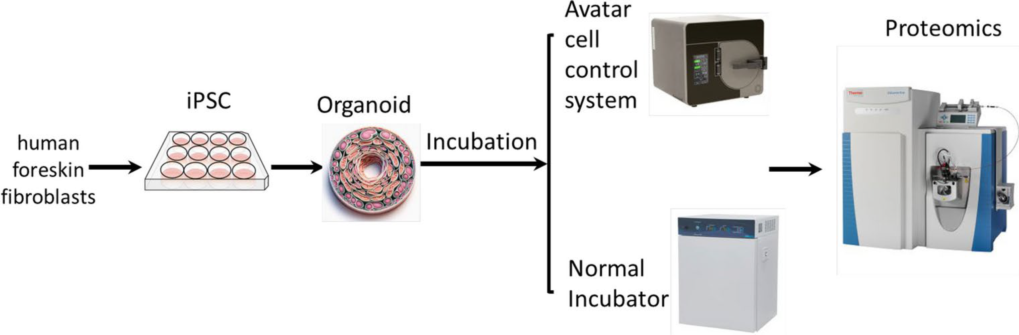
圖1. 實驗流程圖
iPSCs分別在標準培養箱(37℃,5% CO2)和AVATAR系統中分化為成熟肺類器官。
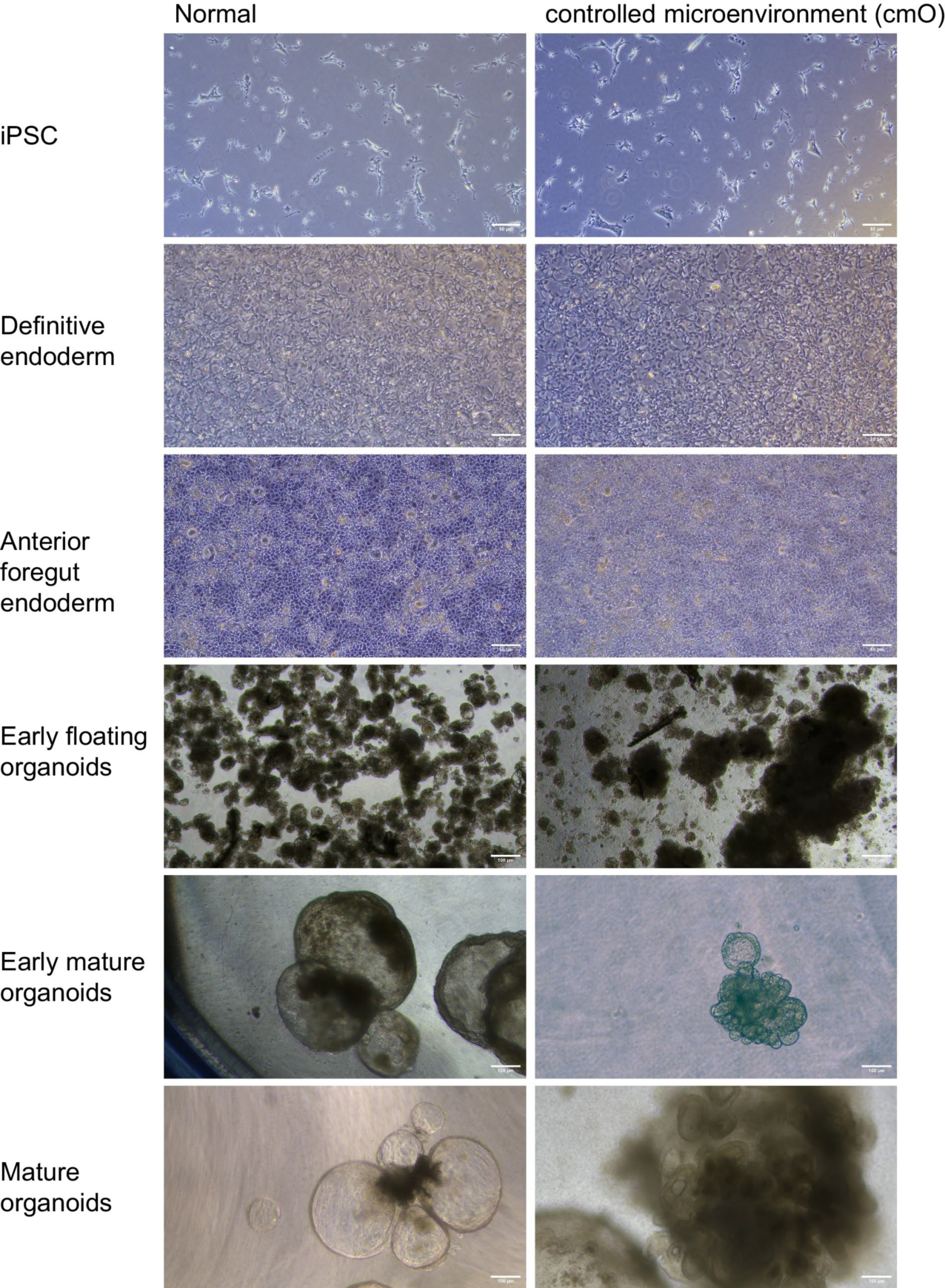
圖2. 兩種培養條件下,iPSCs所有分化階段的明場圖像
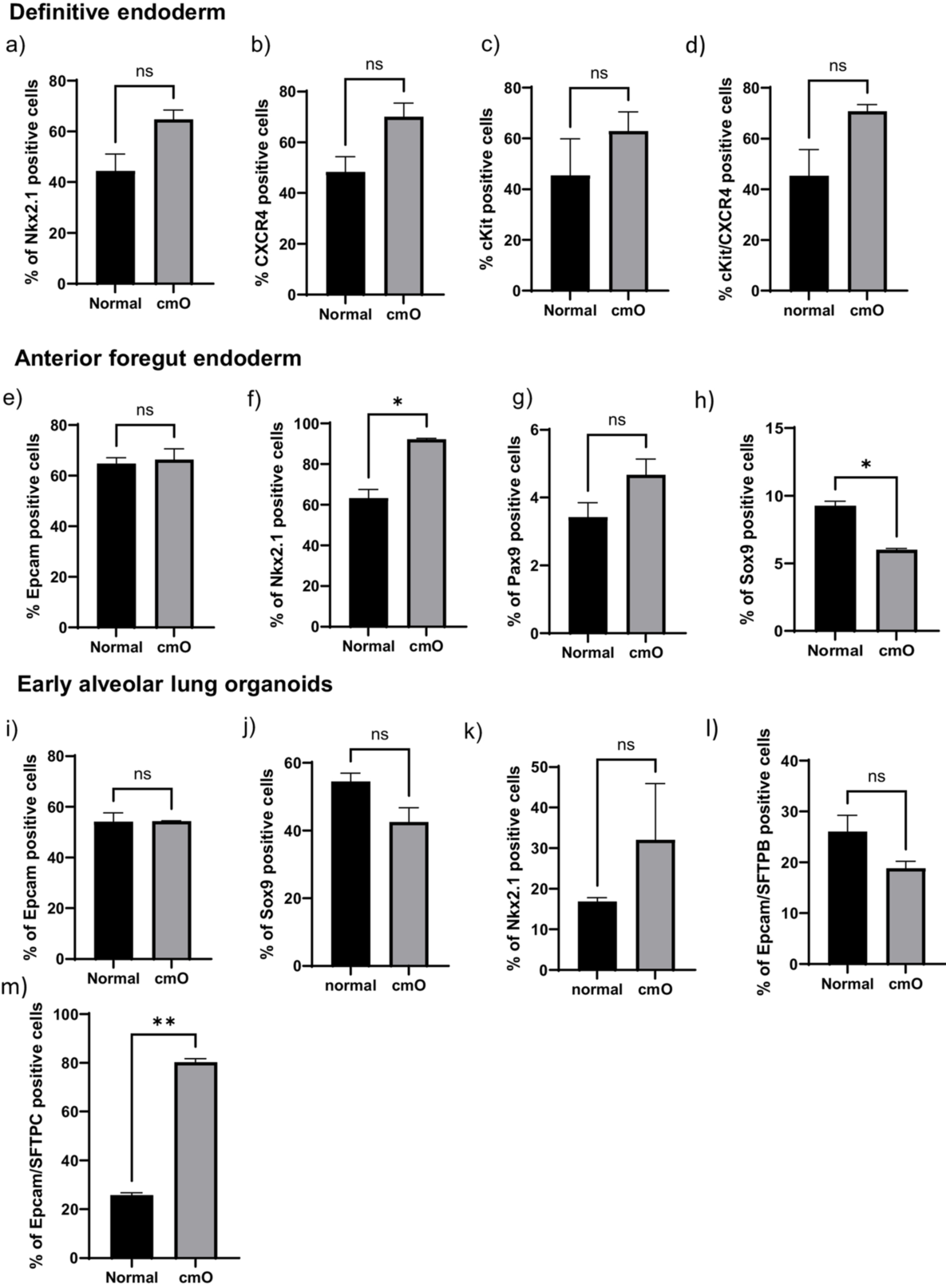
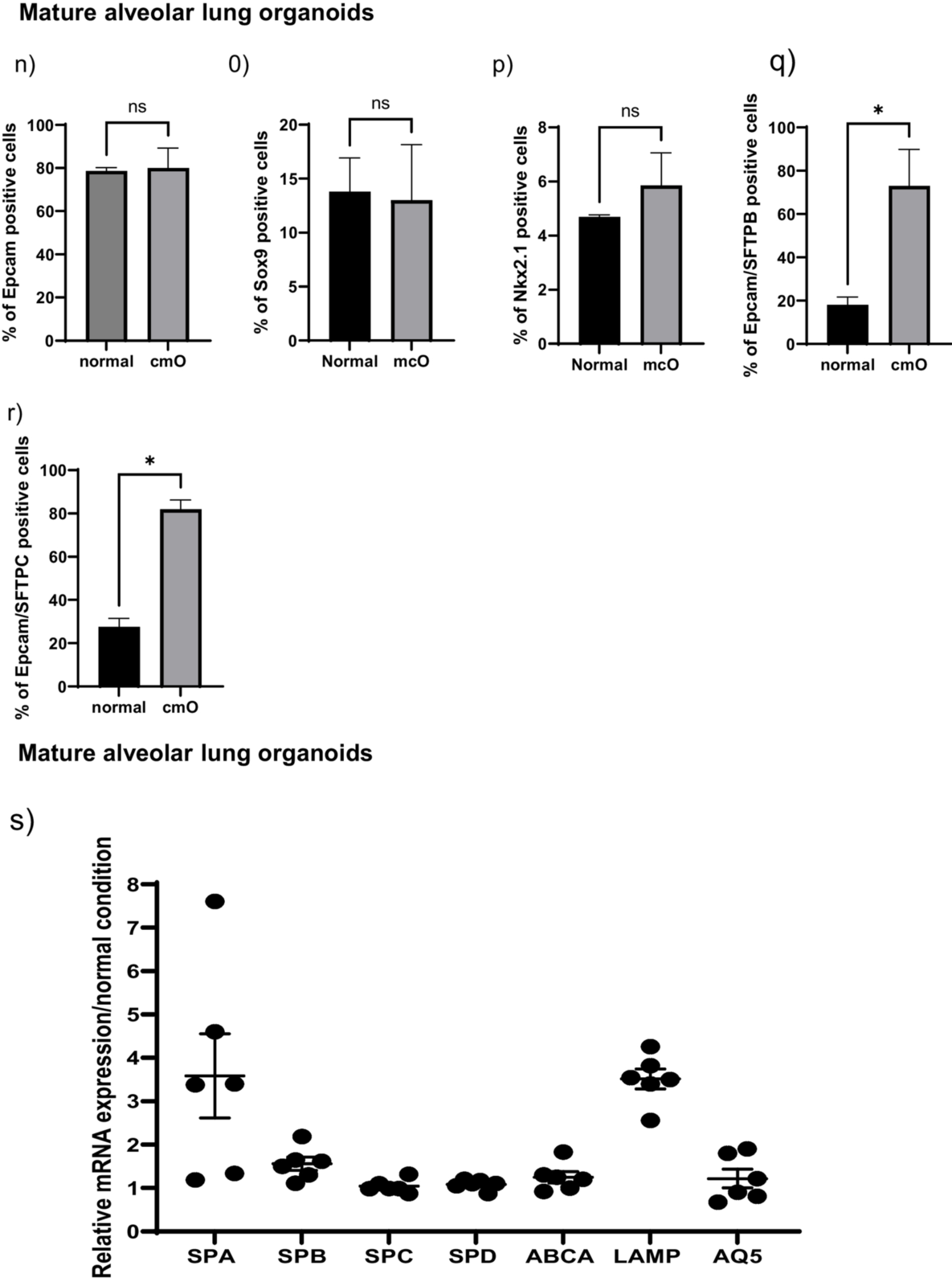 圖3. 細胞表面標記物和細胞內標記物分析。通過流式細胞術分析所有階段的細胞表面標記物和細胞內標記物的表達,數據以表達所測標記的活細胞的百分比表示,并對標準培養箱中與AVATAR系統中生長的類器官之間進行比較。
圖3. 細胞表面標記物和細胞內標記物分析。通過流式細胞術分析所有階段的細胞表面標記物和細胞內標記物的表達,數據以表達所測標記的活細胞的百分比表示,并對標準培養箱中與AVATAR系統中生長的類器官之間進行比較。
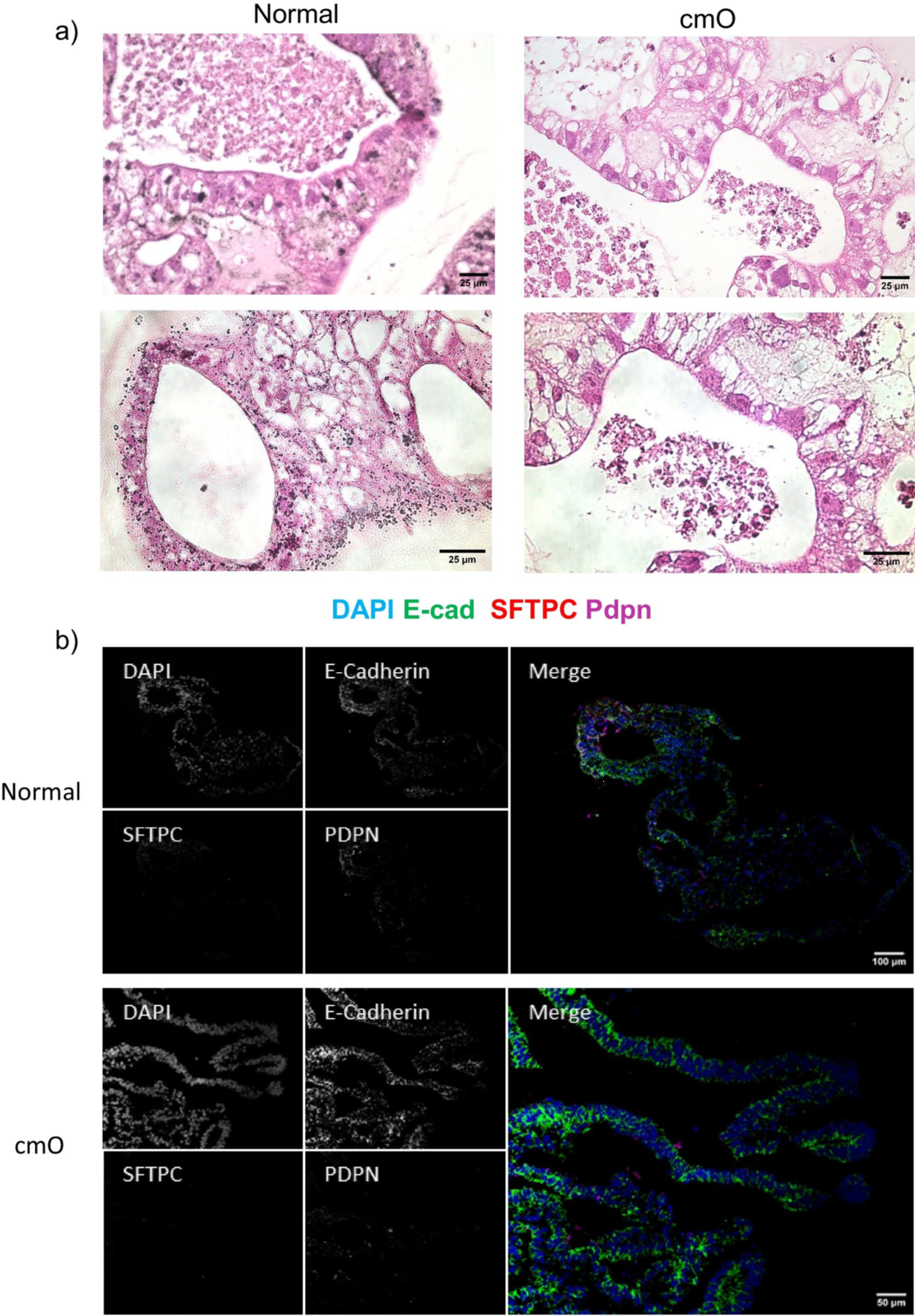
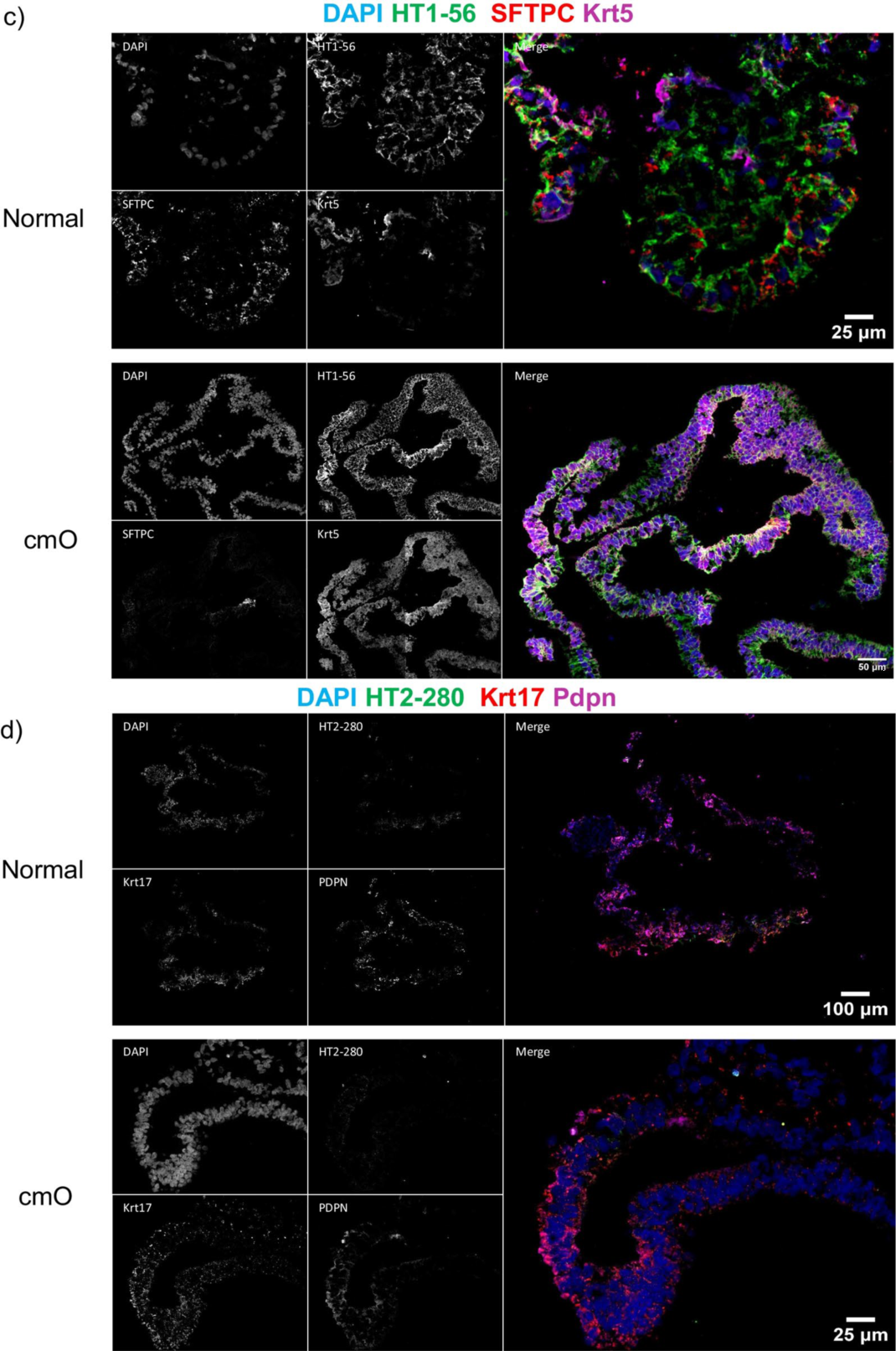
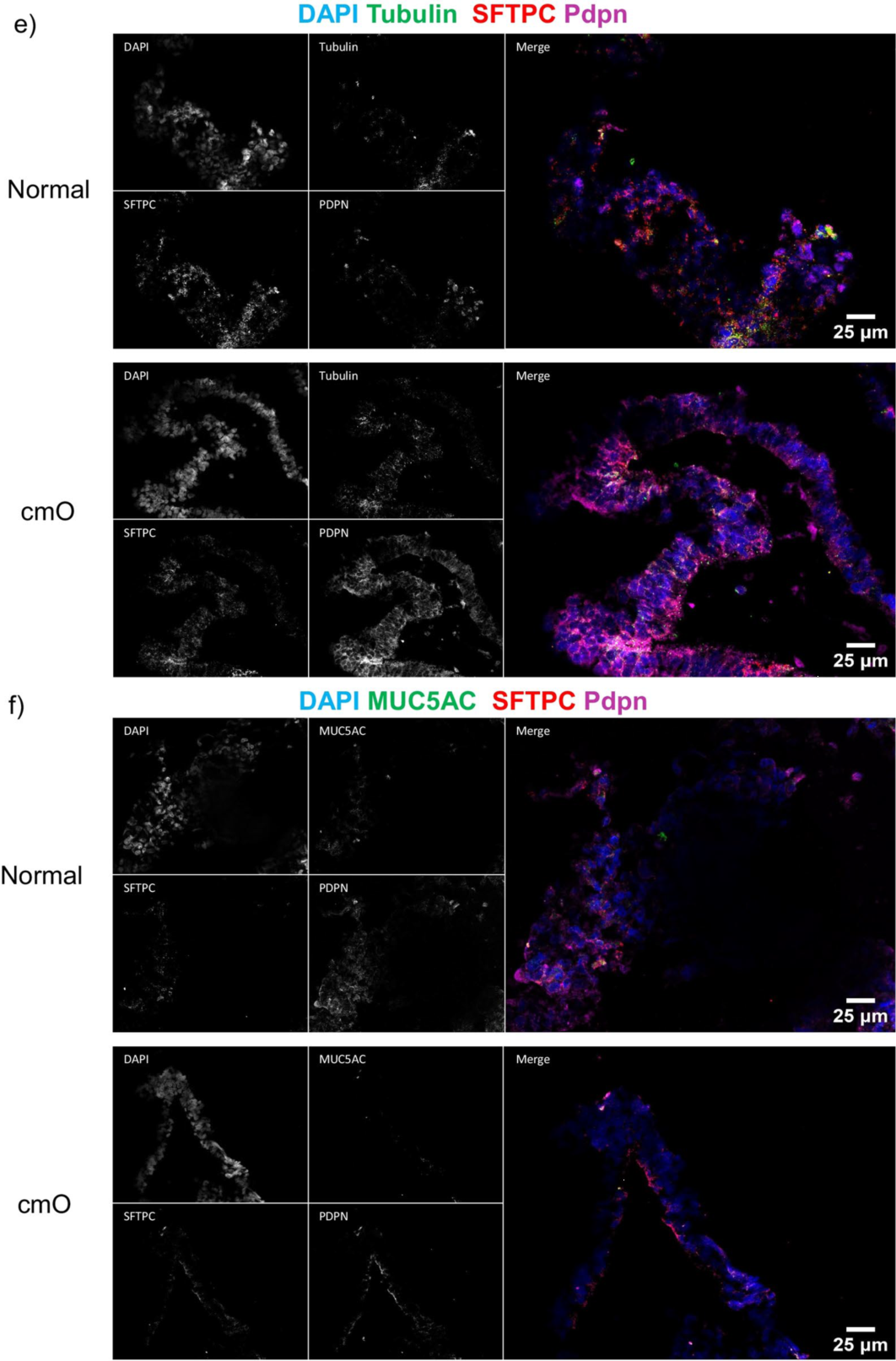
圖4. 對成熟的類器官進行染色

誘導多能干細胞(iPSCs)可以用來做疾病建模,并促進藥物篩選,近年來已逐漸成為生物醫學領域很有前景的體外研究工具。研究人員已經可以將人iPSCs分化為肺細胞和三維肺球體或類器官。肺是一個多細胞的復雜器官,在微環境的交互影響下發育。
在本研究中,研究人員在可控的AVATAR微環境(cmO組,氧氣和壓力)中利用iPSCs制造出具備與肺泡結構復雜性相似的多細胞肺類器官。并通過SFTPC、PDPN和KRT5染色,證明存在2型和1型肺泡上皮細胞以及基底細胞。此外,cmO組中基因和蛋白表達量提高。蛋白質組學通路分析顯示,與正常培養組相比,cmO組中肺發育特異性通路上調。
此項研究中,研究人員通過使用可控的微環境,建立了一個由iPSCs衍生的多細胞肺類器官,可將其作為一種新的細胞模型,用于研究肺部健康和肺泡相關疾病。

圖1. 實驗流程圖

圖2. 兩種培養條件下,iPSCs所有分化階段的明場圖像





圖4. 對成熟的類器官進行染色
AVATAR系統中的類器官顯示出更明確的分支和細胞分布,類似于遠端肺的結構,并且細胞分布的組織方式與遠端肺中觀察到的類似(圖4a)。上皮細胞標記物SFTPC、HT1-56、HT2-280、E-cadherin、PDPN(圖4b-f)的免疫染色證實了與遠端肺相似的細胞分布。值得注意的是,還對AVATAR系統中的KRT 5進行了染色(圖4c),顯示類器官中存在基底細胞。

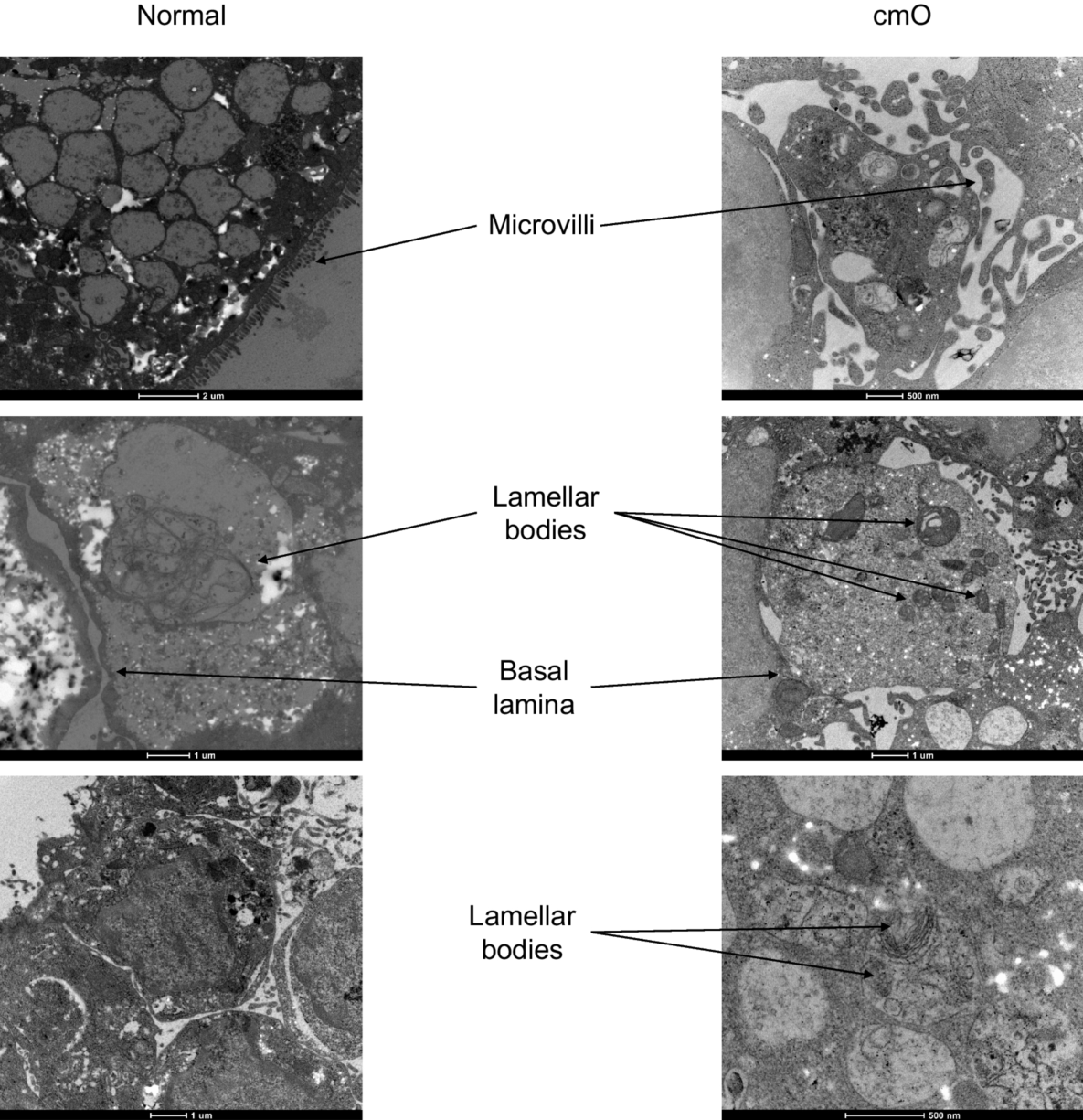
圖5. 標準培養箱和AVATAR系統中培養的類器官的電子顯微鏡圖像。標準培養箱中的類器官表現為微絨毛和疏松的板層小體,AVATAR系統中的類器官表現為微絨毛和結構良好的板層小體。

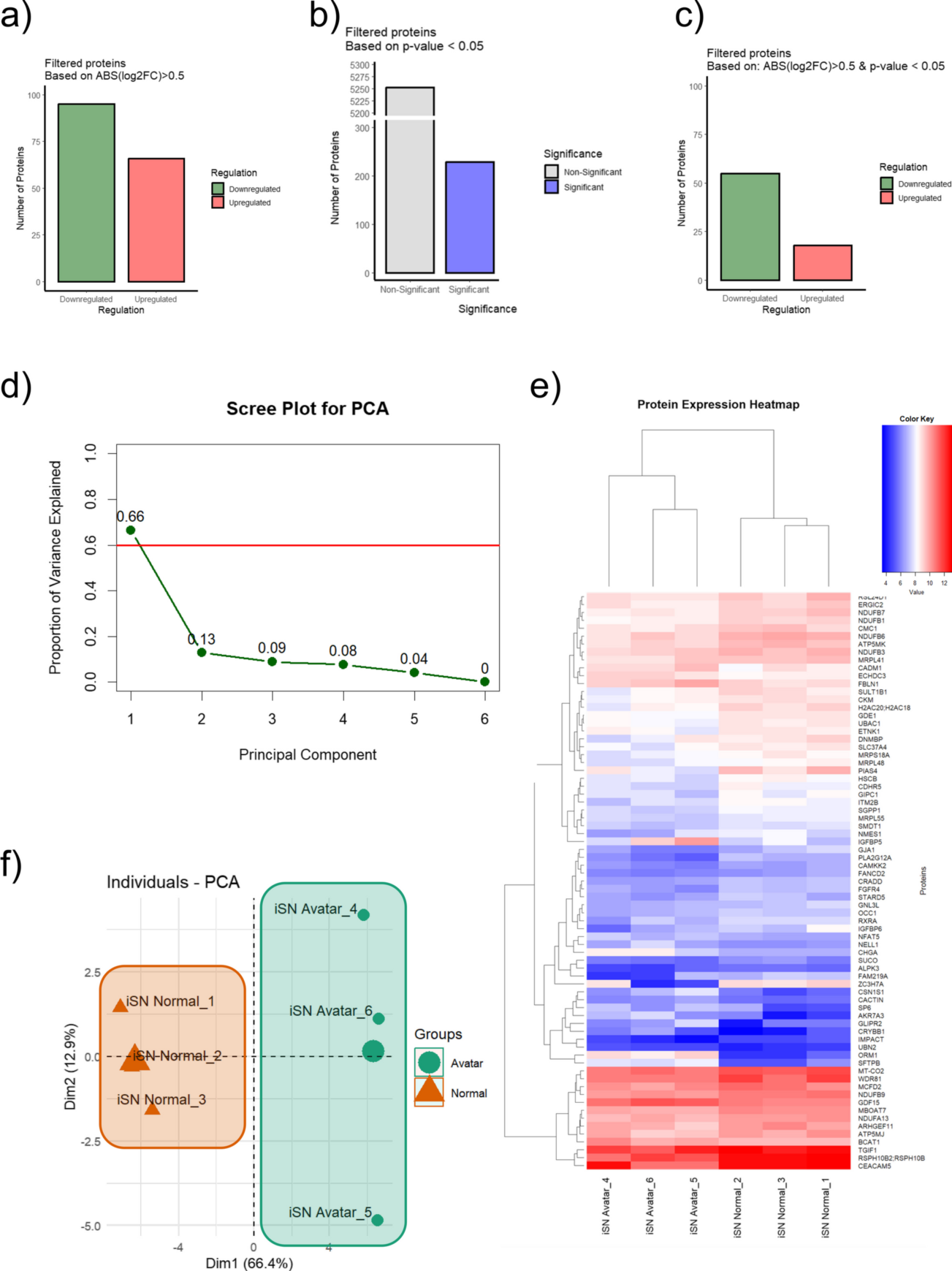
圖6. (a)柱狀圖顯示了基于絕對log2(倍數變化)> 0.5過濾的蛋白質數量,并描繪了下調和上調的蛋白質;(b)基于p值< 0.05過濾的蛋白質數量的柱狀圖;(c)基于絕對log2(倍數變化) > 0.5和p值< 0.05過濾的蛋白質的柱狀圖,根據顯著性和調節分類;(d)顯示PCA分析中各主成分解釋的方差比例的Scree圖;(e)蛋白質組學分析結果的二維PCA圖,對比AVATAR系統中受控微環境(cmO)培養的類器官(綠色)和標準培養箱中培養的類器官(橙色),展示了數據中最顯著變化的Dim1和Dim2的主成分分布;(f)具有層次聚類的熱圖,顯示多個樣本中蛋白質的表達模式,不同顏色鍵表示從低(藍色)到高(紅色)的表達水平。

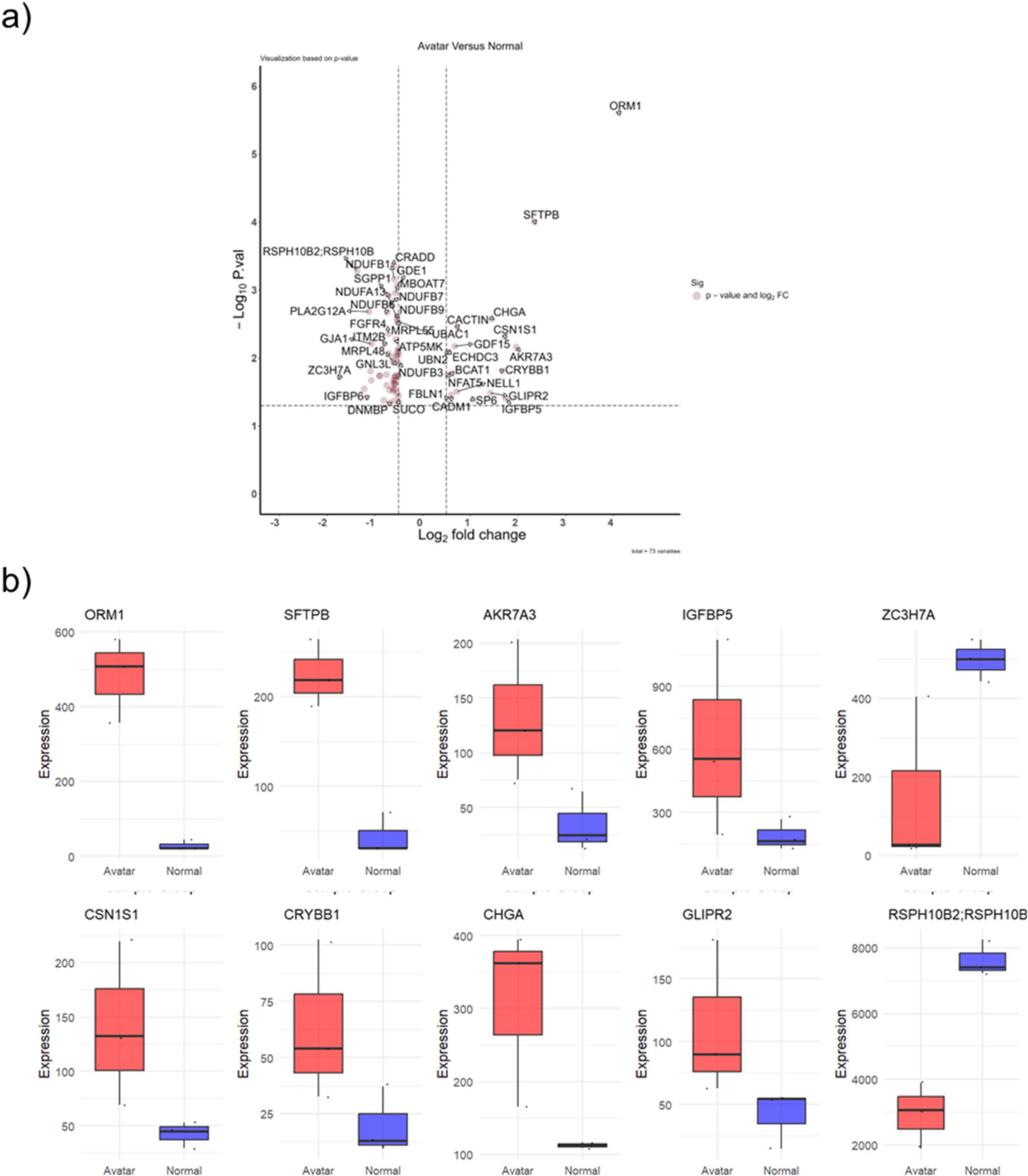
圖7. 來自AVATAR系統和正常培養箱的類器官培養物的差異蛋白質表達情況。(a)顯示所分析蛋白質的log2倍變化與p值的負對數的火山圖,AVATAR系統中顯著上調的蛋白位于右側,顯著下調的蛋白位于左側,顯著程度以y軸上的高度表示;(b)頂部差異表達蛋白的箱線圖,紅框表示在AVATAR系統中培養的類器官的蛋白表達水平,藍框表示標準培養箱中培養的類器官的蛋白表達水平,每個框中的中心線代表中位表達水平,框邊界表示四分位距(interquartile range, IQR)。

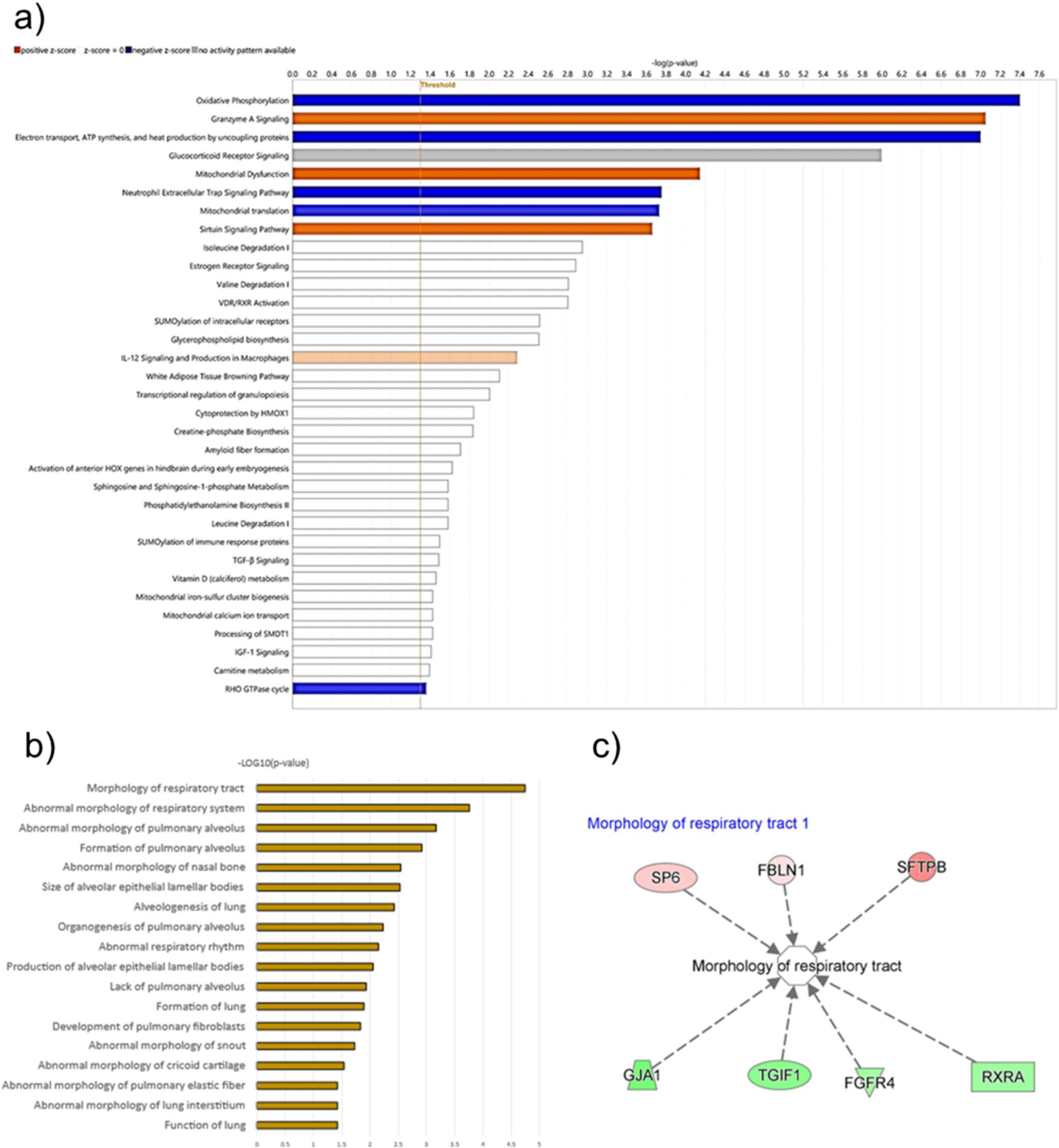
圖8. 類器官培養物蛋白質組學數據的通路和功能分析。(a)利用Ingenuity Pathway analysis (IPA)工具生成的通路分析,展示了在不同條件下培養的類器官的蛋白質組學數據中富集的生物通路。通路通過-log(p-value)進行排序,閾值設置為p < 0.05,表示通路受培養條件影響的可能性。條形圖的長度表示顯著性水平,藍色條形圖表示預測的激活,橙色條形圖表示預測的通路抑制;(b)強調與差異蛋白表達相關的疾病和生物學功能的功能分析。函數按-log(p-value)排序,閾值設為p < 0.05。條形的長度代表了組合的重要性;(c)聚焦于“呼吸道形態”功能的網絡分析,在數據集中識別關鍵基因,根據其表達變化的方向預測影響該功能。AVATAR系統與標準培養箱相比,紅色節點代表表達上調的基因,綠色節點代表表達下調的基因。
綜上所述,研究人員成功地利用iPSCs制造出了肺類器官,并且在壓力和氧控制的微環境中觀察到肺類器官的發育和成熟,標志著肺類器官研究的一個重大飛躍。
本研究不僅強調了微環境因素在肺類器官形成中的作用,而且將這些受控的體外模型定位為研究肺發育和疾病的有效工具。可控微環境作為一個關鍵決定因素出現,為藥物篩選、疾病建模和解開肺生理的復雜性提供了一個真實的平臺,此項研究為其奠定了堅實的基礎,肯定了微環境控制對體外肺類器官模型保真度的深遠影響。
綜上所述,研究人員成功地利用iPSCs制造出了肺類器官,并且在壓力和氧控制的微環境中觀察到肺類器官的發育和成熟,標志著肺類器官研究的一個重大飛躍。
本研究不僅強調了微環境因素在肺類器官形成中的作用,而且將這些受控的體外模型定位為研究肺發育和疾病的有效工具。可控微環境作為一個關鍵決定因素出現,為藥物篩選、疾病建模和解開肺生理的復雜性提供了一個真實的平臺,此項研究為其奠定了堅實的基礎,肯定了微環境控制對體外肺類器官模型保真度的深遠影響。
標簽:
AVATAR 模擬微環境
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com





