ADCЛҺОпуwНвСРҫҝЎ°Т»ХҫКҪЎұ®aЖ·ҪвӣQ·Ҫ°ё
ҝ№уwЕјВ“ЛҺОпЈЁAntibody-Drug ConjugateЈ¬ADCЈ©КЗНЁЯ^ЯBҪУЧУҢўРЎ·ЦЧУ»ҜәПОпЕјВ“ЦБ°РПтРФҝ№уw»тҝ№уwЖ¬¶ОЙПөДТ»оҗРВРНөДЙъОпјјРgЛҺОпЈ¬ҝЙТФФцҸҠЛҺОп°РПтРФәН·Җ¶ЁРФЎўңpЙЩЕRҙІ¶ҫёұ·ҙ‘ӘЎўМбёЯЦОҜҹЦё”өЈ¬јжҫЯӮчҪyРЎ·ЦЧУЛҺОпөДҡўӮыР§‘ӘәНҝ№уwЛҺОпөД°РПтРФЈ¬ЦчТӘ‘ӘУГУЪҝ№Д[Бц»тХЯЖдЛыјІІЎөД°РПтЦОҜҹЎЈ
Т» ADCЛҺОпөДҪYҳӢҪMіЙ
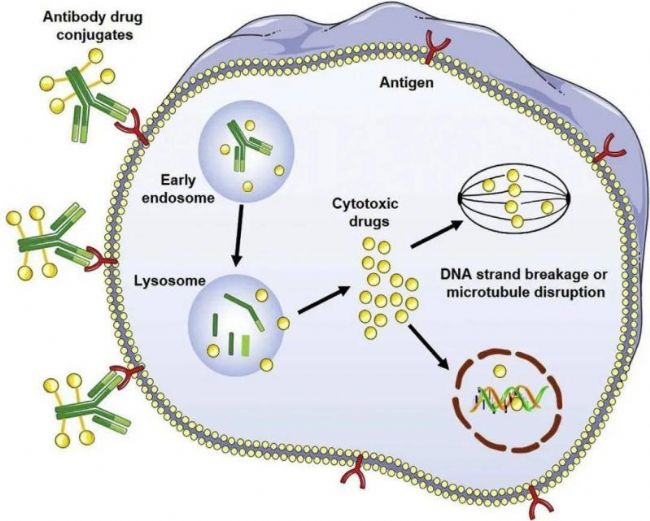
ADCЛҺОпУЙҝ№уw»тҝ№уwЖ¬¶ОЎўЯBҪУЧУәНРЎ·ЦЧУ»ҜәПОпИэӮҖІҝ·ЦҪMіЙЎЈЖдЦРЈ¬ҝ№уwНЁіЈЯxУГҝЙғИНМөДҝ№уwЈ¬ЦчТӘЧчУГКЗ°РПтРФҪйҢ§ҝ№уwТАЩҮРФјҡ°ыНМКЙЈ»ЯBҪУЧУҫЯУРТ»¶ЁөДСӯӯh·Җ¶ЁРФЈ¬ҝЙТФЦ§іЦЛҺОпФЪөҪЯ_°РЖч№ЩЗ°І»ұ»ҪөҪв»тХЯЙЩБҝҪөҪвЈ¬ЯMИлјҡ°ыәуДЬүтҝмЛЩбҢ·Е»оРФРЎ·ЦЧУ»ҜәПОпЈ»РЎ·ЦЧУ»ҜәПОпДЬүтҢҰ°Рјҡ°ы®aЙъЛҺР§ЧчУГЎЈ
ADC·ЦЧУЯMИлуwғИәуЈ¬ҝЙНЁЯ^ҶОҝЛВЎҝ№уwөДҢ§ПтЧчУГЕc°Рјҡ°ыұнГжөДҝ№ФӯҪYәПЈ¬ІўЯMТ»ІҪЮDИл°Рјҡ°ығИЈ¬ЯMИлјҡ°ығИ (ЦчТӘФЪИЬГёуwғИ) өДADC·ЦЧУЈ¬ҝЙНЁЯ^»ҜҢW/»тГёҙЩЧчУГбҢ·ЕРЎ·ЦЧУ¶ҫЛШәН/»т¶ҫЛШоҗЛЖОп (јҙР§‘Ә·ЦЧУ) ТФ “ҡўңз”°Рјҡ°ыЎЈADCЛҺОпФЪҪYәПБЛҶОҝЛВЎҝ№уwөДёЯ¶И°РПтРФәНРЎ·ЦЧУ¶ҫЛШөДҸҠјҡ°ы¶ҫРФөИғһьc•rЈ¬ТІҪoЖдЛҺҙъ„УБҰҢWСРҫҝҺ§ҒнБЛЦT¶аМф‘рЎЈ

ҲD1 ADCЛҺОпҪYҳӢ
¶ю ADCЛҺОпөДЛҺҙъ„УБҰҢWМШХч
ҸД·ЦЧУБҝҙуРЎәНҝХйgуw·eҒнЦvЈ¬ҝ№уwҳӢіЙБЛADCҪYҳӢЙПөДЦчуwЎЈЧчһйХыуwЈ¬ADCұн¬FіцЦT¶аЕcҝ№уwұҫЙноҗЛЖөДЛҺҙъ„УБҰҢWМШХчЈ¬ө«УЙУЪADCЛҺОпКЗ¶а·ЦЧУҪMіЙөД»мәПОпЈ¬ёчІҝ·Ц·ЦЧУј°ЖдҙъЦxОпөДҙжФЪәН·ЦІјҫщРиұ»Н¬•rСРҫҝЎЈ
ТтҙЛЈ¬ADCЛҺОпЭ^ӮчҪyҝ№Д[БцЛҺОпЈ¬ЖдЛҺҙъ„УБҰҢWСРҫҝёьА§лyЈ¬ЗТЦчТӘуw¬FФЪОьКХЈЁAbsorptionЈ©Ўў·ЦІјЈЁDistributionЈ©ЎўҙъЦxЈЁMetabolismЈ©әНЕЕР№ЈЁExcretionЈ©Ј¬јҙADMEЯ^іМЦРЎЈADCІЙУГЧўЙд·ҪКҪҪoЛҺЈ¬Жд·ЦІјН¬ҝ№уwЛҺОпоҗЛЖЈ¬ҫщМШ®җРФөДлSҝ№Фӯ·ЦІјФЪУЪСӘТәБҝҙуөДҪMҝ—ЦРЈ¬ИзёОЎўДIөИЖч№ЩЦРЎЈёОЕKКЗИЛуwЧоҙуөДЛҺОпҙъЦxЖч№ЩЎЈADCЛҺОпЯMИлИЬГёуwЈЁ»тЛб»ҜөДёО„тқ{ТәЈ©ғИЈ¬Ц®әуҸДADCЛҺОпЙПбҢ·ЕөДРЎ·ЦЧУ¶ҫРФР§‘ӘіЙ·ЦәНҫЯУРЛҺР§өДҙъЦx®aОпҫщФЪёОЕKЦРөДјҡ°ыЙ«ЛШP450ГёЯMРРҙъЦxЈ¬ТІ•ю°lЙъУЙГёХTҢ§»тГёТЦЦЖҢ§ЦВөДЛҺОп—ЛҺОпПа»ҘЧчУГ¬FПу°lЙъЎЈЧоҪKЈ¬ADCЛҺОпҪӣҙъЦxәуІҝ·ЦУОлxР§‘ӘРЎ·ЦЧУЎўІҝ·Ц·ЦЧУБҝЭ^РЎ¶алДј°°ұ»щЛбЯBҪУөДР§‘Ә·ЦЧУЎў·ЦЧУБҝЭ^РЎөДҝ№уwҙъЦxЖ¬¶ОҝЙДЬНЁЯ^ДIРЎЗтһVЯ^»тЮDЯ\уwҪйҢ§¶шұ»ЕЕР№ЦБјSұгЦРЎЈ
ЈЁҒнФҙЈәActa Pharm Sin B. 2020 Sep;10(9):1589-1600Ј©
ИэЎўADCЛҺОпуwНвСРҫҝ“Т»ХҫКҪ”®aЖ·ҪвӣQ·Ҫ°ё
ёщ“юҮшјТЛҺЖ·ФuҢҸЦРРДЈЁCENTER FOR DRUG EVALUATION, CDEЈ©°lІјөДЎ¶ADC·ЗЕRҙІСРҫҝјјРgЦёҢ§Фӯ„tЎ·Ј¬ҢҰADCЛҺОпФЪ·ЗЕRҙІлA¶ОөДСРҫҝІЯВФәН»щұҫҝтјЬМбіцБЛПакPТӘЗуЈ¬ІўЦшЦШҸҠХ{БЛADCЛҺОпРиТӘЯMРРуwНвәНуwғИЛҺАнҷCЦЖәНЛҺР§ЧчУГөДСРҫҝөДұШТӘРФЎЈ
һйқMЧгҝН‘фҢҰADCЛҺОп·ЗЕRҙІлA¶ОуwНвФзСРөДРиЗуЈ¬IPHASEЧчһй„“РВЛҺуwНвСРҫҝЙъОпФҮ„©ТэоIХЯЈ¬ҪЁБўБЛADCЛҺОпуwНвСРҫҝ“Т»ХҫКҪ”®aЖ·ҪвӣQ·Ҫ°ёЎЈҢҰУЪADCЛҺОпөДй_°lЈ¬КЧПИРиҙ_¶ЁЖдбҢ·ЕУРР§ЭdәЙЈЁpayloadЈ©өДҫЯуwРОКҪЈ¬¶шНЁіЈуwНвpayloadбҢ·ЕФҮтһКЗФЪёОS9ҪM·ЦЎўИЬГёуwӯhҫіЎўЛб»ҜөДёО„тқ{Тә»тХЯ°Рјҡ°ыөД·хУэуwПөЦРНкіЙЎЈЖдҙОЈ¬бҳҢҰADCЛҺОпҸНлsөДЛҺҙъ„УБҰҢWМШХчЈ¬IPHASEй_°lіцНкХыөДЎў¶а·NҢЩЎў¶аЖ·оҗЎў¶аЖч№ЩөДADME®aЖ·№©ҝН‘фЯx“сЈ¬УГУЪЦ§іЦЛҺОпҙъЦxөДіхЖЪәYЯxЎЈ
Іҝ·Ц®aЖ·БРұн
IPHASE/…RЦЗәНФҙ‘{Ҫи¶аДкөДСР°lҪӣтһЈ¬НЖіцБЛ¶аоIУтЎў¶а·NоҗөДёЯ¶ЛҝЖСРФҮ„©Ј¬һйЛҺОпФзЖЪСР°lМṩәYЯx№ӨҫЯЈ¬һйЙъГьҝЖҢWоIУтөДМҪЛчМṩРВІДБПЎўРВ·Ҫ·ЁәНРВКЦ¶ОЈ¬һйКіЖ·ЎўЛҺЖ·Ўў»ҜҢWЖ·өИөДЯzӮч¶ҫРФСРҫҝМṩұгҪЭ®aЖ·Ј¬НыҸVҙуҝЖСР№ӨЧчХЯҒнлҠЧЙФғЈ¬ЧЙФғҹбҫҖ400-127-6686ЎЈ
кP УЪ ОТ Ӯғ
…RЦЗәНФҙЈ¬ЦВБҰУЪһй„“РВЛҺСР°lЖуҳIј°ЙъГьҝЖҢWСРҫҝҷCҳӢМṩёЯЖ·Щ|өДЙъОпФҮ„©Ј¬IPHASEһ鹫ЛҫәЛРДЖ·ЕЖЈ¬Ж·ЕЖЧЪЦј“Innovative Reagents For Innovative Research”ЎЈ
Т» ADCЛҺОпөДҪYҳӢҪMіЙ
ADCЛҺОпУЙҝ№уw»тҝ№уwЖ¬¶ОЎўЯBҪУЧУәНРЎ·ЦЧУ»ҜәПОпИэӮҖІҝ·ЦҪMіЙЎЈЖдЦРЈ¬ҝ№уwНЁіЈЯxУГҝЙғИНМөДҝ№уwЈ¬ЦчТӘЧчУГКЗ°РПтРФҪйҢ§ҝ№уwТАЩҮРФјҡ°ыНМКЙЈ»ЯBҪУЧУҫЯУРТ»¶ЁөДСӯӯh·Җ¶ЁРФЈ¬ҝЙТФЦ§іЦЛҺОпФЪөҪЯ_°РЖч№ЩЗ°І»ұ»ҪөҪв»тХЯЙЩБҝҪөҪвЈ¬ЯMИлјҡ°ыәуДЬүтҝмЛЩбҢ·Е»оРФРЎ·ЦЧУ»ҜәПОпЈ»РЎ·ЦЧУ»ҜәПОпДЬүтҢҰ°Рјҡ°ы®aЙъЛҺР§ЧчУГЎЈ
ADC·ЦЧУЯMИлуwғИәуЈ¬ҝЙНЁЯ^ҶОҝЛВЎҝ№уwөДҢ§ПтЧчУГЕc°Рјҡ°ыұнГжөДҝ№ФӯҪYәПЈ¬ІўЯMТ»ІҪЮDИл°Рјҡ°ығИЈ¬ЯMИлјҡ°ығИ (ЦчТӘФЪИЬГёуwғИ) өДADC·ЦЧУЈ¬ҝЙНЁЯ^»ҜҢW/»тГёҙЩЧчУГбҢ·ЕРЎ·ЦЧУ¶ҫЛШәН/»т¶ҫЛШоҗЛЖОп (јҙР§‘Ә·ЦЧУ) ТФ “ҡўңз”°Рјҡ°ыЎЈADCЛҺОпФЪҪYәПБЛҶОҝЛВЎҝ№уwөДёЯ¶И°РПтРФәНРЎ·ЦЧУ¶ҫЛШөДҸҠјҡ°ы¶ҫРФөИғһьc•rЈ¬ТІҪoЖдЛҺҙъ„УБҰҢWСРҫҝҺ§ҒнБЛЦT¶аМф‘рЎЈ

ҲD1 ADCЛҺОпҪYҳӢ
¶ю ADCЛҺОпөДЛҺҙъ„УБҰҢWМШХч
ҸД·ЦЧУБҝҙуРЎәНҝХйgуw·eҒнЦvЈ¬ҝ№уwҳӢіЙБЛADCҪYҳӢЙПөДЦчуwЎЈЧчһйХыуwЈ¬ADCұн¬FіцЦT¶аЕcҝ№уwұҫЙноҗЛЖөДЛҺҙъ„УБҰҢWМШХчЈ¬ө«УЙУЪADCЛҺОпКЗ¶а·ЦЧУҪMіЙөД»мәПОпЈ¬ёчІҝ·Ц·ЦЧУј°ЖдҙъЦxОпөДҙжФЪәН·ЦІјҫщРиұ»Н¬•rСРҫҝЎЈ
ТтҙЛЈ¬ADCЛҺОпЭ^ӮчҪyҝ№Д[БцЛҺОпЈ¬ЖдЛҺҙъ„УБҰҢWСРҫҝёьА§лyЈ¬ЗТЦчТӘуw¬FФЪОьКХЈЁAbsorptionЈ©Ўў·ЦІјЈЁDistributionЈ©ЎўҙъЦxЈЁMetabolismЈ©әНЕЕР№ЈЁExcretionЈ©Ј¬јҙADMEЯ^іМЦРЎЈADCІЙУГЧўЙд·ҪКҪҪoЛҺЈ¬Жд·ЦІјН¬ҝ№уwЛҺОпоҗЛЖЈ¬ҫщМШ®җРФөДлSҝ№Фӯ·ЦІјФЪУЪСӘТәБҝҙуөДҪMҝ—ЦРЈ¬ИзёОЎўДIөИЖч№ЩЦРЎЈёОЕKКЗИЛуwЧоҙуөДЛҺОпҙъЦxЖч№ЩЎЈADCЛҺОпЯMИлИЬГёуwЈЁ»тЛб»ҜөДёО„тқ{ТәЈ©ғИЈ¬Ц®әуҸДADCЛҺОпЙПбҢ·ЕөДРЎ·ЦЧУ¶ҫРФР§‘ӘіЙ·ЦәНҫЯУРЛҺР§өДҙъЦx®aОпҫщФЪёОЕKЦРөДјҡ°ыЙ«ЛШP450ГёЯMРРҙъЦxЈ¬ТІ•ю°lЙъУЙГёХTҢ§»тГёТЦЦЖҢ§ЦВөДЛҺОп—ЛҺОпПа»ҘЧчУГ¬FПу°lЙъЎЈЧоҪKЈ¬ADCЛҺОпҪӣҙъЦxәуІҝ·ЦУОлxР§‘ӘРЎ·ЦЧУЎўІҝ·Ц·ЦЧУБҝЭ^РЎ¶алДј°°ұ»щЛбЯBҪУөДР§‘Ә·ЦЧУЎў·ЦЧУБҝЭ^РЎөДҝ№уwҙъЦxЖ¬¶ОҝЙДЬНЁЯ^ДIРЎЗтһVЯ^»тЮDЯ\уwҪйҢ§¶шұ»ЕЕР№ЦБјSұгЦРЎЈ

ҲD2 ADCЛҺОпЧчУГҷCЦЖ
ЈЁҒнФҙЈәActa Pharm Sin B. 2020 Sep;10(9):1589-1600Ј©
ИэЎўADCЛҺОпуwНвСРҫҝ“Т»ХҫКҪ”®aЖ·ҪвӣQ·Ҫ°ё
ёщ“юҮшјТЛҺЖ·ФuҢҸЦРРДЈЁCENTER FOR DRUG EVALUATION, CDEЈ©°lІјөДЎ¶ADC·ЗЕRҙІСРҫҝјјРgЦёҢ§Фӯ„tЎ·Ј¬ҢҰADCЛҺОпФЪ·ЗЕRҙІлA¶ОөДСРҫҝІЯВФәН»щұҫҝтјЬМбіцБЛПакPТӘЗуЈ¬ІўЦшЦШҸҠХ{БЛADCЛҺОпРиТӘЯMРРуwНвәНуwғИЛҺАнҷCЦЖәНЛҺР§ЧчУГөДСРҫҝөДұШТӘРФЎЈ
һйқMЧгҝН‘фҢҰADCЛҺОп·ЗЕRҙІлA¶ОуwНвФзСРөДРиЗуЈ¬IPHASEЧчһй„“РВЛҺуwНвСРҫҝЙъОпФҮ„©ТэоIХЯЈ¬ҪЁБўБЛADCЛҺОпуwНвСРҫҝ“Т»ХҫКҪ”®aЖ·ҪвӣQ·Ҫ°ёЎЈҢҰУЪADCЛҺОпөДй_°lЈ¬КЧПИРиҙ_¶ЁЖдбҢ·ЕУРР§ЭdәЙЈЁpayloadЈ©өДҫЯуwРОКҪЈ¬¶шНЁіЈуwНвpayloadбҢ·ЕФҮтһКЗФЪёОS9ҪM·ЦЎўИЬГёуwӯhҫіЎўЛб»ҜөДёО„тқ{Тә»тХЯ°Рјҡ°ыөД·хУэуwПөЦРНкіЙЎЈЖдҙОЈ¬бҳҢҰADCЛҺОпҸНлsөДЛҺҙъ„УБҰҢWМШХчЈ¬IPHASEй_°lіцНкХыөДЎў¶а·NҢЩЎў¶аЖ·оҗЎў¶аЖч№ЩөДADME®aЖ·№©ҝН‘фЯx“сЈ¬УГУЪЦ§іЦЛҺОпҙъЦxөДіхЖЪәYЯxЎЈ

Іҝ·Ц®aЖ·БРұн
| оҗ„e | ·Цоҗ |
| ҒҶјҡ°ыҪM·Ц | ёОИЬГёуw |
| Лб»ҜёО„тқ{Тә | |
| ёО/Дc/ДI/·ООўБЈуw | |
| ёО/Дc/ДI/·ОS9 | |
| ёО/Дc/ДI/·О°ыЩ|Тә | |
| ФӯҙъёОјҡ°ы | ‘ТёЎёОјҡ°ы |
| ЩNұЪёОјҡ°ы | |
| ЦШҪMГё®aЖ· | CYPЦШҪMГё |
| UGTЦШҪMГё | |
| ЮDЯ\уw | ABCЮDЯ\уw |
| SLCЮDЯ\уw | |
| ҢЈҢЩСӘқ{ | СӘқ{ө°°ЧҪYәП |
| СӘқ{·Җ¶ЁРФ |
IPHASE/…RЦЗәНФҙ‘{Ҫи¶аДкөДСР°lҪӣтһЈ¬НЖіцБЛ¶аоIУтЎў¶а·NоҗөДёЯ¶ЛҝЖСРФҮ„©Ј¬һйЛҺОпФзЖЪСР°lМṩәYЯx№ӨҫЯЈ¬һйЙъГьҝЖҢWоIУтөДМҪЛчМṩРВІДБПЎўРВ·Ҫ·ЁәНРВКЦ¶ОЈ¬һйКіЖ·ЎўЛҺЖ·Ўў»ҜҢWЖ·өИөДЯzӮч¶ҫРФСРҫҝМṩұгҪЭ®aЖ·Ј¬НыҸVҙуҝЖСР№ӨЧчХЯҒнлҠЧЙФғЈ¬ЧЙФғҹбҫҖ400-127-6686ЎЈ
кP УЪ ОТ Ӯғ
…RЦЗәНФҙЈ¬ЦВБҰУЪһй„“РВЛҺСР°lЖуҳIј°ЙъГьҝЖҢWСРҫҝҷCҳӢМṩёЯЖ·Щ|өДЙъОпФҮ„©Ј¬IPHASEһ鹫ЛҫәЛРДЖ·ЕЖЈ¬Ж·ЕЖЧЪЦј“Innovative Reagents For Innovative Research”ЎЈ
- CellЈәҢўпӢКіәНДcөАОўЙъОпҪYәПЖрҒноA·АОёДcөАјІІЎ
- уwТәГвТЯөДәЛРДЎӘЎӘCD19+Bјҡ°ыөД»щұҫҪйҪBј°Жд№ҰДЬ
- ASGPRЈәGaINAc-siRNAЛҺОпҢҚ¬FёОғИ°РПтЯfЛНөДкPжI°Рьc
- »щЩ|ДzУРД[Бц®җ·NТЖЦІДЈРНәНоҗЖч№ЩЕарB¶а·ҪГж‘ӘУГ
- ИзәОёЯР§өШҪвӣQГвТЯФҮ„©ЦР·ЗМШ®җРФёЙ”_өДҶ–о}
- МЗЬХғИЗРГёHҸДө°°ЧЩ|МЗ»щ»Ҝ·ЦОцөҪө°°ЧЩ|ХЫҜB‘ӘУГ
- ФӯҙъёОјҡ°ы·ЦлxМбИЎөДҢҚтһ·Ҫ·ЁЎўБчіМЕcҪY№ы
- ГвТЯПөҪyөДЎ°¶аГжКЦЎұ-CD14+ҶОәЛјҡ°ыҝ№ёРИҫәНҝ№Д[БцГвТЯЦРөДЧчУГ
- IPHASE/…RЦЗәНФҙББПаBIONNOVAЙъОпбtЛҺ„“РВХЯХ“үҜ
- IPHASEЎӘЎӘ„“РВЛҺуwНвФuғrЙъОпФҮ„©Үш®aМжҙъПИРРХЯ
- IPHASEҫ«ІКББПаBIOCHINA2025ТЧЩQЙъОп®aҳIХ№У[
- IPHASEСыДъПаҫЫөЪ64ҢГГАҮш¶ҫАнҢW•юДк•юSOT 2025
- IPHASEББПаөЪК®ЛДҢГЛҺАнҢW•юЛҺОпәН»ҜҢW®җОпҙъЦx•юЧh
- IPHASEББПаөЪК®ЛДҢГЛҺОпәН»ҜҢW®җОпҙъЦxҢWРg•юЧh
- IPHASEЦъБҰ…^Ут„“РВ°lХ№»о„УфЯ®aҢWСРВ“„У„“РВҪ»Бч•ю
- IPHASEХnМГөЪИэЖЪЈәЮDЯ\уwСРҫҝФӯАнј°ФOУӢ
Copyright(C) 1998-2025 ЙъОпЖчІДҫW лҠФ’Јә021-64166852;13621656896 E-mailЈәinfo@bio-equip.com





