ОД«I·ЦПнЈәТЦЦЖРgәу°©°YҸН°lЕcЮDТЖөДРВРНј{ГЧЛҺОпIPI549@HMPСРҫҝ
¶аЙ«ОД«I·ЦПнЈәТ»·NДЬүтТЦЦЖРgәу°©°YҸН°lЕcЮDТЖөДРВРНј{ГЧЛҺОп
ҢҰУЪҙуІҝ·Ц°©°YҒнХfЈ¬КЦРgЗРіэКЗЧоЦШТӘТІКЗЧоЗРҢҚУРР§өДЦОҜҹКЦ¶ОЈ¬ө«КЗһйКІГҙУРР©ІЎИЛРgәуТАЕfРиТӘЧц»ҜҜҹЈ¬ІўЗТ°©°YҸН°lВКәЬёЯЈҝКВҢҚЙПЈ¬КЦРgЦ»ДЬЗРіэИвСЫҝЙТҠөД°©°YД[үKЈ¬И»әуЯm®”өД¶аЗРіэТ»Р©ЦЬҮъөД“ХэіЈ”ҪMҝ—Ј¬ө«Я@Іҝ·ЦҪMҝ—ҝҙЛЖХэіЈЈ¬ҢҚлHҝЙДЬТСҪӣқ“ІШ°©јҡ°ыЈ¬НЁЛЧТ»ьcХfЈәНвҝЖКЦРgІ»ДЬ°С°©јҡ°ы°Щ·Ц°ЩЗеАнөфЎЈЛщТФТ»ө©РgәуөДІЎАнҪY№ыІ»ҳ·У^Ј¬»јХЯТАЕfРиТӘЯMРР»ҜҜҹЈ¬ІўН¬•rЯҖРиТӘУГТ»Р©ГвТЯЦОҜҹөДЛҺОпЈ¬»ЦҸНГвТЯјҡ°ыҢҰД[Бцјҡ°ыөДҡўӮыБҰЎЈ
УЙУЪД[БцҪMҝ—СёЛЩФцйLЈ¬уw·eёЯ¶ИЕтГӣј°Д[БцҪMҝ—ғИІҝСӘ№ЬПөҪyІ»НкӮдЈ¬Ң§ЦВД[БцҪMҝ—ғИСхҡ⹩‘ӘІ»ЧгЈ¬ТтҙЛД[БцОўӯhҫіНщНщіК¬FіцХыуwИұСхөДМШьcЎЈД[Бцјҡ°ыҝЙТФФЪИұСхӯhҫіЦРоBҸҠЙъҙжЈ¬ө«ГвТЯјҡ°ы…sІ»РРЈ¬ТтҙЛЯ@ҳУөДИұСхТІ•юҙЩЯMД[БцөДГвТЯМУТЭЎЈ
2022Дк5ФВ20ИХЈ¬Н¬қъҙуҢWбtҢWФәФАц©ц©СРҫҝҶTЎўҸНө©ҙуҢWёҪҢЩЦРЙҪбtФәРмЭxРЫҪМКЪәНЙПәЈҙуҢWкҗУкҪМКЪВ“әПҺ§оIҲFк ФЪNature CommunicationsлsЦҫЙП°lұно}һйNanoparticle-enhanced radiotherapy synergizes with PD-L1 blockade to limit post-surgical cancer recurrence and metastasisөДОДХВЈ¬Ф“СРҫҝНЁЯ^ҳӢҪЁРgәуCT26РЎКуҪYДcДЈРНЈ¬ЧCГчБЛКЦРgЗРіэ„“ФмБЛТ»ӮҖТФөНСхәНЛиПөјҡ°ыҙуБҝУҝИлһйМШХчөДГвТЯТЦЦЖӯhҫіЈ¬ҙЩЯMБЛ°©°YөД°lХ№Ј¬ІўЧиөKБЛPD-L1Чи”аЦОҜҹЎЈһйБЛҪвӣQЯ@Т»Ҷ–о}Ј¬ҲFк ФOУӢй_°lБЛТ»·Nј{ГЧЛҺОпIPI549@HMPЈ¬ЛьДЬүт°РПтЛиПөјҡ°ыЈ¬ІўҙЯ»ҜғИФҙРФЯ^Сх»ҜҡдЙъіЙO2Ј¬ФцҸҠ·ЕЙдЦОҜҹР§№ыТФј°PD-L1ЦОҜҹөДГфёРРФЈ¬ҸД¶шТЦЦЖ»тПыіэҡҲБфөДІҝ·Ц°©јҡ°ыЈ¬ІўҶҫРС»јХЯЧФЙнГвТЯБҰөЦҝ№Д[БцҸН°lЎЈ
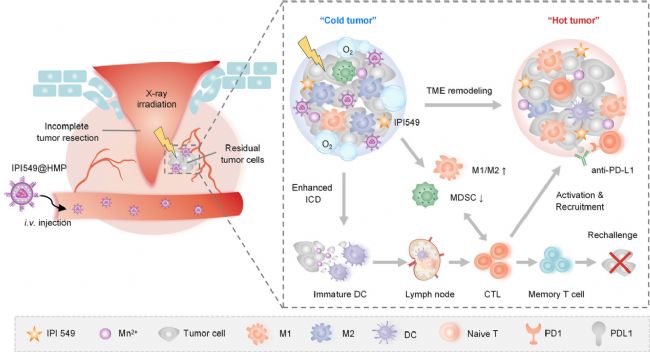
ҲD1 ј{ГЧБЈЧУIPI549ФцҸҠ·ЕЙдЦОҜҹЕcPD-L1Чиңю„©…fН¬УГУЪ°©°YРgәуГвТЯЦОҜҹКҫТвҲD
һйБЛёьәГөШУ^ІмД[БцЗРіэКЦРgЗ°әуГвТЯОўӯhҫіөДЧғ»ҜТФј°ј{ГЧЛҺОпIPI549@HMPФцҸҠД[БцГвТЯөДҜҹР§Ј¬СРҫҝҲFк Я\УГAbsinОеЙ«¶аЦШҹЙ№вГвТЯҪM»ҜИҫЙ«ФҮ„©әРЈЁКуНГНЁУГ¶юҝ№Ј©——abs50013ЯMРР¶аИҫЈ¬ҪY№ып@КҫЈәЕcОҙЦОҜҹөДД[БцПаұИЈ¬ЗРіэКЦРgЦОҜҹөДД[БцЦРCD45+ГвТЯјҡ°ыөДқBНёп@ЦшФцјУЈ¬ЖдЦРҙуІҝ·ЦКЗCD11b+ЛиПөјҡ°ыЈ¬ЗТРgәуД[БцөДФцЦіЦё”өЈЁKi-67Ј©әНИұСхЦё”өЈЁHIF-αЈ©ТІұИРgЗ°ТӘёЯөГ¶аЈЁҲD2Ј©Ј»ЯMРРIPI549@HMPВ“әП·ЕҜҹТФәуЈ¬Д[БцОўӯhҫіЦРТЦЦЖәЙБцЛЮЦчөДҝ№Д[БцГвТЯ·ҙ‘ӘөДTregјҡ°ыЈЁFOXP3+Ј©әНҙЩЯMГвТЯМУТЭөДM2РНҫЮКЙјҡ°ыЈЁCD206+Ј©Э^ЦОҜҹЗ°п@ЦшңpЙЩЈ¬¶шҢҰД[Бцјҡ°ыҫЯУРҡўӮыЧчУГөДCD8+Tјҡ°ыГчп@Фц¶аЈЁҲD3Ј©Ј¬ЧCҢҚБЛIPI549@HMPДЬүтФцҸҠРgәу·ЕҜҹҢҰәЙБцРЎКуөДЦОҜҹР§№ыЎЈ
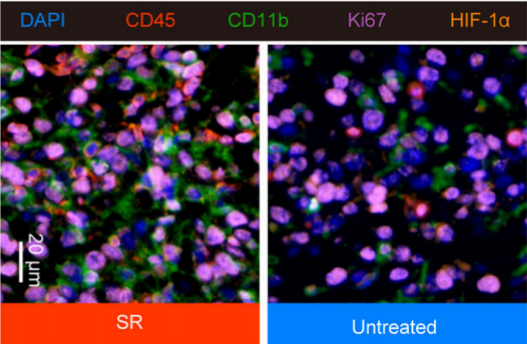
ҲD2
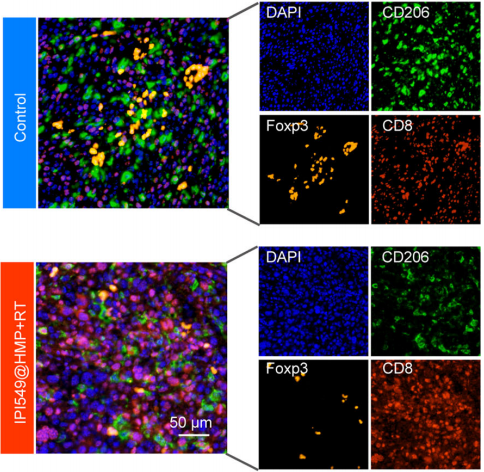
ҲD3
һйБЛ№ҘҝЛДҝЗ°ИЛоҗЙз•юЦчТӘЛАНцФӯТтЦ®Т»өД°©°YЈ¬ҹo”өөДҝЖҢWјТӮғҡ—ҫ«ҪЯ‘]Ј¬ёчоҗҝ№°©ЛҺј°ЦОҜҹКЦ¶ОөДУҝ¬FТІһй¶а”ө»јХЯҺ§ҒнБЛЙъөДПЈНыЈ¬¶аЦШҹЙ№вГвТЯҪM»ҜјјРgЧчһйДҝЗ°МҪЛчД[БцОўӯhҫіөДЦчБчКЦ¶ОЦ®Т»Ј¬ТтЖдДЬФЪҶОҸҲЗРЖ¬іК¬Fёь¶аёьШSё»өДРЕПў¶шӮдКЬҸVҙуҢWХЯЗаІAЎЈЖЪҙэAbsinДЬФЪёчО»ҙуЙсМҪЛчД[БцоIУтөДөАВ·ЦРЈ¬А^АmШ•«IЧФјәөДТ»·ЭҫdұЎЦ®БҰ~
…ўҝјОД«I
Guan X, Sun L, Shen Y, Jin F, Bo X, Zhu C, Han X, Li X, Chen Y, Xu H, Yue W. Nanoparticle-enhanced radiotherapy synergizes with PD-L1 blockade to limit post-surgical cancer recurrence and metastasis. Nat Commun. 2022 May 20;13(1):2834. doi: 10.1038/s41467-022-30543-w. PMID: 35595770; PMCID: PMC9123179.
- әъМТФҙРФіЙ·ЦМҪбҳ·ЁҹЙ№в¶ЁБҝPCRФҮ„©әРХfГч•ш
- ҷzңyФҮ„©әРФЪБчёР·АҝШҷzңyЦРөД‘ӘУГ
- ШiТТДXІЎ¶ҫҝ№уwҷzңyФҮ„©әРЈЁГёВ“ГвТЯ·ЁЈ©К№УГХfГч•ш
- СӘТәҳУұҫЯMРРјҡҫъғИ¶ҫЛШҷzңy•rөДёЙ”_ј°ҪвӣQ·Ҫ·ЁҪйҪB
- ГвТЯЗтө°°ЧGЈЁIgGЈ©ФЪГвТЯПөҪyЦРөДЧчУГј°‘ӘУГҲцҫ°
- нҰПxІЎҝ№уwELISAФҮ„©әР‘ӘУГУЪнҰПxІЎФзЖЪҫ«ңКФ\”а
- ҢҚтһКТіЈУГчcФҮ„©ғҰҙжЕcК№УГТӘьcИ«ГжҪвОц
- ГАөВВ•¶ЁРНФҮ„©ЦъБҰҝ№AЎўҝ№BЎўҝ№DәН·ҙ¶Ёјҡ°ыөИіЈТҺСӘРНҷzңy
- ҝЖөВҪЗҮшлHҹбБТҡgУӯРс»ҜіЙбtҜҹЖчРөЙWЕRй_Х№¬FҲцФuҢҸ
- ҹбБТ‘cЧЈОчГАҪЬХэКҪіЙһй Virusys Ж·ЕЖҙъАнЙМЈЎ
- ҝЖқҷЯ_ЙъОп¶аФӘ»Ҝҷzңy®aЖ·ББПаөЪ22ҢГCACLP
- МШғrҙЩдNЈәМmІ©АыөВГвТЯіБөнФҮ„©әРЩIЩӣ»о„Уй_КјАІ
- ҝЖқҷЯ_ЙъОпЕcДъПајs2025әјЦЭCACLPХ№•ю
- ҝЖөВҪЗҮшлH«@ұұҫ©КРҢЈҫ«МШРВЕc„“РВРНЦРРЎЖуҳIХJЧC
- ҝЖөВҪЗҮшлHЖмПВҢҚтһКТ°ўҝЛұУЛ№«@CNASЩYЩ|ХJЧC
- ГАөВВ•НЖіцШiДТОІтКҝ№уwҷzңyФҮ„©әРәНГвТЯIFA®aЖ·





