腸道微生物群-免疫系統-腦軸:腸道微生物對大腦發育的影響
早產兒(<28周&<1000g)往往面臨著圍產期腦白質損傷的巨大風險,雖然腸道微生物與生命早期的發育有關,但目前研究人員并不是非常清楚早產兒個體中腸道微生物-免疫系統-腦軸之間的詳細關聯。近日,一篇發表在Cell Host & Microbe(IF 15.127)上題為“Aberrant gut microbiota-immune-brain axis development in premature neonates with brain damage”的研究報告中,來自維也納大學的研究團隊發現了一種治療大腦外損傷的早期療法的可能性靶點,腸道微生物在其中扮演關鍵角色,研究人員發現,胃腸道中克雷伯菌(Klebsiella)的過度生長或與早產兒特定免疫細胞數量的增加及神經性損傷的發生直接相關。

研究材料
糞便和血液樣本,早產兒分娩后第3天、第7天、第14天,然后每兩周取樣一次,直至足月。
技術路線
· 步驟1:描述患者的神經生理發育特征;
· 步驟2:與圍產期腦白質損傷相關的T細胞動態發育;
· 步驟3:微生物群與腦損傷的相關性;
· 步驟4:SCFAs與腦損傷的相關性;
· 步驟5:篩選與腦損傷相關的生物標志物。
研究結果
1. 神經生理學特征預測腦損傷
2017年9月至2019年6月期間,研究團隊共招募了60名極早產兒。為了量化腦損傷,研究人員對神經影像學的結果進行Kidokoro評分,正如預期的那樣,嚴重腦損傷嬰兒的Kidokoro評分更高;為了表征患者的神經生理發育,采用振幅整合腦電圖(aEEG)評估,觀察到神經生理學成熟的一致趨勢,其特征是一個初始靜止階段,DV(不連續電壓,discontinuousvoltage)是主要的aEEG模式,隨后是一段神經生理學成熟期,在此階段CV(連續電壓,continuousvoltage)持續增加,最終在足月年齡時趨于穩定。因此,腦損傷嬰兒成熟期延遲,神經發育受到短暫抑制,且顱氧飽和度的不穩定性增加,這些神經生理學特征均可預測腦白質損傷(PWMI),并且在病理學中起重要作用。

圖1 極早產兒的神經生理學發育
2. 腦損傷早產兒表現出促炎性極化T細胞反應
盡管T細胞是腸道微生物組和大腦之間的重要聯系,但它們在生命早期的個體發育以及它們與極早產兒圍產期腦損傷的關系仍然知之甚少。為了研究與圍產期腦損傷相關的T細胞動力學的時間變化,研究人員利用熒光激活細胞分選(FACS)研究了T細胞亞群,結果發現γδ T細胞的增加可能與PWMI的發病機制有關。這種細胞反應起初與IL-8、IL-17a、VEGF-A和PDGF-BB的分泌相關。隨后,VEGF-A和γδ T細胞之間的密切聯系持續存在,而神經保護劑PDGF-BB和BDNF的進一步分泌在患有嚴重腦損傷的嬰兒中受到抑制。
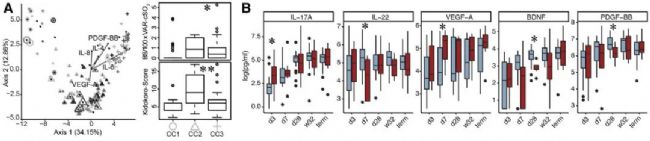
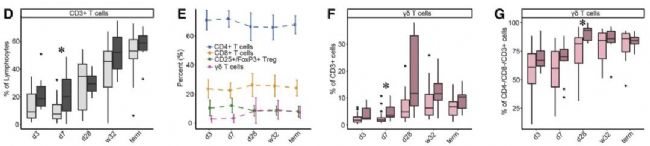
圖2 極早產兒的T細胞發育
3. Klebsiella的過度生長與腦損傷有關
微生物群是免疫耐受的重要發起者,因為微生物抗原的性質和數量決定了淋巴細胞的反應。因此研究人員采用16s rRNA測序來量化早產兒糞便樣本中的細菌數量及群落組成。隨著分娩后時間的推移,細菌的數量逐漸增加,并在分娩后2周趨于穩定。其中,從患有嚴重腦損傷的早產兒糞便中分離出來的克雷伯菌與腦損傷存在顯著的相關性,該菌株基因組具有幾種潛在的毒力因子以及支持其在患有腸炎的腸道中定殖的基因。因此,Klebsiella在腸道中的過度生長與神經病理學相關。

圖3 極早產兒的微生物組群及其與腦損傷對應的多樣性
4. 腸道菌群和代謝物之間的動態變化與腦損傷之間的潛在聯系
雖然健康的成人腸道被認為是一個很大程度上缺氧的環境,但據報道早產兒的胃腸道部分缺氧,因此在產后發育過程中必須過渡到缺氧狀態。16s結果顯示,隨著時間的推移,專性厭氧類群的增加,反映了這種向缺氧的轉變。
在缺氧情況下,細菌必須通過底物的磷酸化獲得能量,而在腸道中,這通常是通過將膳食或宿主衍生化合物發酵成短鏈脂肪酸(SCFAs)來實現的,短鏈脂肪酸可作為神經系統和免疫系統信號分子。因此,研究人員收集了分娩前和分娩后28天的樣本進行代謝組學檢測,評估SCFA與嚴重腦損傷的相關性。結果發現,在分娩前期,腦損傷患者的
 水平顯著升高,
水平顯著升高, 水平略微升高,但在以后的時間點沒有顯著差異,表明SCFA在早期向腸道缺氧過渡可能與腦損傷有關。
水平略微升高,但在以后的時間點沒有顯著差異,表明SCFA在早期向腸道缺氧過渡可能與腦損傷有關。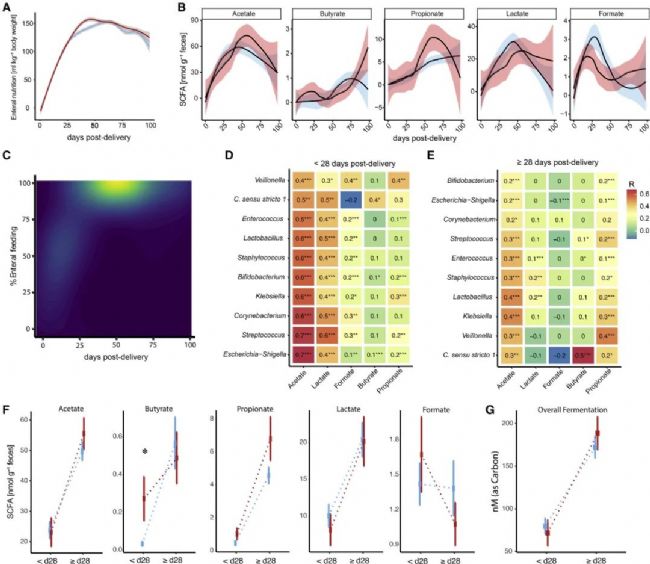
圖4 極早產兒糞便中的SCFAs
5. 可以預測PWMI的腸道微生物-免疫系統-腦軸的生物標志物
為了確定可靠的腦損傷生物標志物,研究人員對微生物組、代謝組、臨床、免疫學和神經生理學數據進行了綜合分析。腦白質損傷的最強指標是Klebsiella水平升高、γδ T細胞的增加,以及促進T細胞生成的幾種細胞因子和趨化因子的增加。幾種數據集之間的相關性分析表明,Klebsiella與γδ T細胞、免疫因子(VEGF-A、PDGF-BB和BDNF)顯著相關。
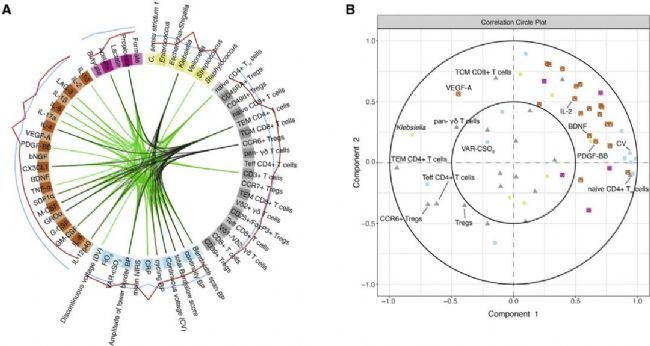
圖5 極早產兒腸道微生物群免疫腦軸與腦損傷生物標志物
小編小結
腸道、大腦和免疫系統的早期發展是密切相關的,早產兒遭受圍產期腦白質損傷的風險很大,但具體機制尚未知。本研究分析了60例接受了包括抗生素和益生菌在內的標準醫院護理的極度早產兒的腸道菌群、免疫學和神經生理發育情況,結果發現患有嚴重腦損傷的嬰兒表現出促炎性T細胞極化,其表現為外周血中γδ T細胞的擴張,并在分娩后不久由升高的IL-17a和VEGF-a分泌驅動。隨后,這些嬰兒的神經生理學成熟開始延遲,其特征是皮層電位受到抑制,頭顱氧飽和度增加不穩定性,以及神經保護劑PDGF-BB和BDNF分泌不足。腸道中的克雷伯菌過度生長是促使與嚴重腦損傷相關的獨特且非常穩定的微生物組的關鍵。因此,我們得出結論,Klebsiella參與腸道微生物群-免疫系統-腦軸的調節,并可能加重PWMI。
中科優品推薦
【中科新生命】全面推出腸道微生物群-免疫系統多組學解決方案,多角度、多層次、全方位深入挖掘腸道菌群和免疫系統之間的關聯性,并結合表型結果,擬幫助科研人員開發一種新型干預性措施的潛在靶點。
腸-免疫-靶軸系統研究方案
· 16s/宏基因組----腸道微生物的組成及改變
· 免疫代謝組----腸道微生物產生的用于調控機體免疫的代謝物
· 免疫因子組----腸道微生物如何影響機體免疫
· 轉錄/蛋白質組----對終端靶器官應對炎癥響應機制的系統描述
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com






