近期生物層干涉技術(BLI)的CNS正刊應用集錦
上半年CNS正刊40篇,這個技術要逆天!
近幾年來,引用生物層干涉技術(BLI)的CNS正刊數量(注意是正刊哦!)是噌噌噌的一路上漲。從2016-2018年三年52篇,到2019年的27篇,以及2020年的51篇,而就在剛剛過去的2021年上半年,發表數量就已經突破了40篇!
在這些CNS文章中,有相當一部分是應用BLI技術開展病毒(主要為新冠病毒)相關研究,包括新冠疫苗、中和抗體以及病理機制等。這些精彩文章陳老濕在之前的微信中已經介紹了很多,估計粉絲們也差不多要審美疲勞了。除去這類文章,其他有趣且好玩的酷文也不少(比如最近很熱的蛋白質計算機設計),陳老濕就挑幾篇給大家嘮嘮。
➤ 新冠疫苗血小板減少和血栓形成機制研究
麥克馬斯特大學【1】
新冠疫苗的安全性仍是重中之重,牛津-阿斯利康新冠疫苗ChAdOx1產生的相關血小板減少癥和血管等不良事件導致一些國家限制其使用。該研究闡釋了部分新冠疫苗誘導的抗體可能會如何導致“疫苗誘導免疫血栓性血小板減少癥”(VITT)這一罕見癥狀。
腺病毒載體疫苗會引發血小板減少和血栓形成(VITT)。VITT 類似于肝素誘導的血小板減少癥(HIT),因為它與針對血小板因子4(PF4)的血小板激活抗體有關。加拿大頂尖學府McMaster大學在Nature發表文章,發現了VITT與針對血小板因子4(PF4)的抗體有關。研究人員應用生物層干涉技術(Octet RED96),證明VITT誘導的PF4抗體對PF4和PF4/肝素復合物的結合能力比HIT誘導的抗體更強。VITT抗體在與PF4上的結合位點與肝素相同,使PF4四聚體聚集并形成免疫復合物,通過FcγRIIa結合產生Fc依賴性血小板活化。
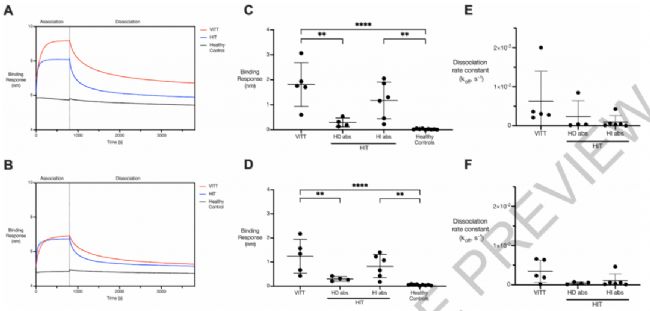 用鏈霉親和素傳感器固化PF4或者PF4/肝素,與VITT,HIT病人血清進行檢測,圖A,C,E為固化PF4分別檢測各種血清樣品,圖B,D,F為固化PF4/肝素復合物分辨檢測跟中血清樣品。
用鏈霉親和素傳感器固化PF4或者PF4/肝素,與VITT,HIT病人血清進行檢測,圖A,C,E為固化PF4分別檢測各種血清樣品,圖B,D,F為固化PF4/肝素復合物分辨檢測跟中血清樣品。
AB為原始的結合解離圖,CD為各種病人的血清樣品檢測信號,EF為各種病人血清樣品的解離速率比較。
陳老濕曰
新冠疫苗的安全性問題事關所有人的健康安全。BLI技術的厲害之處就是能夠通過比較生物分子間的結合和解離速率,準確且定量化分析相互作用過程中的差異變化,而傳統的ELISA技術是完全無法提供相關數據的。
➤ CAR-T治療實體瘤重大突破,只殺癌細胞,不傷健康細胞
加州大學舊金山分校【2】
CAR-T已經在治療血液腫瘤中體現了良好的療效,但在治療實體瘤方面還有待突破。其中一個關鍵瓶頸是如何區分正常組織少量表達的和腫瘤中高表達的腫瘤標志物,以降低“誤殺”導致的副作用。
這篇Science文章的作者以HER2為靶點在CAR-T細胞上共表達了CAR(嵌合抗原受體)和低親和力的合成缺口(synNotch) 受體,synNotch與HER2結合可以激活高親和力的CAR的表達。這樣使得synNotch作為HER2密度濾器,只有HER2密度達到某個閾值才大量激活CAR的表達,達到特異性殺傷腫瘤細胞的目的,此謂之“超靈敏激活(ultrasensitive)”。
為了構建synNotch受體和CARs,研究者制作了一系列抗HER2單鏈抗體,親和度跨越100倍范圍(解離常數在2.0-200 nM之間),并應用Octet系統進行快速且準確的測定(圖D)。
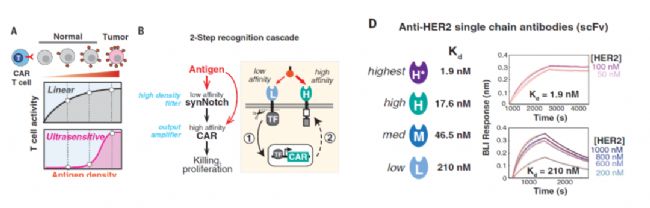 A:超靈敏激活(ultrasensitive)是T細胞活性與抗原呈現S曲線
A:超靈敏激活(ultrasensitive)是T細胞活性與抗原呈現S曲線
B:synNotch可以激活CAR表達,作為抗原密度的過濾器
C:Octet RED384檢測,CAR的親和力為1.9nM,而synNotch親和力為210nM(用GST傳感器固化ScFv與HER2進行結合解離)
陳老濕曰
Octet系統可以準確區分不同樣品間很小的親和力差別。特別是樣品量較多的情況下,Octet系統快速準確的特點可以發揮的淋漓盡致。
➤ 體外蛋白質設計
華盛頓大學(Nature【3】+ Science【4】)
上周,陳老濕的朋友圈被一條內容為“兩款新型AI系統精準預測蛋白結構”的文章刷屏。這兩款AI系統,一個是DeepMild公司的AlphaFold2,另一個就是大神David Baker開發的RoseTTAFold軟件系統。

Baker教授的研究內容陳老濕也寫過好幾期了,實在是牛的一塌糊涂。今年又是一篇Nature加一篇Science,妥妥的YYDS。
在Nature文章中,大神設計了一種能特異性識別靶點的高靈敏度生物傳感器,其本質是一種人工設計的蛋白復合物,只需要把這個生物傳感器與樣品混合,就可以直接測試諸如病毒、抗體等物質。
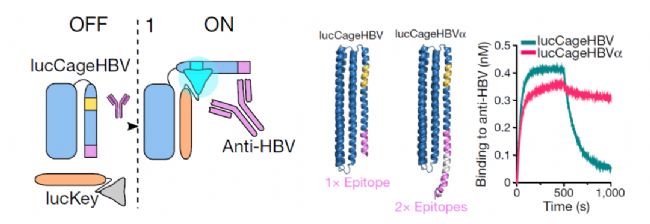 左圖:HBV抗體識別生物傳感器由籠子蛋白和門閂蛋白組成lucCage,門閂蛋白上由激發熒光素酶的蛋白序列(黃色)和識別靶點的序列(粉色)。當lucCage結合靶蛋白(anti-HBV抗體)時,門閂蛋白構象變化,鑰匙蛋白(lucKey,橙色)與籠子蛋白結合,熒光素酶(灰色)同時被門閂蛋白激活,產生熒光。
左圖:HBV抗體識別生物傳感器由籠子蛋白和門閂蛋白組成lucCage,門閂蛋白上由激發熒光素酶的蛋白序列(黃色)和識別靶點的序列(粉色)。當lucCage結合靶蛋白(anti-HBV抗體)時,門閂蛋白構象變化,鑰匙蛋白(lucKey,橙色)與籠子蛋白結合,熒光素酶(灰色)同時被門閂蛋白激活,產生熒光。
中圖:設計的lucCage蛋白,帶有一個(lucCageHBV)或者兩個HBV抗體表位(lucCageHBVα)
右圖:Octet檢測兩種lucCage與HBV抗體的結合。發現帶有兩個表位的lucCage與靶點結合更強
在另一篇Science發表的文章中,Baker團隊設計了一種抗體納米籠結構,可以控制抗體的對稱性和多價性,從而掌握抗體與靶點的親和力。抗體納米籠是由抗體和Fc結合蛋白多聚而成。
 左圖:通過控制Fc結合蛋白的多聚程度,來控制納米籠的結構。紫色為抗體,灰色為Fc結合蛋白。
左圖:通過控制Fc結合蛋白的多聚程度,來控制納米籠的結構。紫色為抗體,灰色為Fc結合蛋白。
右圖:用鏈霉親和素傳感器固化生物素化的IgG1和Fc,與設計的Fc結合序列結合解離檢測動力學參數(Octet RED96)
陳老濕曰
人工智能(AI)模擬雖然可以大大增加效率,并且預測蛋白結構的準確性也越來越高,但最終蛋白實際的活性和功能還是要依靠分子互作分析系統等生物物理學手段進行分析和驗證。
-參考文獻-
【1】Antibody epitopes in vaccine-induced immune thrombotic thrombocytopenia
Angela Huynh, John G Kelton[…]Ishac Nazy
Nature , 1–7
【2】T cell circuits that sense antigen density with an ultrasensitive threshold. Science 371, 1166–1171 (2021)
【3】De novo design of modular and tunable protein biosensors. Nature 591 , 482–487
【4】Designed proteins assemble antibodies into modular nanocages. DOI: 10.1126/science.abd9994
近幾年來,引用生物層干涉技術(BLI)的CNS正刊數量(注意是正刊哦!)是噌噌噌的一路上漲。從2016-2018年三年52篇,到2019年的27篇,以及2020年的51篇,而就在剛剛過去的2021年上半年,發表數量就已經突破了40篇!
在這些CNS文章中,有相當一部分是應用BLI技術開展病毒(主要為新冠病毒)相關研究,包括新冠疫苗、中和抗體以及病理機制等。這些精彩文章陳老濕在之前的微信中已經介紹了很多,估計粉絲們也差不多要審美疲勞了。除去這類文章,其他有趣且好玩的酷文也不少(比如最近很熱的蛋白質計算機設計),陳老濕就挑幾篇給大家嘮嘮。
➤ 新冠疫苗血小板減少和血栓形成機制研究
麥克馬斯特大學【1】
新冠疫苗的安全性仍是重中之重,牛津-阿斯利康新冠疫苗ChAdOx1產生的相關血小板減少癥和血管等不良事件導致一些國家限制其使用。該研究闡釋了部分新冠疫苗誘導的抗體可能會如何導致“疫苗誘導免疫血栓性血小板減少癥”(VITT)這一罕見癥狀。
腺病毒載體疫苗會引發血小板減少和血栓形成(VITT)。VITT 類似于肝素誘導的血小板減少癥(HIT),因為它與針對血小板因子4(PF4)的血小板激活抗體有關。加拿大頂尖學府McMaster大學在Nature發表文章,發現了VITT與針對血小板因子4(PF4)的抗體有關。研究人員應用生物層干涉技術(Octet RED96),證明VITT誘導的PF4抗體對PF4和PF4/肝素復合物的結合能力比HIT誘導的抗體更強。VITT抗體在與PF4上的結合位點與肝素相同,使PF4四聚體聚集并形成免疫復合物,通過FcγRIIa結合產生Fc依賴性血小板活化。

AB為原始的結合解離圖,CD為各種病人的血清樣品檢測信號,EF為各種病人血清樣品的解離速率比較。
陳老濕曰
新冠疫苗的安全性問題事關所有人的健康安全。BLI技術的厲害之處就是能夠通過比較生物分子間的結合和解離速率,準確且定量化分析相互作用過程中的差異變化,而傳統的ELISA技術是完全無法提供相關數據的。
➤ CAR-T治療實體瘤重大突破,只殺癌細胞,不傷健康細胞
加州大學舊金山分校【2】
CAR-T已經在治療血液腫瘤中體現了良好的療效,但在治療實體瘤方面還有待突破。其中一個關鍵瓶頸是如何區分正常組織少量表達的和腫瘤中高表達的腫瘤標志物,以降低“誤殺”導致的副作用。
這篇Science文章的作者以HER2為靶點在CAR-T細胞上共表達了CAR(嵌合抗原受體)和低親和力的合成缺口(synNotch) 受體,synNotch與HER2結合可以激活高親和力的CAR的表達。這樣使得synNotch作為HER2密度濾器,只有HER2密度達到某個閾值才大量激活CAR的表達,達到特異性殺傷腫瘤細胞的目的,此謂之“超靈敏激活(ultrasensitive)”。
為了構建synNotch受體和CARs,研究者制作了一系列抗HER2單鏈抗體,親和度跨越100倍范圍(解離常數在2.0-200 nM之間),并應用Octet系統進行快速且準確的測定(圖D)。

B:synNotch可以激活CAR表達,作為抗原密度的過濾器
C:Octet RED384檢測,CAR的親和力為1.9nM,而synNotch親和力為210nM(用GST傳感器固化ScFv與HER2進行結合解離)
陳老濕曰
Octet系統可以準確區分不同樣品間很小的親和力差別。特別是樣品量較多的情況下,Octet系統快速準確的特點可以發揮的淋漓盡致。
➤ 體外蛋白質設計
華盛頓大學(Nature【3】+ Science【4】)
上周,陳老濕的朋友圈被一條內容為“兩款新型AI系統精準預測蛋白結構”的文章刷屏。這兩款AI系統,一個是DeepMild公司的AlphaFold2,另一個就是大神David Baker開發的RoseTTAFold軟件系統。

Baker教授的研究內容陳老濕也寫過好幾期了,實在是牛的一塌糊涂。今年又是一篇Nature加一篇Science,妥妥的YYDS。
在Nature文章中,大神設計了一種能特異性識別靶點的高靈敏度生物傳感器,其本質是一種人工設計的蛋白復合物,只需要把這個生物傳感器與樣品混合,就可以直接測試諸如病毒、抗體等物質。

中圖:設計的lucCage蛋白,帶有一個(lucCageHBV)或者兩個HBV抗體表位(lucCageHBVα)
右圖:Octet檢測兩種lucCage與HBV抗體的結合。發現帶有兩個表位的lucCage與靶點結合更強
在另一篇Science發表的文章中,Baker團隊設計了一種抗體納米籠結構,可以控制抗體的對稱性和多價性,從而掌握抗體與靶點的親和力。抗體納米籠是由抗體和Fc結合蛋白多聚而成。

右圖:用鏈霉親和素傳感器固化生物素化的IgG1和Fc,與設計的Fc結合序列結合解離檢測動力學參數(Octet RED96)
陳老濕曰
人工智能(AI)模擬雖然可以大大增加效率,并且預測蛋白結構的準確性也越來越高,但最終蛋白實際的活性和功能還是要依靠分子互作分析系統等生物物理學手段進行分析和驗證。
-參考文獻-
【1】Antibody epitopes in vaccine-induced immune thrombotic thrombocytopenia
Angela Huynh, John G Kelton[…]Ishac Nazy
Nature , 1–7
【2】T cell circuits that sense antigen density with an ultrasensitive threshold. Science 371, 1166–1171 (2021)
【3】De novo design of modular and tunable protein biosensors. Nature 591 , 482–487
【4】Designed proteins assemble antibodies into modular nanocages. DOI: 10.1126/science.abd9994
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com






