AD疾病神經元過度激活和睡眠障礙或與MCH功能紊亂關聯詳解
阿爾茨海默病(AD)患者前驅期存在睡眠障礙同時伴有突發性的癲癇樣放電。在Aβ沉積小鼠模型中,在睡眠和麻醉等低覺醒狀態下皮層和海馬神經元的過度活躍更為突出。神經穩態可塑性參與調控多種重要的生理過程,神經元的興奮性處于持續改變狀態時主動啟動程序化事件,對突觸功能進行調節以對抗神經活性的持續性改變,維持正常的神經功能,然而其異常可導致神經網絡的興奮-抑制失衡。
Pmch基因編碼黑色素聚集激素(MCH)前體多肽,加工合成MCH,主要表達在外側下丘腦,在海馬幾乎無表達。海馬注射MCH可促進記憶,示蹤實驗發現下丘腦MCH陽性神經元投射到海馬CA1區,在睡眠期間被激活。
2023年5月15日比利時腦和疾病VIB研究中心Joris de Wit研究團隊發現了在AD疾病早期海馬MCH表達上調介導異常的突觸可塑性,并引起睡眠結構的紊亂。

1、AD模型早期存在異常的穩態突觸可塑性
研究人員通過電生理實驗發現2月齡和3月齡App-NL-G-F 小鼠海馬CA1腦區錐體神經元自發性興奮性突觸后電流增加(該時期還未出現Aβ沉積),然而4月齡該品系小鼠自發性興奮性突觸后電流減弱,這種突觸可塑性在6月齡增強。免疫熒光實驗發現4月齡App-NL-G-F 小鼠海馬CA1腦區神經元激活減少,在6月齡增加激活增多。
單細胞測序技術發現3.5月齡App-NL-G-F 小鼠海馬CA1腦區中200個差異性表達基因中約三分之一與突觸可塑性有關,其中Gria1和Gria2編碼AMPA受體(AMPAR)亞基表達降低,表達上調最為顯著的是Pmch。這些電生理、分子實驗證實App-NL-G-F 小鼠海馬CA1腦區錐體神經元在3月到4月齡之間發生穩態的突觸可塑性。
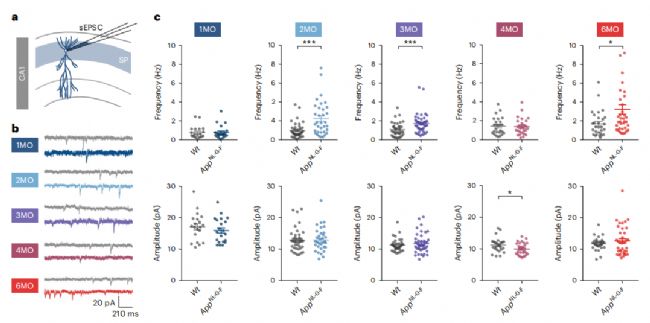
圖1:App-NL-G-F 小鼠海馬突觸可塑性存在時間依賴性變化
2、海馬MCH調控穩態突觸可塑性
為進一步證實MCH在海馬突觸可塑性中的作用,離體細胞實驗發現孵育MCH可減弱海馬神經元興奮性突觸后電流,GluA1絲氨酸845位點磷酸化水平表達降低,在給與GABAB受體激動劑后可明顯阻斷MCH誘發的突觸強度減弱效應。3月齡App-NL-G-F 小鼠CA1腦區錐體神經元孵育MCH后也可明顯減弱微小興奮性突觸后電流。
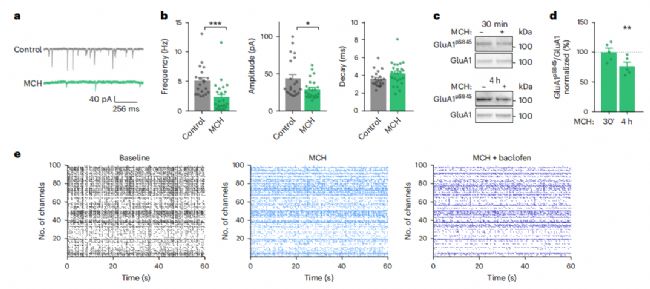
圖2.海馬MCH調控穩態突觸可塑性
3、AD早期海馬 MCH 軸突形態出現障礙
在經歷睡眠剝奪后出現睡眠反彈過程中,野生型小鼠海馬腦區MCH陽性神經元激活增多,但在App-NL-G-F 小鼠并沒有出現這種增強。進一步記錄不同睡眠時期時長,結果發現App-NL-G-F 小鼠快速眼動睡眠時間減少,但非快速眼動睡眠和覺醒時期兩個階段維持時間未發生變化。
免疫熒光實驗發現6月齡App-NL-G-F 小鼠海馬腦區MCH陽性信號面積增多,在AD患者中也能觀察到類似變化。在睡眠剝奪和睡眠反彈期野生型小鼠海馬腦區MCH陽性信號個數增多,然而App-NL-G-F 小鼠并不存在這種變化,這些結果表明App-NL-G-F 小鼠MCH陽性軸突形態出現障礙。
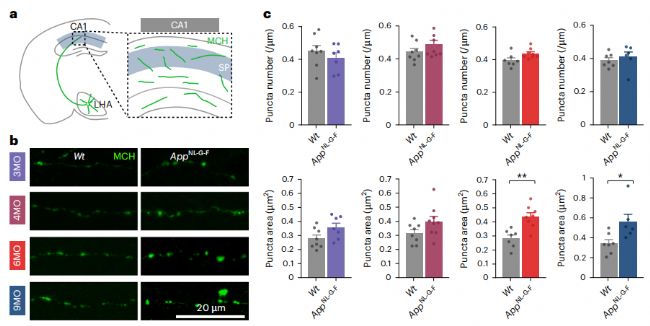
圖3:AD早期海馬 MCH 軸突形態出現紊
總結
本文揭示了AD疾病早期海馬MCH功能紊亂后引起異常的興奮性神經元驅動作用,誘發穩態突觸可塑性障礙,并破壞睡眠結構。


想了解更多內容,獲取相關咨詢請聯系
電 話:+86-0731-84428665
伍經理:+86-180 7516 6076
徐經理:+86-138 1744 2250
郵 箱:consentcs@163.com
官 網:www.consentcs.com





