Nature最新研究綜述:蛋白基因組及其臨床應(yīng)用的光明前景
蛋白基因組(proteogenomics):將蛋白質(zhì)組與基因組等組學(xué)分析手段進(jìn)行整合,用以系統(tǒng)地檢測腫瘤組織等生物樣本中分子的狀態(tài)與變化,進(jìn)而實現(xiàn)從基因變異到蛋白功能改變與調(diào)控的完整描繪,用以發(fā)現(xiàn)疾病的分型、標(biāo)志物及藥物靶點(diǎn),探索更精準(zhǔn)的疾病診斷與治療手段。近三年,Nature、Cell、Cancer Cell等頂級期刊陸續(xù)發(fā)表了近20篇基于蛋白基因組的癌癥精準(zhǔn)醫(yī)學(xué)研究成果。繼2021年4月,Cell以“The next horizon in precision oncology: Proteogenomics to inform cancer diagnosis and treatment”(點(diǎn)擊閱讀)發(fā)表綜述觀點(diǎn)文章后,Nature Reviews Cancer (IF 60)于近日再次綜述了癌癥蛋白基因組的研究進(jìn)展及其未來的光明應(yīng)用前景。
基因組分析推動了對驅(qū)動突變的識別和靶向治療的發(fā)展,對癌癥的治療產(chǎn)生了巨大的影響。然而,腫瘤中絕大多數(shù)體細(xì)胞突變和拷貝數(shù)變異的功能仍然未知,并且對靶向治療產(chǎn)生耐藥性的原因以及克服它們的方法也不清楚。基于質(zhì)譜的蛋白質(zhì)組學(xué)的改進(jìn),可以直接檢查基因組畸變的后果,提供對腫瘤組織的深入和定量的表征。蛋白質(zhì)及其翻譯后修飾與基因組、表觀基因組和轉(zhuǎn)錄組數(shù)據(jù)的整合,構(gòu)成了精準(zhǔn)癌癥解析的新領(lǐng)域,并且已經(jīng)帶來了新的生物學(xué)認(rèn)知和診斷知識,展示出了對腫瘤惡性轉(zhuǎn)化和治療結(jié)果深入理解的巨大潛力。該篇綜述描述了蛋白基因組的最新進(jìn)展,在一系列癌癥研究中的主要發(fā)現(xiàn),以及相關(guān)的分析方法與技術(shù)。蛋白基因組在轉(zhuǎn)化研究中的應(yīng)用和免疫癌癥學(xué)領(lǐng)域正在迅速興起,其完全融入治療試驗和臨床應(yīng)用的前景看起來是一片光明的。
基因組分析推動了對驅(qū)動突變的識別和靶向治療的發(fā)展,對癌癥的治療產(chǎn)生了巨大的影響。然而,腫瘤中絕大多數(shù)體細(xì)胞突變和拷貝數(shù)變異的功能仍然未知,并且對靶向治療產(chǎn)生耐藥性的原因以及克服它們的方法也不清楚。基于質(zhì)譜的蛋白質(zhì)組學(xué)的改進(jìn),可以直接檢查基因組畸變的后果,提供對腫瘤組織的深入和定量的表征。蛋白質(zhì)及其翻譯后修飾與基因組、表觀基因組和轉(zhuǎn)錄組數(shù)據(jù)的整合,構(gòu)成了精準(zhǔn)癌癥解析的新領(lǐng)域,并且已經(jīng)帶來了新的生物學(xué)認(rèn)知和診斷知識,展示出了對腫瘤惡性轉(zhuǎn)化和治療結(jié)果深入理解的巨大潛力。該篇綜述描述了蛋白基因組的最新進(jìn)展,在一系列癌癥研究中的主要發(fā)現(xiàn),以及相關(guān)的分析方法與技術(shù)。蛋白基因組在轉(zhuǎn)化研究中的應(yīng)用和免疫癌癥學(xué)領(lǐng)域正在迅速興起,其完全融入治療試驗和臨床應(yīng)用的前景看起來是一片光明的。

綜述內(nèi)容
癌癥蛋白基因組學(xué),將基于質(zhì)譜的蛋白質(zhì)豐度和翻譯后修飾 (PTM) 測量與基因組、表觀基因組和轉(zhuǎn)錄組數(shù)據(jù)相結(jié)合的方法,用以分析來自腫瘤模型和臨床的腫瘤樣本。基因組和表觀基因組為可能發(fā)生的事情提供了藍(lán)圖,而蛋白質(zhì)組提供了對發(fā)生的事情的確定,因為蛋白質(zhì)及其修飾是生物表型的主要最終決定者。基因組和轉(zhuǎn)錄分析提供了對基因組改變的特征和潛在影響的解讀,而蛋白質(zhì)組提供了有關(guān)蛋白質(zhì)調(diào)節(jié)和響應(yīng)這些變化的信號的直接信息。重要的是,蛋白質(zhì)組還提供了對 PTM 的深入、定量的分析,例如磷酸化、乙酰化和泛素化。這些分析可以檢測由基因組變化或更接近的影響驅(qū)動的信號網(wǎng)絡(luò),并可以提供有關(guān)影響細(xì)胞信號、位置、分子復(fù)合物形成、翻譯和穩(wěn)定性的修飾的信息(DNA或mRNA 分析無法揭示的失調(diào))。以及通過檢查激酶、泛素連接酶和其他酶及其PTM 異常表達(dá)的信息學(xué)方法,可以將注意力集中在可立即成藥的靶標(biāo)上,或集中精力開發(fā)新療法。因此, 蛋白質(zhì)組學(xué)有可能為治療反應(yīng)提供重要見解,并在臨床環(huán)境中診斷多種耐藥來源。從目前的研究及臨床應(yīng)用來看,基因組測序?qū)υ\斷、預(yù)后和治療決策的影響比最初希望的要小,免疫癌癥學(xué)方法也需要考慮癌癥基因組和免疫系統(tǒng)之間的相互作用。綜上所述,蛋白基因組提供了新的機(jī)會。
1. 蛋白基因組的研究進(jìn)展
在乳腺癌、結(jié)腸癌和卵巢癌的早期蛋白基因組的研究發(fā)布后,已發(fā)表了一系列針對各種癌癥類型的蛋白基因組“景觀”研究。這些研究系統(tǒng)地分析和整合了基因組、轉(zhuǎn)錄組、蛋白質(zhì)組和蛋白翻譯后修飾(PTM)數(shù)據(jù),以進(jìn)一步了解疾病發(fā)病機(jī)制并確定每種癌癥類型的治療靶點(diǎn)。這些研究已經(jīng)建立了通用的方法,改進(jìn)了包括:癌癥亞型分類;探索免疫微環(huán)境;推斷新抗原庫;檢查 DNA、RNA、蛋白質(zhì)和PTM水平的協(xié)調(diào)調(diào)節(jié),以及蛋白質(zhì)組特異性或 PTM 特異性調(diào)節(jié);并確定癌癥驅(qū)動因素和治療靶點(diǎn)。涉及的蛋白基因組的分析內(nèi)容如下:

這些研究不僅對疾病的機(jī)制和生物學(xué)過程提供了深度、完整的見解,還利用蛋白質(zhì)組和磷酸化蛋白質(zhì)組發(fā)現(xiàn)了新的潛在治療靶點(diǎn),發(fā)現(xiàn)了治療人群選擇和預(yù)后的標(biāo)志物,評估了癌癥的免疫“景觀”,以及利用多組學(xué)重新定義了癌癥的分型。部分已發(fā)表的蛋白質(zhì)基因組研究,對癌癥的解析及亮點(diǎn)羅列如下:
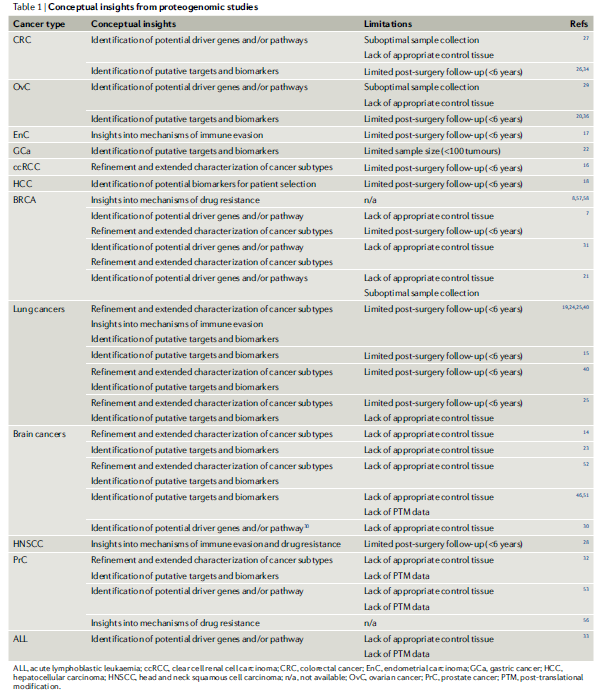
值得注意的是,許多癌癥蛋白基因組的研究強(qiáng)調(diào)了蛋白質(zhì)組學(xué),尤其是 PTM 在描繪癌癥生物學(xué)和確定潛在治療靶點(diǎn)方面的關(guān)鍵作用。當(dāng)前的癌癥臨床實踐幾乎完全由基因組學(xué)驅(qū)動,但蛋白質(zhì)組分析提供的額外信息,則清楚地報告了RNA-蛋白質(zhì)之間相對較低的相關(guān)性。早期的研究報道了RNA-蛋白質(zhì)相關(guān)性平均在0.3-0.45范圍內(nèi)。高度相關(guān)的基因-蛋白質(zhì)產(chǎn)物來自氨基酸和脂肪酸代謝途徑,而管家核糖體和剪接體途徑富含相關(guān)性非常低的基因-蛋白質(zhì)對。多項研究表明,在 mRNA 和蛋白質(zhì)中具有相似穩(wěn)定性的基因往往具有更高的 RNA-蛋白質(zhì)相關(guān)性。具有低 mRNA-蛋白質(zhì)相關(guān)性的基因往往是泛素-蛋白酶體途徑的靶點(diǎn)或受 miRNA 調(diào)節(jié)。更詳細(xì)的mRNA-蛋白質(zhì)相關(guān)性綜述可參見Nat Rev Genet 21, 630–644 (2020)。
2. 走向臨床應(yīng)用
為了解決臨床假設(shè),并朝著臨床實用性邁進(jìn),首先要考慮的是快速冰凍的隊列樣本能夠得到統(tǒng)一規(guī)范化地處理。III期臨床試驗的樣本有必要為基于蛋白基因組學(xué)的臨床實踐提供一級證據(jù)。但這需要在正確標(biāo)本的積累等方面得到保障,包括精心設(shè)計和注釋的臨床數(shù)據(jù),以解決相關(guān)的轉(zhuǎn)化目標(biāo)。同時需要在分析技術(shù)上,實現(xiàn)OTC包埋活檢樣本中的蛋白質(zhì)組(包括PTM)數(shù)據(jù)的有效獲取。為解決這些問題,多項努力正在進(jìn)行中。當(dāng)在發(fā)現(xiàn)隊列中發(fā)現(xiàn)了一些假說和證據(jù)后,下一步的分析就會涉及用靶向蛋白質(zhì)組(如MRM、PRM)和多重免疫的方法進(jìn)行驗證。此外,在單細(xì)胞水平上,進(jìn)行RNA和DNA序列分析的可靠方法已經(jīng)出現(xiàn),其通量足以對數(shù)百到數(shù)千個單細(xì)胞進(jìn)行測序,而在單個細(xì)胞水平上分析大約1000個蛋白的蛋白質(zhì)組學(xué)方法也已經(jīng)開始出現(xiàn)。樣品處理、色譜和質(zhì)譜儀器的進(jìn)一步改進(jìn),將很快以合理的通量實現(xiàn)單細(xì)胞蛋白質(zhì)組分析,從而為整合基因水平的數(shù)據(jù)實現(xiàn)單細(xì)胞水平的蛋白基因組奠定基礎(chǔ)。
總結(jié)
雖然數(shù)百個樣本的單類癌癥,以及數(shù)千個樣本的各類癌癥的蛋白質(zhì)基因組分析,已經(jīng)獲得了大量分子數(shù)據(jù)信息,代表了重大的科學(xué)成就,但蛋白基因組仍然是一個新興領(lǐng)域。與基因組學(xué)的早期一樣,bulk水平的分析可能會對癌癥生物學(xué)產(chǎn)生重要且可操作的見解,但需要更多的數(shù)據(jù)來識別不太常見或細(xì)微的致癌過程,需要進(jìn)行蛋白基因組維度的腫瘤內(nèi)異質(zhì)性的探索。越來越多的國際性合作,可以確保種族和環(huán)境等因素具有更廣泛的代表性,從而更好地研究癌癥的蛋白質(zhì)基因組多樣性。蛋白翻譯后修飾(PTM) 分析可能最有希望揭示癌癥相關(guān)途徑的細(xì)微調(diào)節(jié)。當(dāng)前蛋白基因組景觀研究中所提出的生物學(xué)觀察和治療假設(shè),都需要進(jìn)一步研究和驗證。在可預(yù)見的未來,隨著更多的癌癥和癌癥類型進(jìn)行蛋白基因組分析,更多的PTM被檢測,泛癌的蛋白基因組研究獲得更多的信息,蛋白基因組技術(shù)將會越來越多地應(yīng)用于解決轉(zhuǎn)化背景下的特定臨床問題。最終,隨著這些方法和技術(shù)的成熟,預(yù)計蛋白質(zhì)組將成為癌癥診斷和治療中更不可或缺的一部分,在個體患者水平上提供精確的靶向治療,并利用基因組學(xué)和蛋白質(zhì)組學(xué)數(shù)據(jù)的結(jié)合對該患者的癌癥進(jìn)行全面描述。
中科優(yōu)品推薦
【中科新生命】可提供基于蛋白基因組、蛋白質(zhì)組的多組學(xué)整合分析和數(shù)據(jù)挖掘,為疾病分子圖譜描繪、分子分型、標(biāo)志物與藥靶發(fā)現(xiàn)提供助力。

- 翼和生物SNP基因分型技術(shù):揭秘基因密碼,探尋寶寶健康之路
- 促腎上腺皮質(zhì)激素釋放激素(CRH)在探索肥胖機(jī)制中的研究
- 泌尿系統(tǒng)疾病的關(guān)鍵治療靶點(diǎn)之V2R的介紹及相關(guān)實驗
- 激光共聚焦顯微鏡助力腫瘤抑制劑研究
- 空間多組學(xué)解碼腫瘤微環(huán)境,助力加速精準(zhǔn)治療研究
- 利用單細(xì)胞轉(zhuǎn)錄組技術(shù)解析多種免疫細(xì)胞對大量細(xì)胞因子的響應(yīng)
- Emulate器官芯片助力研究藥物引起肝損傷的機(jī)制
- 骨質(zhì)疏松和甲狀旁腺功能減退關(guān)鍵靶點(diǎn)PTH1R的結(jié)構(gòu)功能及相關(guān)實驗介紹
Copyright(C) 1998-2025 生物器材網(wǎng) 電話:021-64166852;13621656896 E-mail:info@bio-equip.com





