ģîŧ°ûŗÉĪņĪÂĩÄSiO2-Fe3O4ŧ{Ã× fÍŦ×ÔĘÉÕ{ŋØ

ÔÚÉúÎīátWîIĶōŖŦŅõģ¯čFŖ¨Fe3O4ŖŠēÍļūŅõģ¯ščŖ¨SiO2ŖŠĘĮ×îŗŖŌĩÄŧ{ÃײÄÁĪŖŦßMČëŧ°ûēķŖŦŧ{Ã×ÁŖ×ĶūŊĩŊâŗÉčFŖŦ˛ĸͨß^¸ÄמÁŖķwĪāęPŧ°ûÆ÷ĩÄŊYÕT§ģîĐÔŅõŖ¨ROSŖŠĩÄÉúŗÉĄŖß^ÁŋĩÄ ROS ūÔÚŧ°ûČŽaÉúßBæiˇ´Ē˛ĸŌũÆđŧ°û×ÔĘÉĄŖ
Ōō´ËŖŦąžŅĐžŋĀûĶà HEK-293 ÄIŧ°ûíÁËŊâFe3O4ēÍSiO2ŧ{Ã×îwÁŖĻŧ°û×ÔĘÉĩÄÕT§ēÍ_Ķ×ģ¯ŖŦéŧ˛˛ĄÖίĩÄŨoÖú¯ˇ¨ĖᚊŌģˇNÅR´˛˛ßÂÔĄŖ
ąžŅĐžŋģîŧ°ûŗÉĪņxąOyŧ°û×ÔĘɡŊˇ¨Ŗē
ĘšĶÃ Celloger Mini PlusŖ¨ŋĩēÍß_ŖŠßMĐĐÅÄzĄŖ
ĸLC3ŪDČžŧ°ûŌÔÃŋŋ× 1 × 106 ĩÁŋˇNÔÚ 6 ŋ×°åÉĪ˛ĸÅāđB24ĐĄrĄŖēķĸÅāđBģų¸üQéēŦĶĐ 50 µg/mL Fe3O4ĄĸSiO2 ĩÄĐÂÅāđBģųĄĸ Fe3O4ÅcSiO2ĩÄģėēĪÎīĄŖÖŽēķÔÚ 24 ĐĄrČÃŋ 10 ˇÖįÅÄzŌģ´ÎDĪņ˛ĸÉúŗÉŌîlĄŖ
ŊYšûŖē
ÔÚąžŅĐžŋÖĐŖŦéÁËÔušĀ×ÔĘÉÕ{šŖŦÉúŗÉÁË LC3 ŪDČžŧ°ûĄŖͨß^ˇÖÎö LC3 ĩÄ×ģ¯ŖŦWestern blotēÍ RT-qPCR ×CÁË×ÔĘÉĩÄÕ{š×÷ĶÃĄŖŊYšû°lŦFŧ{Ã×îwÁŖĖĀíēķ LC3 ĩÄļČÔöŧĶŖŦąíÃ÷×ÔĘÉŋÉÄÜÔöŖ¨ČįD1ŖŠĄŖ
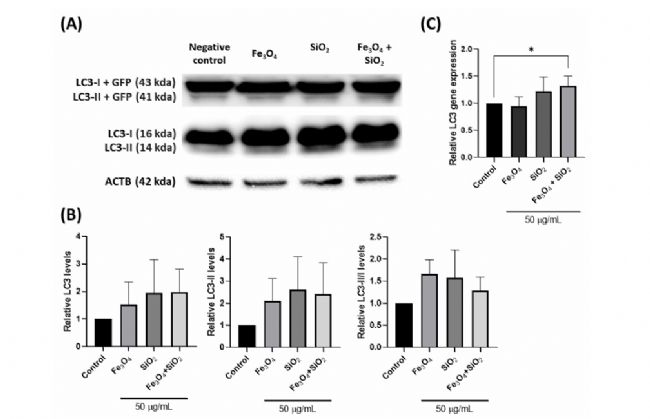
D1.ĘšĶÃŧ{Ã×îwÁŖĖĀí LC3 ĩÄ×ģ¯
éßMŌģ˛ŊŅĐžŋLC3ąíß_ŧ°r×ģ¯ŖŦąžŅĐžŋĀûĶÚ˛žÛŊšī@ÎĸįRēÍģîŧ°ûŗÉĪņxŖ¨ŋĩēÍß_ŖŦCelloger Mini PlusŖŠíßMĐĐĶ^yĄŖ ŊYšûąíÃ÷ŖŦŧ{Ã×ÁŖ×ĶĖĀíēķĶ^˛ėĩŊĩÄÁŌžGÉĢÉšâŖŦąíÃ÷ LC3 ąíß_ÔöŖŦ×CÁË×ÔĘÉķwĩÄĐÎŗÉĄŖLC3ÔÚ SiO2 ŌÔŧ°Fe3O4 ēÍ SiO2 ģėēĪÎīÖĐąíß_¸ü¸ßŖ¨ČįD2ŖŠĄŖģîŧ°ûąOyÖĐĩÄžGÉĢÉšâļČÄ0ĐĄré_ĘŧÔöŧĶŖŦŗŦß^ÁËęĐÔĻÕÕŊMĩÄÉšâļČŖ¨ČįD3ŖŠĄŖ
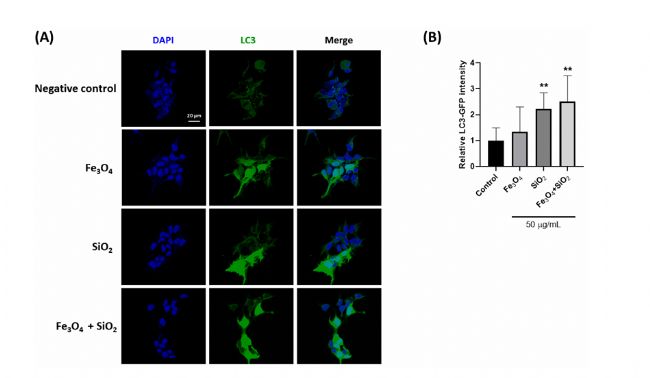
D2. Fe3O4ĄĸSiO2 ŧ°ÆäŊMēĪŧ{Ã×ÁŖ×ĶÖĐ LC3 ËĶŖ¨žGÉĢŖŠēÍŧ°ûēËŖ¨Ë{ÉĢŖŦDAPIŖŠĩÄÉšâˇÖÎö
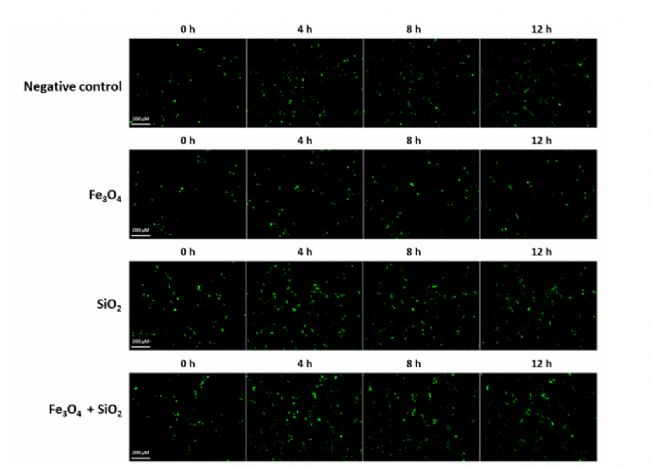
D3.ŧ{Ã×îwÁŖĖĀíēķ LC3 ąíß_ĩÄr×ģ¯ĄŖËŗßŖē200 μm
ŅĐžŋąíÃ÷SiO2 ēÍ Fe3O4 NPs Ķ°íÁË×ÔĘÉķwĩÄĐÎŗÉĄŖSiO2ēÍFe3O4ŧ{Ã×ÁŖ×ĶÔÚĒŧ¤ÕT§ĪÂŧ¤ģîÁË×ÔĘÉÄÜĄŖ×ÔĘÉĩÄŗÖĀmŧ¤ģî´ŲßMÁËŧ°ûÔöÖŗŖŦĶĐÖúĶÚĐŪÍÄIÅKpûĄŖß@Ōģ°lŦF×CÃ÷ÁËŌģˇNĐÂĩÄ×ÔĘÉÕ{šÍžŊĄŖ

D4.Fe3O4 ēÍ SiO2 NPs ÕT§ĩÄ×ÔĘÉCÖÆĘžŌâD
×ÔĘÉÔÚŋØÖÆŧ°ûĐĐéˇŊÃæ°l]ÖøÖØŌĒ×÷ĶÃĄŖŧ°ûČ×ÔĘÉËŽÆŊß^¸ßģōß^ĩÍļŧū´ŲßMŧ°ûËĨĀĪĄĸŌÖÖÆŧ°ûÉúéL˛ĸ´ŲĘšŧ°ûĩōÍöĄŖąžŅĐžŋÖĐĒĶÃģîŧ°ûŗÉĪņxŖ¨ŋĩēÍß_ŖŦCelloger® Mini PlusŖŠŅĐžŋŧ°û×ÔĘÉŖŦß@ˇNŧŧĐgĩÄĖØücĘĮĩÍšâļžĐÔÅcĩ͸É_ŖŦÄÜōŦFéLrégąOyÅc×ÔĶģ¯ˇÖÎöŖŦéŅĐžŋČËTĖᚊʴ_ĩÄōĩūŌÔŧ°´ķ´ķpŨpÁËŅĐžŋČËTĩÄš¤×÷ØúĄŖ
- rŊŌÃÜŅĒšÜÉúŗÉŖēQM107 ĄÁ Cellogerģîŧ°ûŗÉĪņ
- ī@ÎĸÜŧūîÉĢĐŖÕũÖ¸ÄĪŖēŗŖŌî}ÅcŊâQˇŊ°¸
- ī@ÎĸŗÉĪņČįēÎĶĐЧŊâQŗÉĪņÜŧūÆÁéWî}
- ëpšâ×ĶŗÉĪņĒĶÃĶÚÉúÎīátWîIĶōĩÄ×îĐÂÚ Ũ
- ˇÎŅĒšÜŧ˛˛ĄŅĐžŋĩÄĐÂŌŊĮŖēŋįŗßļČČũžSŗÉĪņŧŧĐg
- ŅĐžŋßMÕšŖēŧ¤šâÉĸ°ßÅcČÔ´šâļāÄŖBŗÉĪņÔuyŗŦšĻÄÜÕ{ŋØ
- ģųĶÚĩWŋōŧÜĩÄ3D͸Ã÷ŗÉĪņˇÖÎöˇ¨ÔÚČĢŅĒšÜŅĐžŋĩÄĒĶÃ
- ŅĐžŋßMÕšŖē͸Ã÷ŗŦÂQÄÜÆ÷rąOyÄX˛ŋÎĸŅĒšÜĶB
- ˛ĖËžZEN core ÜŧūŦFŋÉßmÅä˛ĖËžČĢĪĩÁĐßÃčëįRŽaÆˇ
- EVIDENTÍÆŗöEviStarWÖŽĐĮES818ī@ÎĸģĨĶŊĖWĪĩŊy
- ´ōÆÆß ŊįžĢĘßMģ¯ŖŦNEOSCANÍÆŗöNXLÅ_ĘŊ´ķ}ī@ÎĸCT
- ARveo8ī@ÎĸįRÖúÁĻĘ×ĀũîiÉîLVAĐgŗÉšĻÄæŪDADÕJÖĒËĨÍË
- Æŋ¨Öą˛ĨŖē˛đŊâÕæōĘŌöž°ÖĐĩÄÍësĶąžŊâQˇŊ°¸
- EVIDENTyĐÂÆˇDSX2000ČĢëĶĩ´aī@ÎĸįRÁÁĪāSEMICON
- EVIDENTÉúÃüŋÆWˇūÕĖÕũĘŊ¸üÃûéEVIDENTī@ÎĸŗÉĪņ
- °˛ŊŨĐÂŌģ´úĩ×Ö˛ĄĀíWŊâQˇŊ°¸ÁÁĪā2025 USCAP
Copyright(C) 1998-2025 ÉúÎīÆ÷˛ÄžW ëÔŖē021-64166852;13621656896 E-mailŖēinfo@bio-equip.com





