O2k在氣體信號分子H2S誘導氧化代謝長期多效性影響機制研究的應用
摘要:
中等劑量的H2S暴露會導致哺乳動物出現嚴重但可逆的低代謝。在細胞水平上,H2S通過還原羧化抑制電子傳輸鏈(ETC),增強有氧糖酵解和谷氨酰胺代謝;然而,這些變化的持久性是未知的。作者研究表明,盡管H2S預處理具有揮發性,但它會增加P50(O2),即半飽和氧分壓,并對氧化代謝具有多效性影響,這種影響會持續24小時以上。H2S誘導的低代謝在血液供應不足或中斷引起的創傷或疾病臨床中是有益的,作者的研究對減輕缺血再灌注損傷和/或延長血小板等生物制品的保質期具有重要意義。
結果:
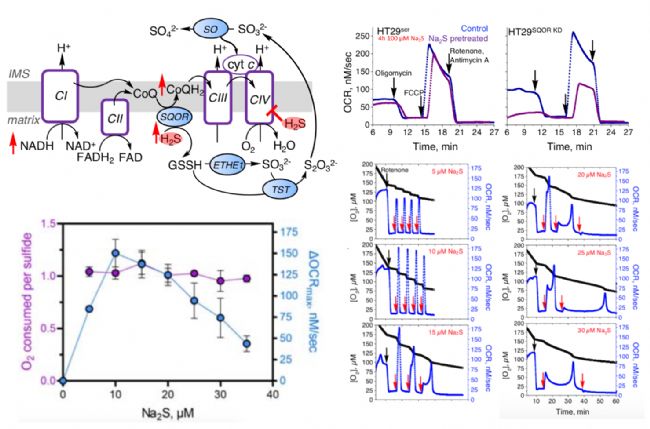
H2S氧化途徑通過一系列氧化和硫轉移酶步驟將H2S轉化為硫代硫酸鹽和硫酸鹽。硫醌氧化還原酶(SQOR)使H2S分解代謝產生電子,利用輔酶Q(CoQ)作為電子受體,促進CoQ還原態增加,因此存在于H2S氧化和電子傳輸鏈(ETC)的交叉點。SQOR依賴的H2S氧化增強了電子傳遞,促進了ATP的合成。然而,當H2S濃度超過SQOR分解代謝能力時,H2S抑制復合體IV,表現為細胞耗氧率(OCR)降低。
為了進一步驗證不同劑量的H2S暴露對OCR的影響,作者利用奧地利Ororboros O2k多維度線粒體能量代謝分析系統具有無加藥數量限制及完全封閉環境下檢測的特點,添加了復合體I抑制劑魚藤酮(Rotenone),減少了CoQ氧化還原態變化的干擾;然后重復添加硫化鈉(Na2S,產生H2S),Na2S低濃度(<15 μM)引發OCR最大值急劇增加, Na2S高濃度(>20 μM)引發OCR最大值逐漸降低,由此,OCR最大值變化表現出對H2S濃度的鐘形依賴性。
為了進一步驗證H2S誘導線粒體功能的長期性變化,將HT29Scr、HT29SQOR KD細胞預處理暴露于Na2S(100 μM,4小時),HT29Scr基礎代謝率和最大呼吸率相對于Control組,都有降低;而HT29SQOR KD基礎代謝率和最大呼吸率相對于Control組,都有顯著性降低;同時也進一步說明硫醌氧化還原酶(SQOR)使H2S分解代謝產生電子,增加了電子傳遞,增強了線粒體功能。
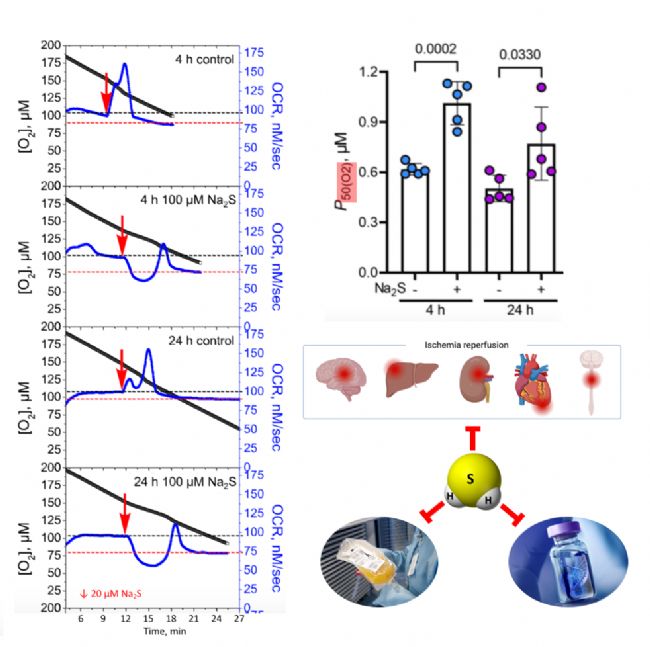
單次急性H2S暴露對氧化代謝產生長期影響:作者檢查了4小時、24小時單次急性暴露于Na2S(100 μM)后代謝效應的持久性;在單次暴露于Na2S(100 μM)后4小時和24小時,P50(O2)值出現了顯著性增加,表明耗氧能力顯著降低。
討論:實驗結果顯示細胞對H2S的反應范圍從低濃度H2S的O2消耗急速增加到高濃度H2S的O2消耗抑制,反映了H2S對氧化代謝的多效性;并且細胞暴露于H2S后,其氧化代謝水平持續性降低超過24小時。所以作者還提出既然H2S預處理可以維持低代謝時間窗口,防止進一步的氧化損傷,那么對嚴重創傷(如中重度燒傷)的高代謝反應、缺血再灌注損傷以及失控性炎癥等臨床病癥就具有潛在的治療作用;也會具有對延長生物制品保質期的潛在作用。
參考文獻:David A. Hanna , et al. H2S preconditioning induces long-lived perturbations in O2 metabolism. PNAS. 2024 March 13;121(12)e2319473121. https://doi.org/10.1073/pnas.2319473121.





