核酸殘留煩惱?全能核酸酶檢測助您輕松解決
隨著越來越多的生物制品(重組蛋白疫苗、病毒載體疫苗、細胞治療/基因治療藥物等)進入治療領域,生物制品的質量控制也日趨嚴格,其中核酸殘留因其潛在的危害性,是各類質控標準的重中之重。
我國參照WHO、FDA和歐盟標準,在藥典中明確規定酵母、大腸桿菌表達的生物制品中DNA殘留量不超過10ng/劑量。我國2020年藥典將人用狂犬病疫苗(Vero細胞)DNA殘留標準更新為≤3ng/劑量。除了殘留量的規定,FDA、CDE發布的相關指導文件中建議,殘留的細胞宿主DNA片段不能超過一個功能基因的長度(約200bp)。
因此,在生物制品的生產工藝中必須有去除核酸殘留的步驟,確保生物制品的中的核酸殘留滿足相應法規的要求。
逐典生物提供高品質
全能核酸酶殘留檢測試劑盒
靈敏度高
為生物制品解決宿主核酸殘留困擾
逐典Pannarase全能核酸酶
殘留檢測試劑盒
01
產品特點
兼容不同品牌核酸酶
靈敏度高,線性范圍廣
抗體直接包被,批間一致性好
02
數據展示—不同品牌核酸酶檢測
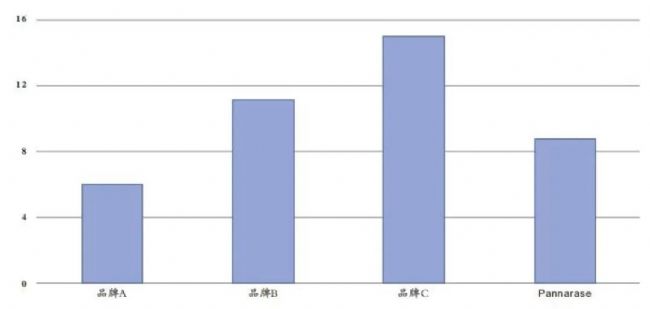
可響應市面上多種國產及進口品牌核酸酶,檢測結果具有較高的穩定性和可重復性。
03
標準曲線
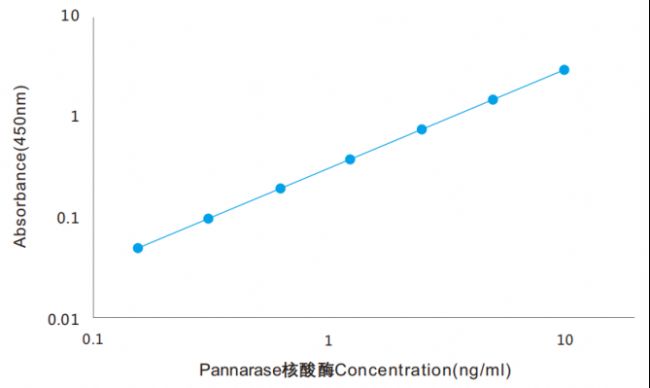
線性范圍寬,從0.2ng/ml到10ng/ml,對于常規工作濃度10-20U/ml,無需重復繁瑣稀釋,即可檢出殘留量。
04
準確性檢測
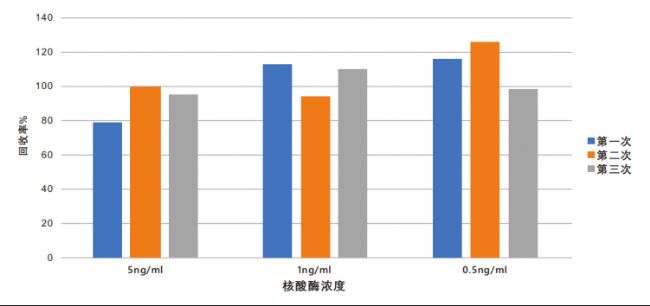
通過低中高三個濃度點Pannarase核酸酶的添加,均得到高回收率的檢測數據。
05
精密度檢測
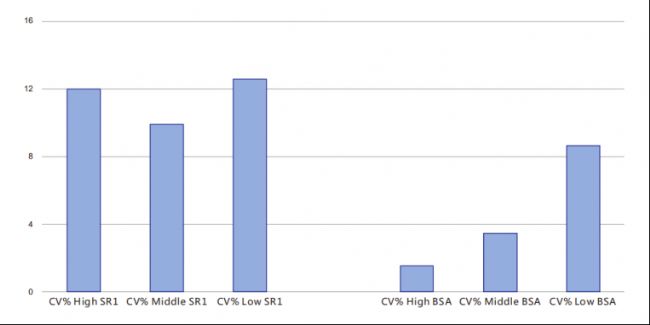
高、中、低三個濃度點下,對照品SR1(Pannarase核酸酶標準品)與1%BSA(補加Pannarase核酸酶標準品)中,CV%表現良好,均在15%以下,具有較高的精密度和重復性。
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com





