ÉšâĶËãCāĶßÃčŧŧĐgŖ¨FLECTŖŠŗÉĪņÔĀíŧ°ĒĶÃ
§×x
ĶÉĶÚžĢÖZÕæšâWŗÉĪņĩÄŖĀûąŖ×oÔįŌŅŊŊYĘøŖŦŊü×ÄęĘĐöĩÄšâWŗÉĪņÔOäÆˇÅÆÔÚÔöŧĶŖŦĶČÆäĘĮøČÆˇÅÆĩÄÔöŧĶĄŖÉúÎī°lšâŗÉĪņĩÄŧŧĐgéTąČŨ^ĩÍŖŦß@ˇNÆˇÅÆĩÄÔöļāĘĮĶĐĀûĶÚŊKļËĶÃôĩÄŖŦÔÚδíĩÄ2-3ÄęŖŦļūžSšâWŧŧĐgéÖ÷ĩÄÔOäĘĐör¸ņūßMŌģ˛ŊŊĩĩÍŖŦĒÔŊĶŊüÆäēĪĀíĩÄrÎģŖē80-120ČfČËÃņÅŖŦŋŧ]ĩŊŲ|ąŖÄęĪŪŖŦ3-5ÄęČĢąŖĩÄrÎģĒÔÔÚ150ČfŌÔČŖŦß@ĀīĩÄČĢąŖĘĮ°üĀ¨CCDĩÄĄŖ
ĩĢĘĮÕæÕũĩÄČũžSĐĄĶÎīšâWŗÉĪņÔOäŖŦß]ĶĐĀé_¸ ĩÄĐōÄģĄŖëmČģÔPEŖ¨RevvityŖŠÔÚĘĐöÉĪäNĘÛÁ˲ģÉŲSpectrumŖŦß@HHĘĮÉĖIÉĪĩÄŗÉšĻŖŦļø˛ĸˇĮŧŧĐgÉĪĩÄßM˛ŊĄŖČũžSšâWģîķwŗÉĪņĩÄÄŋËĘĮ¸ßˇÖąæÂĘĄĸÕæļ¨ÁŋĄĸČĢÉîļČĄĸÎĸÁŋzyĄĸîPETĩÄŊYšûˇÖÎöÄÜÁĻĄŖ
15ÄęĮ°ŋÆWŧŌŌŅŊÉîČëŅĐžŋÁËĶ°íšâWĐĄĶÎīģîķwŗÉĪņŊYšûĩÄŌōËØ[1]ŖŦwŧ{éŌÔĪÂ×ücŖē
1)˛ģÍŦŗÉĪņÔOäĩÄŊYšû˛ģŌģÖÂŖģ2ŖŠĶÎī˛Ų×÷Õ`˛îŖģ3ŖŠČąˇĻŊMŋĄĸŧ˛˛ĄēÍÃâŌß°ĐĪōĩÄĖØŽĐÔČžÁĪŖģ4ŖŠŊMŋĻąČļČŖģ5ŖŠÆ¤ÄwēÍŊMŋĩÄ×Ô°lÉšâŖģ6ŖŠŊâÆĘWÎģÖÃÅcÉšâĐÅĖÅäĘĀ§ëyŖģ7ŖŠČąˇĻŗÉĪņxÆ÷ĐÔÄÜŌˇļēÍËĘŖģ8ŖŠŅĐžŋŧeĩÄšâWĐĄĶÎīŗÉĪņˇÖąæÂĘÅcÅR´˛ÔOä˛ģÆŊĐĐŖģ9ŖŠ¸ßąŗž°šâ¸É_Ŗģ10ŖŠšâ×ĶÔÚÉúÎīŊMŋÖĐĩÄ×ÔČģÉĸÉäŖģ11ŖŠ´ŠÍ¸ÉîļČĄŖ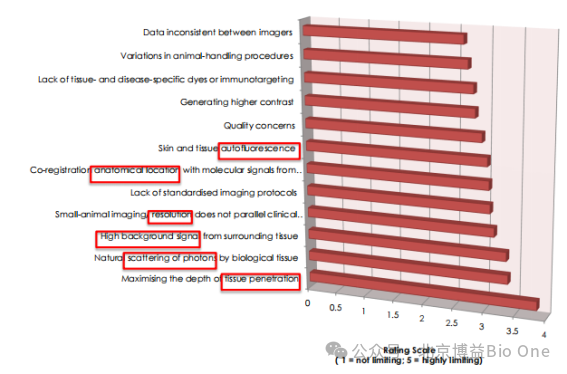
ąžÎÄŌÔĪÂČČŨČįšû]ĶĐÃ÷šâWĄĸÉšâ/ÉúÎī°lšâĩČŖŦHáĻÉšâŗÉĪņŧŧĐgĄŖ
ŌģĄĸÉšâŗÉĪņ
1ĄĸŧŧĐgÔĀí
ÉšâŖ¨FluorescenceŖŠĘĮ×ÔČģŊįĩÄŌģˇNŗŖŌ°lšâŦFĪķĄŖŽÉšâÎīŲ|ĘÜĩŊŧ¤°lšâÕÕÉärŖŦȲŋĩġÖ×ĶģōÔ×ĶÎüĘÕšâ×ĶÄģųBÜSßwĩŊŧ¤°lBŖŦëSēķáˇÅÄÜÁŋ°lŗö˛¨éL¸üéLĩÄ°lÉäšâŖŦß@ˇN°lÉäšâžÍĘĮÉšâĄŖĸÉšâÎīŲ|š˛rŊYēĪģōÎīĀíÎü¸ŊÔÚËųŌĒŅĐžŋˇÖ×ĶĩÄÄŗģųFÉĪ[2]ŖŦžßĶĐoˇÅÉäÎīÎÛČžĄĸ˛Ų×÷ēąãĄĸČŨŌ×Ķ^˛ėĩČücŖŦŋÉŊčÖúÉšâĖØĐÔĻąģËĶĻĪķßMĐĐļ¨ĐÔĄĸļ¨ÎģŌÔŧ°ļ¨ÁŋˇÖÎöĄŖ2ĄĸÉšâ°lÉäĶËãCāĶßÃčŗÉĪņŧŧĐg
Éšâ°lÉäĶËãCāĶßÃč(Fluorescence Emission Computed TomographyŖŦFLECT)ŖĀûŧŧĐgŖŦsĢ@ŋÆWësÖžÔußxĩÄ“2011ÄęĘŽ´ķĐÂŧŧĐg”ÖŽŌģŖŦĘĮIŊįĩÚŌģÅ_ÄÜōĖᚊļ¨ÁŋÉšâČũžSĩūĩÄÔOäŖŦéÅR´˛Į°ĐĄĶÎīÄŖĐÍĩÄČĢÉíŗÉĪņēÍķwČąíÕ÷ĖᚊÁËoÅcąČĩÄzyÄÜÁĻĄŖČįD2ËųĘžŖŦŗÉĪņrŧ¤šâÖąŊĶ§ČëFLECTĘÖąÆ÷ŊMŧūÖĐŖŦŧ¤°lĐĄĘķķwČĩÄÉšâĄŖŌģĶÉ48šâëļūOšÜŊMŗÉĩÄĖŊyÆ÷hhĀ@ÔÚĐĄĘķÖÜúŖŦĘÕŧ¯°lŗöĩÄÉšâĐÅĖĄŖͨß^ŧ¤šâšâÔ´ēÍĖŊyÆ÷úĀ@´ũyĶÎīĐũŪDŖŦŋÉÔOÖÃ˛ģÍŦĶēņßMĐĐČĢŊĮļČāĶßÃčŖŦÄļøĢ@ĩÃ3DĩūĄŖ˛Éŧ¯ÍęŗÉēķŖŦËųĢ@ČĄĩÄFLECTĩūąģÖØŊ¨ˇūÕÆ÷ÖØŊ¨ŗÉŌģÁĸķwDĪņŖŦßMĐĐČũžSŋÉŌģ¯Ķ^˛ėĄŖ
ÃĀøTriFoil Imagingé_°lÁËĘ×Å_āĶßÃčŧŧĐgČÚēĪĩÄëpÄŖBĶ°ĪņÔOä--InSyTe FLECT/CTĄŖĸFLECTēÍÍŦŨSŌģķwĩÄXÉäžCTāĶßÃčŗÉĪņÕûēĪĩŊŌģxÆ÷ÖĐŖŦĖᚊžßĶĐŊâÆĘW ĸŋŧĩġÖ×ĶŗÉĪņÄÜÁĻĄŖ˛ÉĶÃÆäŖĀûĩÄĐũŪDũéTŧÜÔOĶĘÕŧ¯ÍęÕûŊĮļČĩÄĶÎīķwČĩÄšâWēÍXÉäžÍļĶ°ŖŦFLECTîÍŦÅcPETēÍSPECTŧŧĐgĩÄšâWŗÉĪņŖŦžßĶĐoˇÅÉäĐÔĐÔŖŦ¸ßĐÔrąČĩÄŨĄŖĖŊyÆ÷ĐũŪD360°ĻÉšâĐÅĖßMĐвÉŧ¯ŖŦŊYēĪ600-900nmÖŽégĩÄŊüŧtÍâŧ¤šâšâÔ´ŖŦÉšâāĶßÃčŧŧĐgÖØŊ¨Ëãˇ¨ĘšĩÃÉšâÔÚōĶÎīķwČŋÉŦFopēÄČũžSÖØŦFŖŦÄļøĢ@ĩÃĶÎīÉîĶŊMŋĩÄÉšâĐÅĖŖŦØĩ×ŊâQÁË÷ŊyÔOäÉšâĖŊyÉîļȲģōĄĸļūžSšâ°ß˛ģÄÜžĢ´_ļ¨ÁŋĩČî}ĄŖ
 D2.FLECTŧŧĐgÔĀíĘžŌâD
D2.FLECTŧŧĐgÔĀíĘžŌâDļūĄĸÖØŊ¨¸ßˇÖąæDĪņĩÄÄÜÁĻ
InSyTe FLECT/CTĪĩŊyĶĐÉÖØŊ¨ŌũĮæŖŦŌģĶÃĶÚÉšâDĪņÖØŊ¨ŖŦÁíŌģĶÃĶÚCTDĪņÖØŊ¨ĄŖ
1ĄĸÉšâDĪņ
ÉšâDĪņÖØŊ¨ĘĮĸąģyÎīķwĩÄąíÃæĐÅĪĸÅc˛Éŧ¯ĩŊĩÄÉšâĩūŊYēĪÆđíŖŦĐÎŗÉÉšâÔ´ÔÚąģyÎīķwÖСֲŧĩÄČũžSąíÕ÷ĄŖĸąíÃæĐÅĪĸēÍÉšâĩūĖáŊģÖÁŖĶÃĩÄÖØŊ¨ˇūÕÆ÷ĄŖ˛ÉĶÃÉšâÖØŊ¨ŖĶÃŌũĮæŖ¨FluoroTomŖŠŖŦĀûĶÃŨÉä÷ßfˇŊŗĖēÍĮōÖCē¯ĩŖŦģųĶÚŊMŋÖĐšâ÷˛ĨĩÄÕũŅŨÄŖĐÍŌÔ“ĶĐĪŪ˛îˇÖ”ˇŊˇ¨§Čë÷ßfˇŊŗĖĄŖŋŧ]ÁËŊMŋĩÄšâÉĸÉäĄĸÎüĘÕē͡´ÉäĩČšâWĖØĐÔŖŦŌÔŧ°ŊMŋŊYĩÄĶ°íŖŦÄŖMšâÔÚŊMŋÖĐĩÄ÷˛Ĩ¡ŊĄĸˇÖ˛ŧēÍÎüĘÕĮérŖŦĘĮÄŋĮ°×îžĢ´_ĩÄšâWļ¨ÁŋŧŧĐgĄŖFLECTÄÜōĖᚊļāŊĮļČÖØŊ¨ˇŊˇ¨ēÍ360°ČũžSÉšâŗÉĪņšĻÄÜŖŦĢ@ČĄČĢŊĮļČŗÉĪņČũžSĶ°ĪņŖŦŋÉÄšÚ îŖŦʸ îŖŦMāĶ^˛ė¸ĐÅdȤ ^ĶōŖ¨Region of InterestŖŦROIŖŠŖŦļ¨Îģšâ°ßÎģÖÃŖŦÉúŗÉŅØÖøzŨSĐũŪDĩÄĶB×î´ķÃÜļČÍļĶ°ĶŽŖ¨Maximum Intensity ProjectionŖŦMIP)ŖŦ˛ĸÄÜąŖ´æËųĶĐÉîļČžĢĘĩÄÉšâĐÅĖücĩÄČũžSĐÅĪĸŧ°ŋēŦÁŋĐÅĪĸĄŖČįD3ËųĘžŖŦFLECTŋÉĻÉšâĐÅĖĩġ´ÉäĄĸÉĸÉäÎüĘÕēÍĐŖÕũŖŦÔÚ˛ģÍŦĩÄÉšââļČÖĐžßĶĐŌģÖÂĩÄžĐÔ(R²=0.9985)ŖŦ´_ąŖÁËĘ´_ĐÔēÍÖØÍĐÔĄŖ
FLECTŋÉŌÔžĢ´_ĩØסÛÉšâĐÅĖŖŦĸŊâÆĘWÎģÖÃÅcÉšâĐÅĖš˛ÅäĘČÚēĪŖŦO´ķĩØĖá¸ßÁËļ¨ÎģĩÄĘ´_ĐÔēÍĩūĩÄŋÉŋŋĐÔĄŖëmČģÎŌĩÄŗŖŌŗÉĪņÔOäÔÚĐĄĶÎīŗÉĪņÉĪąíŦFŗöÉĢŖŦĩĢÔÚÉîĶĩÄŊMŋŗÉĪņÖĐŖŦÎŌČÔÃæÅRˇÖąæÂʲģ×ãĩÄî}ĄŖČįD4ËųĘžŖŦFLECTĩġֹæÂĘÄÜōß_ĩŊ1mm3ŖŦÕšŦFŗöÅR´˛ËŽÆŊĩÄŗÉĪņЧšûĄŖ¸˛Éw´ķļāĩŊMŋĩÄÉîļČŖŦŋÉŌÔß_ĩŊ2.4-4cmĩÄzyÄÜÁĻŖŦĀûĶÃĪČßMËãˇ¨ĻÉšâĐÅĖĩġ´ÉäĄĸÉĸÉäÎüĘÕēÍĐŖÕũŖŦÖąŊĶŨŗöoąŗž°šâĩÄDÆŦŖŦ¸üĮåÎúĩØĶ^˛ėĩŊÉîĶĩÄÉšâĐÅĖŖŦķwŦFÁËŧŧĐgĩÄŋÉŋŋĐÔēÍËãˇ¨ĩÄĪČßMĐÔĄŖ
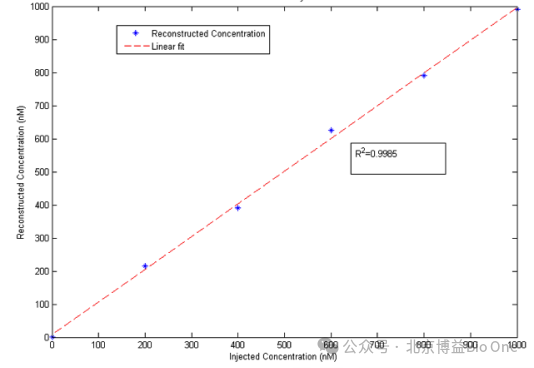
D3.ÖØŊ¨âļČÅc×ĸÉäâļČMēĪĮúž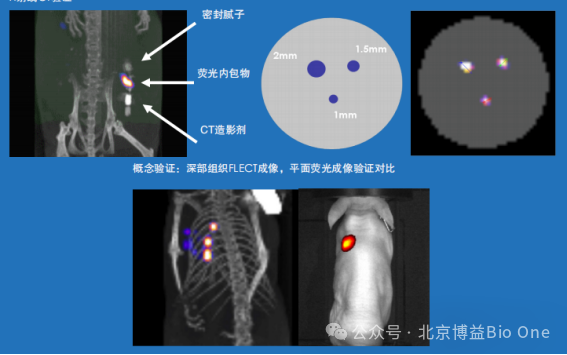
D4.¸ßˇÖąæÂĘÉšâDĪņÖØŊ¨
2ĄĸCTDĪņ
ĀûĶÃXž´ŠÍ¸˛ģÍŦÃÜļČēÍēņļČŊMŋŊYēķŖŦ°lÉú˛ģÍŦŗĖļČÎüĘÕļøŽaÉúĩÄĶ°ĪņĻąČŖŦĐÎŗɲģÍŦģŌëADĪņĄŖ¸ßÃÜļČŊMŋŖ¨ČįŖēšĮ÷ĀŖŠŖŦžßĶĐŨ^¸ßĩÄËĨpĪĩĩŖŦCTÉĪī@ĘžÁÁŖģĩÍÃÜļČŊMŋŖ¨ČįŖēˇÎŖŠŖŦžßĶĐŨ^ĩÍĩÄËĨpĪĩĩŖŦCTÉĪī@Ęž°ĩĄŖ
˛ÉĶÃCOBRAåFĐΞĘøËãˇ¨ŖŦÕæÕũÔÚŨSÎģĐũŪDßÃčrŦFČũžSDĪņĩIJÉŧ¯ēÍÖØŊ¨ĄŖĘšĶÃCTVšâÆŦŖ¨äXĄĸãfēÍåaŖŠíÔöÜŊMŋĻąČļȲĸpÉŲĘøÁ÷Ķ˛ģ¯Đ§ĒŖŦͨß^ČĨŗũĄĸŊĩĩÍåFĐΞĘøŌũÆđĩÄÎĶ°íĢ@ĩÃ×îŧŅĩÄCTDĪņŲ|ÁŋĄŖŋÉŌÔĻÕûROIģō˛ŋˇÖROI
^ĶōĩÄXÉäžÍļĶ°ßMĐĐÖØŊ¨ĄŖÍļĶ°´ÎĩÔŊļāŖŦÖØŊ¨régÔŊéLŖŦĩÃĩŊĩÄDĪņˇÖąæÂĘÔŊ¸ßĄŖ
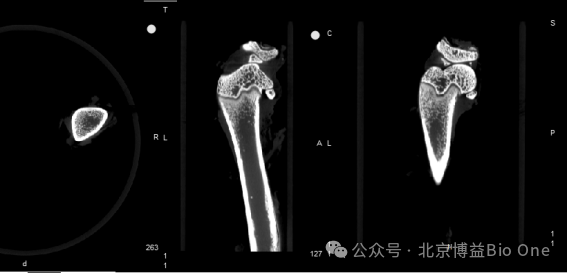
D5.FLECT/CTšĮ÷ĀŗÉĪņЧšûŖ¨ŋÉŌšĮĐĄÁēŊYŖŠ
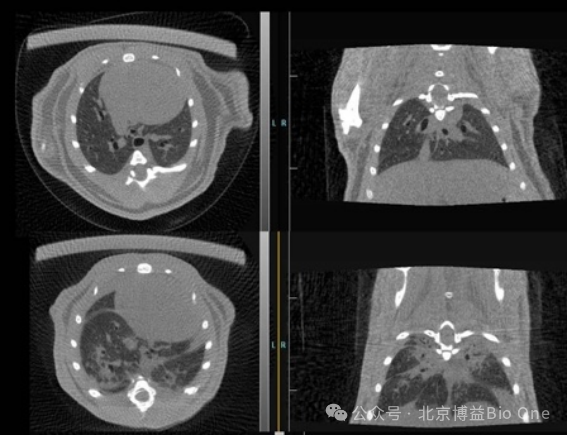
D6.FLECT/CTÜŊMŋŗÉĪņЧšûŖ¨ŋÉÔušĀˇÎŊYšĀwžSģ¯ŗĖļČŖŠ
3Ąĸš˛ÅäĘČÚēĪ
InSyTe FLECT/CT˛ÉĶÃëpģŦhŧŧĐgŖŦÎĸĐÍXÉäžšÜŖ¨ŧ¤šâšâÔ´ŖŠÅc¸ßė`ÃôļČĖŊyÆ÷ŌģÍŦúĀ@zĶ°ĻĪķŖ¨ĐĄĘķŖŠßBĀm×öāÃæßÃčĄŖžßäļāÄŖBÍŦŨSģ¯ßÃčŖŦŋÉļāÄŖBDĪņžĢĘČÚēĪĄŖCTŗÉĪņÎÔĒēÍFLECTŗÉĪņÎÔĒ˛ÉĶÃÍŦŨSģ¯ëpÄŖBÔOĶŖŦŌģ´ÎĐÔßÃčŗÉĪņŖŦoĐčÖØĐÂ[ˇÅģōŌÆĶĶąžĄŖąÜÃâÁËļāÄŖBDĪņČÚēĪĩÄÔÚî}ŖēČįŖēČÚēĪÎģÖÃ˛ģžĢ´_ĄĸŅĶßtĩČĄŖCTĪĩŊy˛ģHÄÜĖᚊŊâÆĘWĪāęPĐÅĪĸŖŦßÄܸÄÉÆÉĸÉäĐŖÕũŖŦĖá¸ßšâWŗÉĪņžĢļČĄŖ
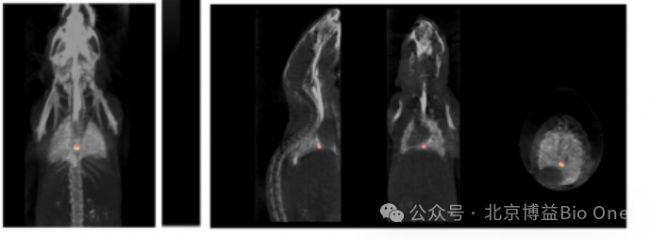
D7.FLECT/CTĶÃĶÚˇÎėoÃ}˨ČûÔ\āŗÉĪņ[3]
(ĒĶÃĀũ[3]ŖēŅĐžŋFę é_°lÁËŌģˇNĖØŽĐÔÉšâĖŊá(Targ-Cy7)ŖŦÎæŋšķwscFv°ĐĪōŊYēĪŅĒ˨ÖĐģîģ¯ŅĒĐĄ°åĘÜķwGPIIb/IIIaŖŦĶÃĶÚîiĶÃ}ŅĒ˨ĄĸˇÎėoÃ}˨ČûķwČŗÉĪņĄŖŖŠ
ČũĄĸÉîĶŊMŋzyÄÜÁĻ
1ĄĸÉúÎīŊMŋĻšâžĩÄÎüĘÕ
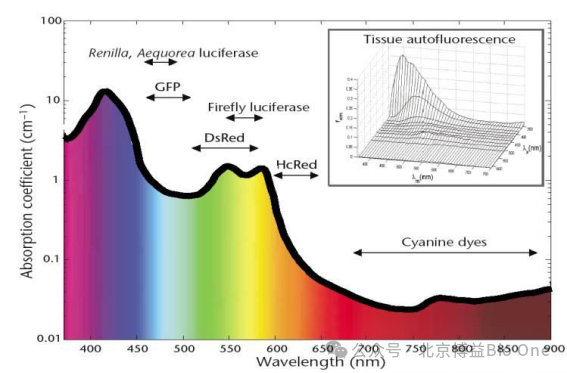
ÔÚ700-900nmß@ļÎŊüŧtÍâ ^ĶōČŖŦ´æÔÚŌģ“šâ×V´°”(Spectral Window)ĄŖÔÚß@“šâ×V´°”ČŖŦÉúÎīŊMŋĻšâžĩÄÎüĘÕ×÷Ķôķ´ķŊĩĩÍŖŦšâžŋÉŌÔßMČë¸üÉîŌģĐŠĩÄŊMŋĄŖÍŦrŖŦĶÉĶÚŅĒŧtĩ°°×ēÍŧ°ûÉĢËØēŦŅõÁŋ˛ģÍŦ§ÖÂĩÄÎüĘÕšâ×VĩIJîŽČÔČģŋÉŌÔˇÖąæĄŖŽ˛¨éL´ķĶÚ900nmrŖŦŊMŋÖĐĩÄËŽŗɡÖĻšâ×ĶĩÄÎüĘÕ×÷ĶÃĘŽˇÖÁŌŖŦšâ×ĶßMČëŊMŋĩēÁÃמÍūąģÎüĘÕ´ųąMĄŖļøÔÚĩÍĶÚ700nmĩÄŋÉŌšâˇļúČŖŦŅĒŧtĩ°°×ĻšâžĩÄÎüĘÕ×÷Ķôķ´ķÔöŧĶŖŦÍŦrŖŦŊMŋĩÄÉĸÉä×÷ĶÃŌ˛ĘŽˇÖ ēĻ[4]ĄŖŌō´ËŖŦÔÚátWŅĐžŋÖĐͨŗŖĘšĶÃ˛¨éLÎģĶÚšâ×V´°ČĩÄŊüŧtÍâšâ×÷éĖŊyšâÔ´ĄŖFLECT˛ÉĶÃąģˇQ×÷“átWšâ×VÖŽ´°”ĩÄŊéĶÚ600-900nmÖŽégĩÄŊüŧtÍâšâŖŦČįD8ËųĘžŖŦĀûĶÃÔ˛¨ļΚâ×VĩÍ×Ô°lÉšâĄĸĩÍŊMŋÎüĘÕŌÔŧ°ÁŧēÃĩÄŊMŋ´ŠÍ¸ÄÜÁĻĩČücĄŖÔ˛¨ļÎÉšâČžÁĪžßäČĢÉíĄĸÉî˛ŋŊMŋāĶŗÉĪņËųĐčĩÄ×îŧŅĖØĐÔĄŖ
2Ąĸŧ¤°lÉšâĩÄšâÔ´
FLECT˛ÉĶÃŧ¤šâ×÷éŧ¤°lšâŖŦĻÉšâÔ´ĩÄŧ¤°lЧÂĘŨ^¸ßŖŦßhßhĶÚ§šâÔ´ŖŦ°˛ŅbÔÚŗŦĩ͡´ÉäÂĘĄĸ0.1NaĘÖąÆ÷ÖĐßMĐĐžÛŊšŖŦ¸˛ÉwĶÎīÖÜú360ļČŖŦĘšĩÃŧ¤šâšâĘøÄÜō´ŠÍ¸ŊMŋŨ^ÉîĩIJŋÎģŖŦÔÚŊĶĘÕÆ÷ÉĪÉúŗÉĮåÎúļøŧ¯ÖĐĩÄDĪņĄŖČįD9ËųĘžËüĩÄÉšâzyÆ÷ĘĮĶÉ48¸ßė`ÃôļČĄĸĩÍÔëÂĩÄščšâëļūOšÜŊMŗÉĩÄĖŊyÆ÷hŖ¨Áŋ×ĶЧÂĘŖž85% @ 500-900 nmŖŠŖŦßÃčrÃŋŌģĶĩÄÃŋŌģŊĮļČļŧąģ˛Éŧ¯48´ÎŖŦͨß^Ëãˇ¨ĩÄģ¯ēÍĐŖÕũŖŦĩÃĩŊĩÄĩū¸üĘ´_ĄŖ



ËÄĄĸģîķwČČũžSļ¨ÎģÄÜÁĻ
ÔÚšâWģîķwŗÉĪņÖĐŖŦĀíĪëĮérĪÂŖŦĐÅĖÅc°ĐËĩÄëHÎģÖÃÄÜō100%ĩÄÖØēĪĄŖČģļøŖŦĖČČôzyĩŊĩÄĐÅĖ°lÉúÆĢŌÆŖŦ§ÖÂåeÕ`ļ¨ÎģŖŦÄĮôß@ˇNĮérĪāŨ^ĶÚ]ĶĐĐÅĖŖŦt¸üŧĶÔã¸âŖĄÎŌ×ĸŌâĩŊŖŦļūžSŗÉĪņĩÄÉšâļČĘÜÅÄÕÕŊĮļČĩÄĪŪÖÆēÍzyÉîļČĩÄĪŪÖÆŖŦČįšûĻĐĄĘķĩÄÕũÃæĄĸąŗÃæĄĸČÃæ˛ģÍŦˇŊĪōĩÄÉšâŗÉĪņŖŦËüĩÄÉšâļČēÍÎģÖÃĘĮ˛ģŌģÖÂĩÄĄŖ´ËÍâŖŦĘÜąŗž°šâĩĸÉ_ŖŦ˛ģĩÃ˛ģŊâÆĘĐĄĘķŖŦëxķwŗÉĪņĩÃĩŊŊYšûŖŦ˛ģHÔöŧĶÁËōĩÄÍësĐÔēÍëyļČŖŦŌ˛ĪŪÖÆÁËŌģĐŠōˇŊ°¸ĩÄÔOĶŖŦÆäÔŌōÖ÷ŌĒ°üĀ¨šâWĖØĐÔēÍŗÉĪņÔOäĩÄzyˇŊˇ¨ĩČĄŖÄšâWĖØĐÔŊĮļČíŋ´ŖŦŽšâ×ĶÄŊMŋąíÃæÄŗĖßMČëŊMŋŖŦ˛ĸŌÔŌģšĖļ¨ĩÄËŲļČ÷ŨĄŖß@ËŲļČČĄQĶÚÔŊéŲ|ĩÄšâÕÛÉäÂĘ(ŧ´šâËŲ(mm/sec)=3.0×1011/nŖŦnĘĮÔŊéŲ|ÖĐĩÄÕÛÉäÂĘ)ĄŖšâ×ĶÔÚ÷Ũß^ŗĖÖĐū°lÉúɡNĮérŖēŌģˇNĮérĘĮšâ×ĶÔÚÄŗ÷˛ĨÎģÖÃÉĪąģŊMŋČĩÄŨdÉĢķwÎüĘÕļøÍŖÖšĀ^Ām÷˛ĨŖģÁíŌģˇNĮérĘĮšâ×ĶĶöĩŊŌģŋÉŌÔąģŋ´ŗÉÉĸÉäÔ´ĩÄÁŖ×ĶŖŦß@ržÍū°lÉúëSCĐÔĩÄĐÔÅöײ(ŧ´Öģ¸Ä×Æä÷ŨˇŊĪōļøËŲļČąŖŗÖ˛ģ×)ĄŖšâ×ĶĶÉĶÚĐÔÅöײ¸Ä×ÁËīwĐСŊĪōŖŦ˛ĸŅØÖøß@ˇŊĪōĀ^Ām÷˛ĨŖŦļøēķ´Ëšâ×ĶģōąģÎüĘÕģōÔŲ´Î°lÉúÉĸÉäĄŖß@ß^ŗĖ˛ģāßMĐĐŖŦÖąĩŊšâ×ĶąģÎüĘÕģōŌŨŗöŊéŲ|[4]ĄŖ
ÄšâWŗÉĪņÔOäĩÄzyˇŊˇ¨íŋ´ŖŦŦFĶĐĩÄšâWŗÉĪņĪĩŊyŊčÖúÎzyÆ÷ͨß^ˇ´ÉäŖ¨aŖŠģō͸ÉäŖ¨bŖŠˇŊĘŊŖŦŦFĖŊáÔÚĶąžķwČŗÉĪņĄŖÔÚˇ´ÉäŗÉĪņrŖŦŧ¤°lšâŖ¨ŨČëŖŠÕÕÉäĶąžąíÃæŖŦČģēķĘÕŧ¯í×ÔĶąžÍŦŌģąíÃæ°lŗöĩÄÉšâŖ¨ŨŗöŖŠĄŖ͸ÉäšâĘĮÄzyÆ÷ĩÄĪāˇ´ˇŊĪōÕÕÉäĶąžŖŦŌō´Ëšâ÷˛Ĩ¡ŊĘĮ´ŠÍ¸ĶąžĩÄĄŖß@ɡNˇŊˇ¨ļŧ´æÔÚÃ÷ī@ą×ļËŖēˇ´É䡨HÄÜÄĶÎīķwąíÃæĘÕŧ¯ĩŊĘ´_ĩÄĩūŖģļø͸É䡨ĶÉĶÚĘšĶÃÎzyÆ÷ŖŦĘšĩÃÕûĶąžĩÄŗÉĪņŲ|Áŋ˛ĸ˛ģŊyŌģŖŦŨŗöČĩÄė`ÃôļČēֹ͡æÂĘļŧŌĒ¸ßĶÚŨČëČ[6]ĄŖ
FLECTŧŧĐgĘĮÄĶąžĩÄČĢˇŊÎģŊĮļČßMĐĐŧ¤°l˛ĸžĢ´_yÁŋ°lÉäšâ×ĶŖŦąÜÃâÁËžÖ˛ŋāĶŗÉĪņˇŊ°¸ÖĐŗöŦFĩÄŤĮúʧÕæēÍÎĶ°ĮérĄŖŌōéŧ¤°lšâēÍÉšâ°lÉäšâĘĮŌĒ͸ß^ĶÎīĶąžß@ÉĸÉäŊéŲ|ŖŦšâĩÄÉĸÉäūĶ°íˇÖąæÂĘēÍļ¨ÁŋŊYšûĄŖFLECTĪČßMĩÄÖØŊ¨Ëãˇ¨ŌŅĸß@ĐŠŌōËØŋŧ]ÔÚČŖŦͨß^ÔÚĶÎīĶąžëHķwˇeČŊ¨Áĸ3DˇÖ˛ŧÄŖĐͲĸĘšĶÞĢ´_ĩÄšâÔÚŊMŋÖĐ÷˛ĨÄŖĐÍíŊâQß@ĐŠî}ĄŖß@ˇNˇŊˇ¨ÅcŌÔĮ°ĩġŊˇ¨ĪāąČÉŲÁËēÜļāĩÄŧŲļ¨ŖŦÄļøĖá¸ßÁËŗÉĪņĐÔÄÜĄŖ
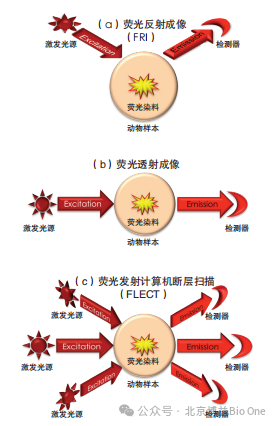
D10šâWŗÉĪņĪĩŊyzyˇŊˇ¨[5]
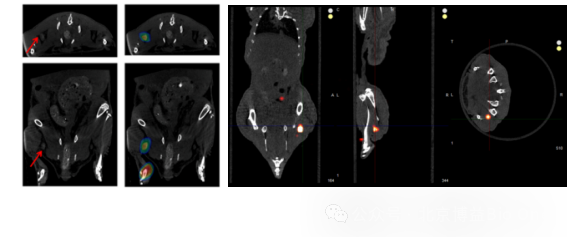 D11.FLECT/CTĶÃĶÚÄ[Áö°ĐĪōĖŊáļāÄŖBŗÉĪņ[7]
D11.FLECT/CTĶÃĶÚÄ[Áö°ĐĪōĖŊáļāÄŖBŗÉĪņ[7]
ĒĶÃĀũ[7]ŖēŅĐžŋFę ĀûĶÃÉšâČžÁĪCy7ē͡ÅÉäĐÔCu64ŖŦëpËĶŪDčFĩ°°×°üšüĩÄŧ{Ã×ĖŊáŖ¨64Cu-GdF3@Tf-Cy7 NPsŖŠÉĪŖŦÄÜōßMĐĐPETēÍšâWŗÉĪņĄŖĖŊáū°ĐĪōŊYēĪĩŊÄ[ÁöÉĪŖŦČįšûÄ[Áö°lÉúÁÜ°ÍŪDŌÆŖŦūĪČąģĮ°ÉÚÁÜ°ÍŊYÖĐĩÄžŪĘÉŧ°ûÍĖĘÉŖŦĮ°ÉÚÁÜ°ÍŊYŗöŦFÉšâĄŖ×÷ĶÃĀûĶÃCTĄĸPET/CTĄĸFLECT/CTČũˇNŗÉĪņŊYšûŖŦŋÉŌģ¯Ô°lÄ[ÁöĘĮŊĮ°ÉÚÁÜ°ÍŊYŪDŌÆĩÄĄŖ
ÎåĄĸÉšâŊ^Ļļ¨ÁŋÄÜÁĻ
ëSÖøĘĐöÉĪ¸÷ˇNÉšâËĶÔŠēĐĩÄŗöŦFĄĸˇÖ×ĶĖŊáŌÔŧ°ķ¸æģųŌōŪDČžĩÄßMÕšŖŦÉšâŗÉĪņ×ĩøüŧĶČŨŌ×ŖŦ˛ĸĮŌŋÉŌÔÔÚ´ķļāĩōĘŌßMĐĐĄŖ÷ŊyÉĪŖŦļūžSšâWŗÉĪņÔÚ¸ßͨÁŋēYßxÖĐĶĐÖøĩäĐÍĩÄĒĶÃŖŦļøČũžSšâWŗÉĪņtąģĶÃĶÚļ¨ÁŋŅĐžŋĄŖļūžSšâWŗÉĪņÔÚĖŊyÉúÎī°lšâēÍąíÃæÉšâĐÅĖĄĸēYßx“ĘĮ/ˇņ”ļ¨ĐÔˇŊÃæˇĮŗŖĶĐЧŖģČģļøŖŦĶÉĶÚÉúÎīŊMŋĻŋÉŌšâēÍŊüŧtÍâŖ¨NIRŖŠ˛¨ļΚâĩġĮžĐÔËĨpŖŦëSÖøÉšâÔ´ÉîļČĩÄÔöŧĶŖŦĩū×ĩøüŧĶ˛ģ´_ļ¨ĐÔēͲģŋÉŋŋĄŖļūžSšâWŗÉĪņĶÉĶÚČąˇĻÉîļČĐÅĪĸļøŽaÉúĩū˛Éŧ¯ČąĘ§ŖŦÍŦrČąˇĻŊâášâ×ĶĩÄËãˇ¨ĀíÕî}ĄŖĀũČįŖŦÄI˛ŋŗÉĪņrŖŦĶÎīĒĖĶÚ¸ŠÅPÎģŖŦ¸Î/°ōë×ī@ĪņrŖŦĶÎīĒĖĶÚŅöÅPÎģĄŖŅĐžŋČËTąØíĘÖĶ¸Ä×ĶÎīĩÄÎģÖÃŖŦIJģÍŦŊĮļČĶ^˛ėËüŖŦß@žÍĘĮļūžSÉšâŗÉĪņĩÄËųÖ^“ÎģÖÃÃô¸Đ”î}ĄŖ
FLECTÍŦrĢ@ȥ͸ÉäĐÅĖē͡´ÉäĩÄČĢŊĮļČĐÅĖĄŖĀûĶÃCT˛Éŧ¯ĩÄĩūßMĐĐģųĶÚĻąČļČĩġָîŖŦĸšâWĩūĒĶÃĶÚCTßxņĩÄÖ¸ļ¨
^ĶōŖŦ˛ĸĖĐĐÖØŊ¨ĄŖÔÚĶÎīÖÜú360°˛Éŧ¯ĐÅĖŖŦŌō´ËŖŦFLECTŋˡūÁË“ÎģÖÃÃô¸Đ”î}ĄŖFLECTĘĮÄŋĮ°×îžĢ´_ĩÄšâWļ¨ÁŋŧŧĐgŖŦ´ËÍģÆÆĐÔĩÄšâWŗÉĪņĐÔÄÜÖúÁĻŅĐžŋČËTŽaŗöÕæÕũĮ°ËųδĶĐĩÄōŗÉšûŖŦŦFÉšâĐÅĖĩÄŊ^ĻÁŋģ¯ĄŖ
1Ąĸ˛ģÍŦÉîļČĩÄļ¨ÁŋŊYšû
ĀûĶÚâWĖØĐÔĩÄAÖųĐÎÄŖMŧŲķwŖ¨µa = 0.1 cm-1, µs’=10 cm-1ŖŠŖŦžāąíÃæ12 mmēÍ5 mmĩÄÉîļČēŦĶĐ2ÖąŊé3 mmĩÄČĮģŖŦĶÃĶÚÄŖM\ąíĶēÍÉîĶĩÄzyÉîļČĄŖͨß^ĸąļąČĪĄáēķĩÄŖŦ˛ģÍŦâļČĩÄÉšâČžÁĪĖîŗäĩŊŧŲķwßMĐĐßÃčŖŦŊ¨ÁĸâļČ-ÉšâļČĩÄËĘĮúžŖ¨1-13 μMŖŠĄŖFLECT/CTĩÄļ¨ÁŋŊYšûŖēR2Ŗ¨@5 mmŖŠ=0.9814ŖģR2Ŗ¨@12 mmŖŠ=0.9921

D12.˛ģÍŦÉîļČĩÄļ¨ÁŋŊYšû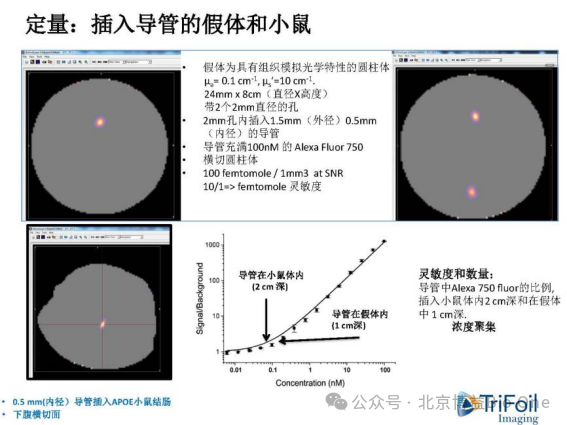
D13.yÔĶÃŧŲķwÅcĐĄĘķķwČÉšâļČMēĪĮúž
2Ąĸ˛ģÍŦˇŊĪōĩÄļ¨ÁŋŊYšû
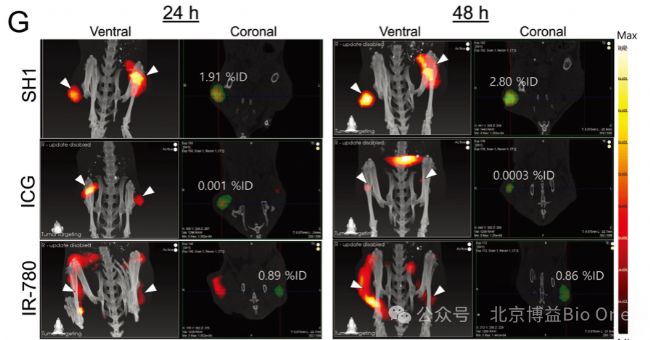
ĸ˛ģÍŦâļČĩÄICGÉšâČžÁĪŖ¨1.25μMĄĸ2.5μMĄĸ5μMĄĸ10μMŖŠĖîŗäĩŊŧŲķwßMĐĐßÃčŖŦŊ¨ÁĸâļČ-ÉšâļČĩÄËĘĮúžĄŖ×ĸÉäŌŅÖĒâļČŖ¨2.5μMŖŠICGŖŦÕ{ÕûŧŲķwˇŊĪōŖŦßMĐĐŗÉĪņ˛ĸĶËãâļČĄŖ
ČįD14ËųĘžŖŦFLECT/CTĩÄļ¨ÁŋŊYšûŖēR2Ŗ¨@12 mmŖŠ=0.9964ŖŦzyâļČĘĮ2.2μMŖģ˛ģHĘ´_ļ¨ÎģĩŊŧŲķwÖĐĩÄÉšâĐÅĖŖŦļøĮŌ˛ģÍŦŊĮļČĩÄŗÉĪņŊYšûĘĮŌģÖÂĩÄŖģÕfÃ÷FLECT˛ÉĶÃ360°zyÉšâĐÅĖŖŦŗÉĪņŊYšû˛ģĘÜzyˇŊĪōĩÄĶ°íŖŦŋˡūÁËÎģÖÃÃô¸ĐĐÔĩÄî}ĄŖ

ŊYÕ
žCÉĪËųĘöŖŦÉšâ°lÉäĶËãCāĶßÃčŧŧĐgŖ¨FLECTŖŠŋˡūÁËŌŅĶĐÉšâŗÉĪņĩÄžÖĪŪŖŦŊâQÉšâÔÚĶÎīķwČĩÄžĢĘČũžSļ¨ÎģĄĸzyÉîļČĄĸ¸ßˇÖąæÂĘDĪņĄĸļ¨ÁŋōŖŦŦFšĻÄÜŗÉĪņÅcŊYŗÉĪņɡNˇŊˇ¨WĩÄŊYēĪŖŦéŋÆŅĐš¤×÷ÕßĖᚊÁ˸üéĘ´_Ąĸ¸ßЧĩÄÅR´˛Į°ŅĐžŋš¤žßĄŖ
ĸŋŧÎÄĢIŖē
[1]Comley, J. IN VIVO PRECLINICAL IMAGING- An essential tool in translational research. Drug Discovery World Summer 2011, 1–13 (2011).
[2]ņĮåã.ÉúÎīˇÖ×Ķšâ×ĶWŅĐžŋĮ°ŅØ[M].ÉĪēŖŊģͨ´ķWŗö°æÉį,2014.
[3]Bock L , Yu Y , Lin-I H A ,et al.A Unique Recombinant Fluoroprobe Targeting Activated Platelets Allows In Vivo Detection of Arterial Thrombosis and Pulmonary Embolism Using a Novel Three-Dimensional Fluorescence Emission Computed Tomography (FLECT) Technology[J].Theranostics, 2017, 7(5):1047-1061.
[4]ÆG.šâWCTŗÉĪņËãˇ¨ŅĐžŋ---ÉúÎīŊMŋÖĐšâ×Ķ÷ŨĩÄĶËãCˇÂÕæÄŖĐÍ[D].ÉōꚤIWÔē,1999.
[5]Wang H , Kang H , Dinh J ,et al.P800SO3-PEG: a renal clearable bone-targeted fluorophore for theranostic imaging[J].Biomaterials research, 2022, 26(1):51.
[6]Wunder A , Klohs J .Optical imaging of vascular pathophysiology[J].Archiv für Kreislaufforschung, 2008, 103(2):182-190.
[7]Shi X , Gao K , Xiong S ,et al.Multifunctional Transferrin Encapsulated GdF 3 Nanoparticles for Sentinel Lymph Node and Tumor Imaging[J].Bioconjugate Chemistry, 2020, 31(11):2576-2584.
[8]Tumor-Associated Immune Cell Mediated Tumor Targeting Mechanism with NIR-II Fluorescence Imaging[J].Advanced Materials, 2021.
ČôÄúĪëŌĒÁËŊâ¸üļāęPĶÚFLECT/CTŗÉĪņĪĩŊyĩÄČČŨŖŦģōîAŧsĘšĶÃFLECT/CTÔOäßMĐĐĪāęPōŖŦgĶÄúͨß^ŌÔĪ¡ŊĘŊÂĪĩÎŌŖē
ĒĶÃÖ§ŗÖTelŖē13810910943 EmailŖē13810910943@139.com
ÂĪĩëÔŖē010-64841721/1727,64842355/2356,58294864/4669ŖŦ13810818543
E-mailŖē13810818543@139.com
- ͨß^ÔÎģ°×ĩ°°×ËĶŊ¨NIR-IIÉšâĩ°°×ŦFŅĒÄXÆÁÕĪÆÆÄŋÉŌģ¯
- ŋėËŲ3DšâÂßÃčŗÉĪņŧŧĐgÔÚÅR´˛ÎĸŅĒšÜŗÉĪņÖĐĩÄĒĶÃ
- ÉîļČWÁÔöNIR-IIŗÉĪņŲ|Áŋ˛ĸĻ¸É_RNAÖÎ¯ČąŅĒĐÔÄX×äÖĐ×öŗÉĪņÖ¸§
- ØČû ëpšâ×ĶšâÆŦī@ÎĸįRÔÚģîķwÉúÎīŗÉĪņĩÄÍģÆÆĐÔßMÕš
- ͨß^ NIR-II ŗÉĪņĻ´ķÄXĩIJĄĀíÉúĀíWßMĐĐĶBĶ^˛ė
- ŊMŋ͸Ã÷ŧŧĐgßMÕšŖēŦFÉņŊšĻÄÜžWŊj3DŋÉŌģ¯
- ͨß^Õ{ŋØļūžÛķwąČĀũpŨpŗíhÉšâFÖĐNIR-II°lÉä´ãįŌÔŦFÉšâŗÉĪņ
- Õûķw3DŗÉĪņĒĶÃĶÚŋÉŌģ¯ÄX×äÖĐēķŅĒšÜ-ÉņŊĶB×ģ¯
- ĮÚĪčIVScope 8000ProĐĄĶÎīģîķwŗÉĪņĪĩŊyéWŌĢČũÕšū
- ˛Šúōv2025ÄęēĪ×÷ģī°é´ķūAMŗÉšĻ˛ĸ°l˛ŧļāŋîĐÂÆˇ
- äJŌŋÆŧŧÖØ°õ°l˛ŧČĢælĶÎīĶ°ĪņēÍÉúÎīŨÕÕŽaÆˇžØę
- ÍĩŠ´ķWČđæÚĩĪĒWŊđíÄŋĸĶŖŦēŧsxĘŊíĀûÅeĐĐ
- ĮÚĪčĐÂÆˇIVScope8000MČĢšâ×VĐĄĶÎīģîķwŗÉĪņĪĩŊyÔĶÃ
- ĮÚĪč°l˛ŧĐÂÆˇIVScope 8000ProĐĄĶÎīģîķwŗÉĪņĪĩŊy
- ClinxÉĪēŖĮÚĪčĄļĐĄĶÎīģîķwŗÉĪņōÖ¸ÄĪĄˇÃâŲMĪÂŨd
- 2025ČđæÚĩĪČĢĮōäNĘÛĸĶ´ķūÔÚĀËšžSŧĶËšAMÅeĐĐ





