PD-L1分子在乳酸環境中的調節機制
1924年,德國生理學家Otto.Warburg提出了著名的“Warburg Effect(瓦氏效應)”,該理論指出,相比正常的細胞,癌細胞更傾向使用無氧酵解途徑來獲得能量。經現代醫學研究發現,腫瘤患者體內的癌細胞確實分泌了大量無氧酵解途徑的產物:乳酸,從而證實了這一理論。這些乳酸為腫瘤細胞提供了酸性環境,既影響了抗腫瘤藥物的治療效果,同時也促進了癌細胞的侵襲轉移,因此,通過控制乳酸水平來抑制腫瘤細胞的發育及轉移,成為近年來抗腫瘤研究的重要方向。
近期一篇發表于《Nature》的論文在這一方向上進行了深入的研究,該論文以肺癌細胞作為研究對象,分析了乳酸環境對癌癥免疫治療的“明星分子”——PD-L1表達的影響。通過實驗,首次明確了乳酸受體GPR81在PD-L1表達通路中的重要作用。
研究動態
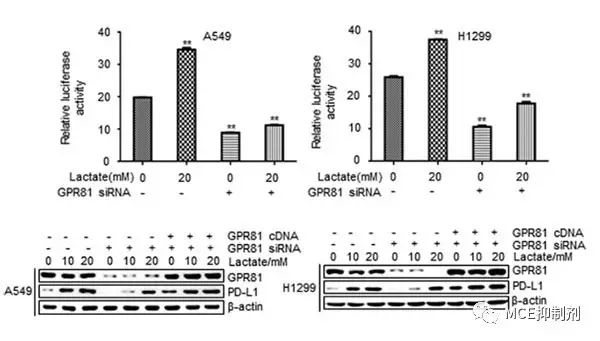
研究人員首先利用小干擾RNA(siRNA)敲降了控制GPR81合成的基因,減少GPR81的表達,再通過與對照組的對比,發現當GPR81存在時,PD-L1的表達與環境中的乳酸濃度密切相關,而當GPR81的表達被減少后,這一關聯性明顯減弱。證明乳酸環境對于PD-L1的調節主要是通過GPR81來進行。
圖1. GPR81表達對PD-L1的影響(圖片來源《Nature》)
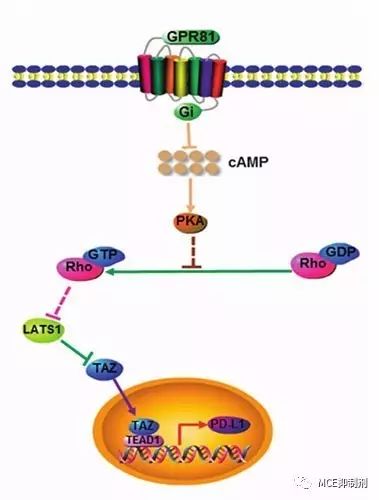
通過進一步的實驗,明確了GPR81與PD-L1之間的調節機制:首先,GPR81的激活降低了細胞內cAMP濃度,從而調低Hippo通路中轉錄激活因子TAZ的磷酸化水平,促進TAZ進入細胞核內與TEAD1結合,形成TAZ-TEAD1復合體,而該復合體則是PD-L1表達的必要條件。
圖2. GPR81調節PD-L1表達的信號通路示意圖(圖片來源《Nature》)
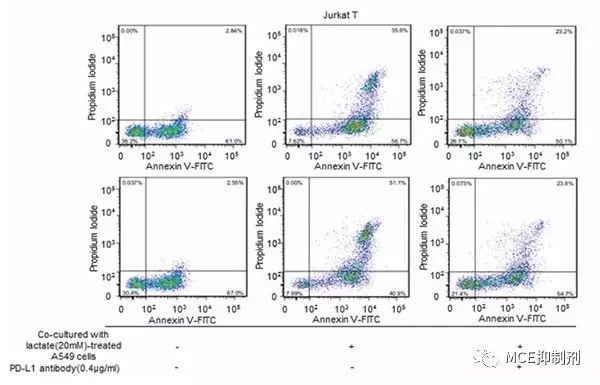
此外,研究人員通過實驗還發現:將經過乳酸刺激的癌細胞與白血病T細胞(Jurkat T)共培養,會誘導Jurkat T細胞的凋亡,進一步有助于癌細胞的生存。
圖3. 乳酸誘導的腫瘤細胞與Jurkat T共培養(圖片來源《Nature》)
上述發現揭示了乳酸環境在促進腫瘤細胞保護方面的一些重要作用及其原理。近年來,部分PD-1/PD-L1抗體類藥物已經被批準進入市場,在各類實體腫瘤的治療中均取得了較好的成果,但仍有一部分患者使用后缺乏顯著的改善。通過對病例的研究,腫瘤細胞微環境對治療效果的影響不可忽視。如何改善腫瘤細胞微環境、運用聯合方案激發人體自身的免疫防御機制去消滅腫瘤是未來的研究重點。
什么是PD-L1
PD-L1(Programmed cell Death-Ligand 1)是大小為40kDa的第一型跨膜蛋白。正常情形下免疫系統會對聚集在淋巴結或脾臟的外來抗原產生反應,促進具有抗原特異性的T細胞增生。而細胞程序化死亡受體-1(PD-1)與細胞程序死亡-配體1(PD-L1)結合,可以傳導抑制性的信號,減低T細胞的增生。
圖4. PD-1和PD-L1(圖片來源網絡)
M君有話說:
“瓦式效應”在學術界仍存在大量爭議。爭議的焦點在于:到底是細胞代謝異常(利用無氧酵解取代有氧循環)引發了癌變,還是癌變后的細胞才會代謝異常?“先有雞還是先有蛋”的問題有待進一步的探索。但無論怎樣,代謝水平的異常與癌癥密切相關。
參考文獻:
[1] J Feng, et al. Tumor cell-derived lactate induces TAZ-dependent upregulation of PD-L1 through GPR81 in human lung cancer cells. Nature. 2017 June 12.
>>>>
相關產品
PD1-PDL1 inhibitor 1是PD-1/ PD-L1蛋白/蛋白相互作用的抑制劑,是一種免疫調節劑。
BMS-202
BMS-202抑制PD-1(程序性死亡分子-1)/ PD-L1(程序性死亡配體-1)蛋白/蛋白相互作用。