動物活體成像系統(tǒng)助力開發(fā)通過血腦屏障靶向治療帕金森病的納米平臺
近日,華南師范大學生命科學學院關燕清教授課題組在開發(fā)靶向治療帕金森病的納米平臺中取得新進展,相關研究成果已在線發(fā)表在國際權威期刊《Advanced Healthcare Materials》(IF=11.092、一區(qū)top期刊)。

帕金森病(PD)作為一種常見的神經退行性疾病,已經嚴重威脅到人類健康,其主要特征是黑質致密部多巴胺能神經元的退行性喪失和大腦中多巴胺的減少。
基因療法可以通過引入治療性基因(DNA/RNA)或通過替換、沉默或糾正有缺陷的基因來治療疾病,這為PD提供了一條很有前途的潛在治療途徑。然而,基因藥物很容易在血液或細胞中降解,很難進入細胞;更重要的是,血腦屏障(BBB)的存在阻止了大多數(shù)藥物從血液進入大腦,這成為治療PD的主要障礙。
因此,有必要開發(fā)一種新的藥物輸送平臺,既能將基因藥物裝載到細胞內,又能穿透血腦屏障。
基于上述背景,關燕清教授課題組開發(fā)了一種與非侵入性近紅外輻射相結合,具有良好生物相容性的MgOp@PPLP納米平臺。該納米平臺使用MgO納米顆粒作為基底,聚多巴胺作為外殼,將抗SNCA質粒包裹在內部,并在表面修飾聚乙二醇、乳鐵蛋白和葛根素來分別改善顆粒的親水性、腦靶向性和抗氧化性能。
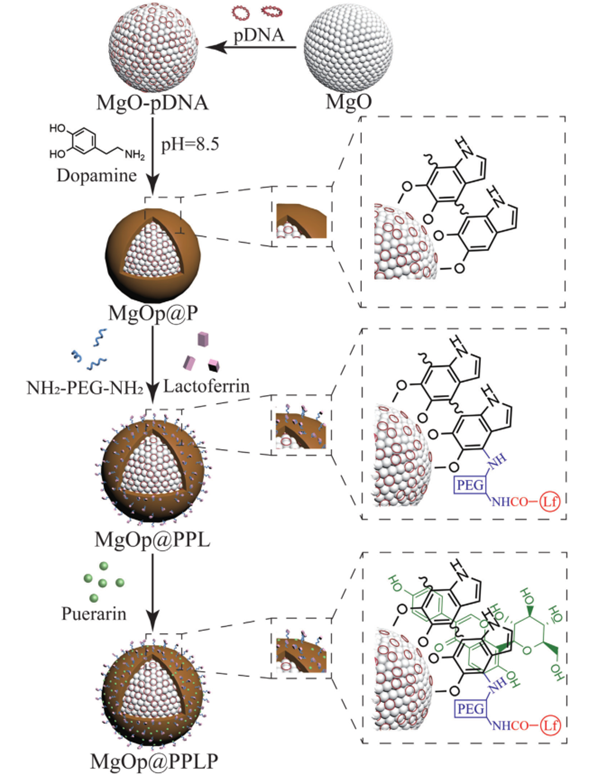
MgOp@PPLP具有優(yōu)異的近紅外輻射(NIR)響應。在光熱效應的引導下,這些MgOp@PPLP顆粒能夠穿透血腦屏障,被神經細胞攝取,發(fā)揮基因治療和抗氧化治療的作用。在體內和體外帕PD模型中,MgOp@PPLP均表現(xiàn)出良好的神經保護作用。這些結果表明,MgOp@PPLP納米平臺可以作為一種對抗神經退行性疾病的理想材料。
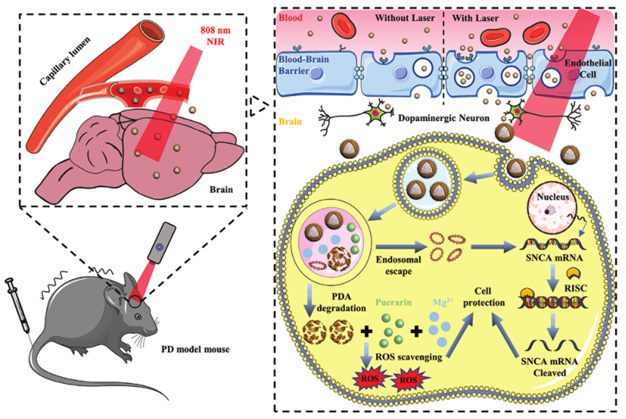
MgOp@PPLP通過血液循環(huán)到達血腦屏障,并在近紅外輻射的幫助下穿透血腦屏障,進入到神經細胞中。隨之,NPs被運輸?shù)饺苊阁w,在PDA殼解體后,釋放pDNA和Pue。pDNA可以表達siRNA,通過SNCA mRNA降解抑制α-syn表達;PDA和Pue能清除細胞內的ROS,達到保護神經細胞和治療PD的目的。
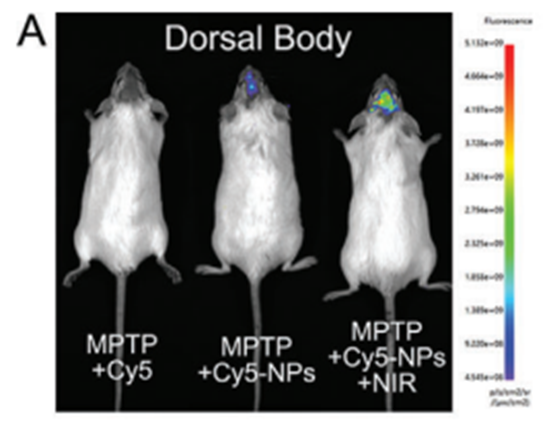
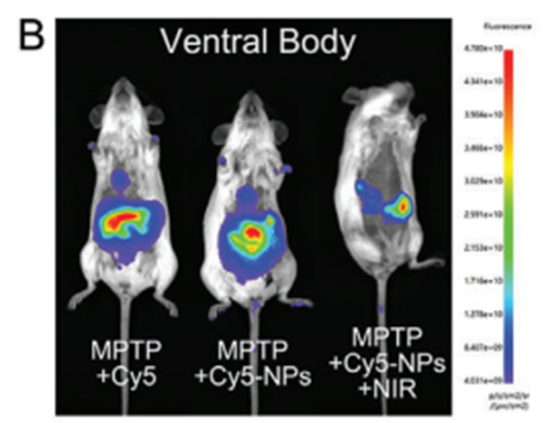
研究中,在觀察MgOp@PPLP在PD模型中的生物分布時,使用了AniView系列多模式動物活體成像系統(tǒng)進行拍攝。
論文鏈接:https://doi.org/10.1002/adhm.202201655

帕金森病(PD)作為一種常見的神經退行性疾病,已經嚴重威脅到人類健康,其主要特征是黑質致密部多巴胺能神經元的退行性喪失和大腦中多巴胺的減少。
基因療法可以通過引入治療性基因(DNA/RNA)或通過替換、沉默或糾正有缺陷的基因來治療疾病,這為PD提供了一條很有前途的潛在治療途徑。然而,基因藥物很容易在血液或細胞中降解,很難進入細胞;更重要的是,血腦屏障(BBB)的存在阻止了大多數(shù)藥物從血液進入大腦,這成為治療PD的主要障礙。
因此,有必要開發(fā)一種新的藥物輸送平臺,既能將基因藥物裝載到細胞內,又能穿透血腦屏障。
基于上述背景,關燕清教授課題組開發(fā)了一種與非侵入性近紅外輻射相結合,具有良好生物相容性的MgOp@PPLP納米平臺。該納米平臺使用MgO納米顆粒作為基底,聚多巴胺作為外殼,將抗SNCA質粒包裹在內部,并在表面修飾聚乙二醇、乳鐵蛋白和葛根素來分別改善顆粒的親水性、腦靶向性和抗氧化性能。

△ 圖1 合成MgOp@PPLP的示意圖
MgOp@PPLP具有優(yōu)異的近紅外輻射(NIR)響應。在光熱效應的引導下,這些MgOp@PPLP顆粒能夠穿透血腦屏障,被神經細胞攝取,發(fā)揮基因治療和抗氧化治療的作用。在體內和體外帕PD模型中,MgOp@PPLP均表現(xiàn)出良好的神經保護作用。這些結果表明,MgOp@PPLP納米平臺可以作為一種對抗神經退行性疾病的理想材料。

△ 圖2 MgOp@PPLP治療PD的示意圖
MgOp@PPLP通過血液循環(huán)到達血腦屏障,并在近紅外輻射的幫助下穿透血腦屏障,進入到神經細胞中。隨之,NPs被運輸?shù)饺苊阁w,在PDA殼解體后,釋放pDNA和Pue。pDNA可以表達siRNA,通過SNCA mRNA降解抑制α-syn表達;PDA和Pue能清除細胞內的ROS,達到保護神經細胞和治療PD的目的。
研究中,在觀察MgOp@PPLP在PD模型中的生物分布時,使用了AniView系列多模式動物活體成像系統(tǒng)進行拍攝。


腦A)和內臟B)中Cy5-NPs生物分布的圖像
論文鏈接:https://doi.org/10.1002/adhm.202201655
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com





