代謝組學(xué)非靶標(biāo)代謝流助力揭示18SrRNA中m6A控制
文章標(biāo)題:N6-methyladenosine (m6A) in 18S rRNA promotes fatty acid metabolism and oncogenic transformation
發(fā)表期刊:Nature Metabolism
影響因子:19.865
作者單位:中山大學(xué)第一附屬醫(yī)院
百趣生物提供服務(wù):非靶標(biāo)代謝流分析
研究背景
能夠快速無(wú)限地生長(zhǎng)和分裂是癌細(xì)胞最廣為人知的特征之一,癌細(xì)胞核糖體生物合成失調(diào)以及mRNA翻譯活性異常,均會(huì)促進(jìn)癌癥的進(jìn)展,然而,癌癥中核糖體生物生成失調(diào)的分子機(jī)制仍不清楚。
核糖體生物發(fā)生是一個(gè)高度協(xié)調(diào)的過(guò)程,最近的研究表明,不同的RNA轉(zhuǎn)錄后修飾在基因表達(dá)和癌癥進(jìn)展的調(diào)節(jié)中均發(fā)揮重要作用。rRNA占細(xì)胞總RNA的80%以上,并受到不同的修飾,但是對(duì)于rRNA修飾在調(diào)節(jié)癌癥中的rRNA加工和功能中的功能和機(jī)制知之甚少。關(guān)于mRNA中m6A的修飾已經(jīng)成為癌癥進(jìn)程的關(guān)鍵信號(hào),而rRNA中m6A修飾的研究還有很多待揭示的問(wèn)題。
為揭示METTL5介導(dǎo)的18S rRNA m6A修飾對(duì)決定細(xì)胞命運(yùn)和生長(zhǎng)的作用,讓我們走入作者的研究故事。
研究結(jié)果
1.METTL5和TRMT112在各種癌癥中上調(diào),并與不良預(yù)后相關(guān)
根據(jù)前人的報(bào)道在rRNA中存在兩個(gè)酶METTL5和TRMT112分別催化18SrRNA上1832位(m6A1832)和28SrRNA上4220位(m6A4220)的甲基化修飾。為了探明m6A修飾在癌癥進(jìn)程中的作用,作者首先對(duì)TCGA數(shù)據(jù)進(jìn)行了分析,發(fā)現(xiàn)包括HCC在大多數(shù)TCGA癌癥類(lèi)型中METTL5和TRMT112均顯著上調(diào)(圖1a-c),并且發(fā)現(xiàn)METTL5和TRMT112的高表達(dá)與肝癌患者的晚期病理分級(jí)、腫瘤分期、總體生存率均相關(guān)(圖1e-h)。為了進(jìn)一步確定上述現(xiàn)象,作者在HCC細(xì)胞系以及HCC組織樣本中做了進(jìn)一步確認(rèn),正如預(yù)期的那樣,無(wú)論在細(xì)胞系還是組織樣本中,相較于對(duì)照組,METTL5和TRMT112的mRNA和蛋白水平均有不同程度的上調(diào)(圖1i-m)。同時(shí)m6A定量檢測(cè)也確認(rèn)了,在HCC細(xì)胞系和HCC患者樣本中m6A1832的修飾顯著增高(圖1n)。顯然METTL5和TRMT112介導(dǎo)的18S rRNA m6A修飾很可能在HCC的進(jìn)程中有重要的作用。
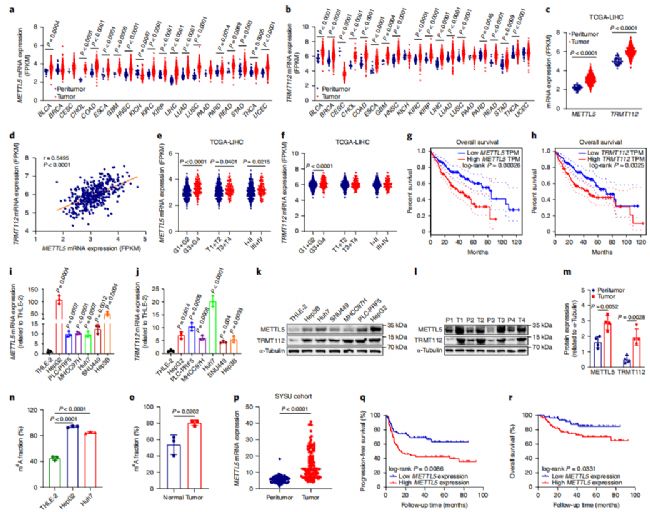
圖1. MettL5在各種癌癥中上調(diào),并與低生存率相關(guān)
2.METTL5的過(guò)表達(dá)在體外和體內(nèi)促進(jìn)肝癌進(jìn)展
為了深入研究METTL5的致癌功能,作者首先構(gòu)建了METTL5過(guò)表達(dá)肝癌細(xì)胞系(圖2a,b),顯然METTL5的過(guò)表達(dá)顯著的增加了HCC細(xì)胞中18S rRNA的m6A修飾(圖2c)。不出意外的,METTL5的過(guò)表達(dá)從生長(zhǎng)、遷移、侵襲等各方面促進(jìn)了細(xì)胞系的活力(圖2d-k)。表明METTL5可以在體外促進(jìn)HCC的進(jìn)展。
回到體內(nèi)實(shí)驗(yàn),METTL5的mRNA和蛋白質(zhì)在METTL5過(guò)表達(dá)質(zhì)粒轉(zhuǎn)染的小鼠模型中均顯著上調(diào)(圖2l-n)。腫瘤形態(tài)檢測(cè)與免疫組織化學(xué)實(shí)驗(yàn)同樣從表型角度表明METTL5過(guò)表達(dá)的小鼠腫瘤有更高的增殖活性,綜上所述,METTL5在體內(nèi)體外均會(huì)促進(jìn)HCC腫瘤的發(fā)生。
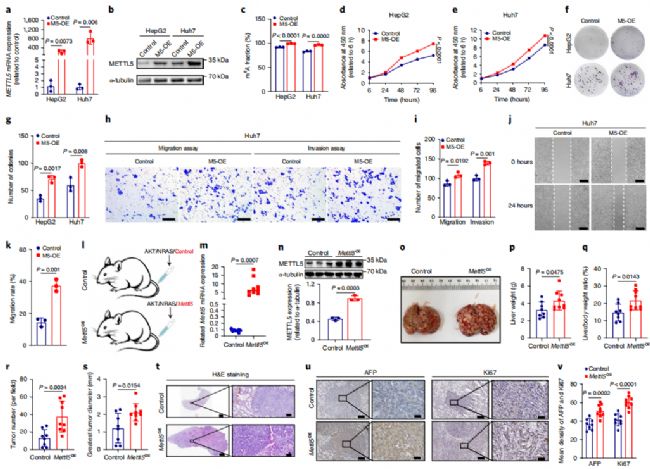
圖2. MettL5的過(guò)表達(dá)在體外和體內(nèi)促進(jìn)肝癌的發(fā)生
3.METTL5介導(dǎo)的18S rRNA m6A修飾調(diào)節(jié)80S核糖體組裝和全局mRNA翻譯
為了全面分析METTL5在HCC中的功能,作者同樣的對(duì)HCC細(xì)胞中的METTL5進(jìn)行了敲低處理(圖3a)。在體外試驗(yàn)中,METTL5敲低的處理使得HCC細(xì)胞的生長(zhǎng)能力和集落形成能力均有所降低(圖3b-d),除了增殖表型之外,METTL5的缺失對(duì)HCC的凋亡以及細(xì)胞周期均產(chǎn)生了不良的影響(圖3e-l),結(jié)合上文的過(guò)表達(dá)數(shù)據(jù),表明METTL5確實(shí)對(duì)HCC細(xì)胞起到了促進(jìn)的作用。
作者進(jìn)一步探究METTL5的作用機(jī)制,發(fā)現(xiàn)在METTL5缺失的細(xì)胞中,18S rRNA的m6A修飾顯著減少(圖3m),同時(shí)為了確定METTL5對(duì)18S rRNA的m6A的影響并非是通過(guò)影響18S rRNA表達(dá)量導(dǎo)致的,作者對(duì)18S rRNA表達(dá)量進(jìn)行了檢測(cè)(3圖o)。18S rRNA是核糖體的主要成分,作者進(jìn)一步研究METTL5對(duì)核糖體功能的影響機(jī)制,多聚體分析表明METTL5的敲減會(huì)使80S核糖體組裝受損(圖3q)。
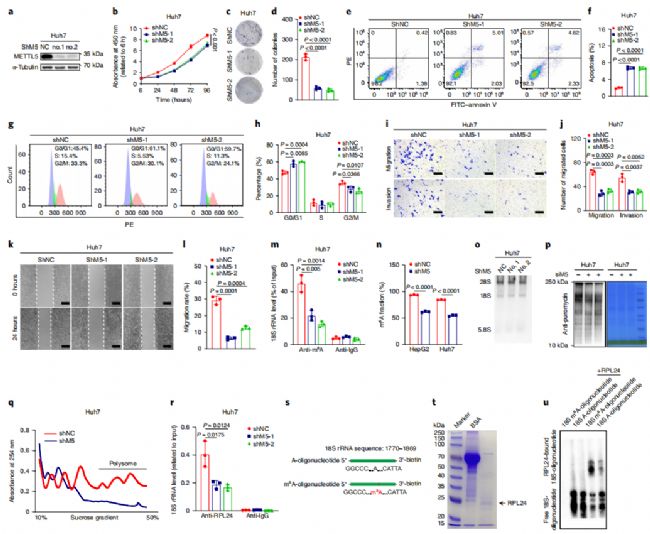
圖3. MettL5基因敲除體外抑制肝癌的發(fā)生
通過(guò)核糖體測(cè)序分析發(fā)現(xiàn)。受METTL5缺失影響的mRNA主要富集于非酒精性脂肪肝、脂肪酸生物合成等途徑,表明METTL5對(duì)HCC進(jìn)展的影響很可能與脂肪酸代謝重組相關(guān)(圖4a-c)。脂質(zhì)組學(xué)分析表明受METTL5敲除影響顯著降低的脂質(zhì)包括游離脂肪酸、甘油三酯、膽固醇(圖4d-f)。為了確認(rèn)這些受影響的脂質(zhì)的來(lái)源信息,作者做了[U-13C]葡萄糖的代謝流分析,發(fā)現(xiàn)許多長(zhǎng)鏈脂肪酸及其下游產(chǎn)物均被U-13C標(biāo)記,表明這些脂肪酸來(lái)源于葡萄糖的生物合成,而隨著METTL5的敲除,這些碳代謝產(chǎn)物的U-13C標(biāo)記率顯著降低了,顯然METTL5影響了肝癌細(xì)胞中脂質(zhì)代謝的重編程(圖4h)。
作者進(jìn)一步對(duì)長(zhǎng)鏈脂肪酸進(jìn)行LC-MS分析表明,大多數(shù)長(zhǎng)鏈脂肪酸特別是多不飽和脂肪酸隨著METTL5敲除顯著降低,對(duì)代謝物進(jìn)行富集分析發(fā)現(xiàn),這些顯著減少的多不飽和脂肪酸主要與β氧化途徑相關(guān)(圖4i-k),說(shuō)明METTL5的缺失可能會(huì)損害細(xì)胞的β氧化。
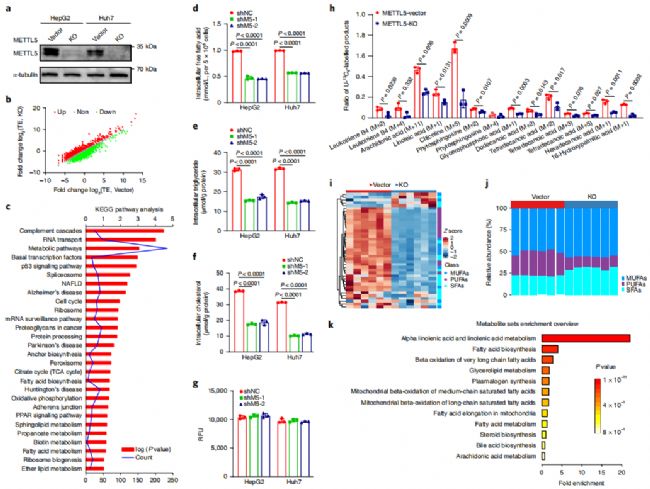
圖4. MettL5敲除損害脂肪酸β-氧化
5.ACSL4介導(dǎo)MettL5在脂肪酸代謝和肝癌進(jìn)展中的功能
為了深入探究MettL5潛在的分子機(jī)制,作者分析了靶mRNA的特征,在富含脂肪酸代謝途徑的mRNA中,酰基輔酶A合成酶長(zhǎng)鏈家族(ACSL)成員,包括ACSL1、ACSL3、ACSL4和ACSL5,在缺乏METTL5的細(xì)胞中顯示翻譯效率降低,同樣的METTL5缺乏的細(xì)胞中ACSL家族蛋白的表達(dá)水平也同步降低了(圖5f)。
ACSL家族能夠?qū)㈤L(zhǎng)鏈脂肪酸轉(zhuǎn)化脂肪酰基輔酶a酯,在癌癥的長(zhǎng)鏈脂肪代謝中起到至關(guān)重要的作用,為了分析ACSL在METTL5對(duì)HCC調(diào)控中的作用,作者在METTL5敲除的細(xì)胞中過(guò)表達(dá)的了ACSL4進(jìn)行拯救實(shí)驗(yàn)。通過(guò)強(qiáng)制過(guò)表達(dá)ACSL4增加了細(xì)胞中的脂質(zhì)水平(圖5g-j)。同時(shí)細(xì)胞的增殖、集落形成、侵襲等能力均受ACSL4 表達(dá)而得到增強(qiáng),(圖5k-q),ACSL4 的強(qiáng)制表達(dá)同樣的減少了HCC細(xì)胞的凋亡,并促進(jìn)了細(xì)胞周期的進(jìn)展(圖5r-u)。上述實(shí)驗(yàn)說(shuō)明,ACSL4的過(guò)表達(dá)可以在一定程度上挽救因MettL5缺失而受到的影響的癌癥進(jìn)展。為了研究結(jié)論的完整性,作者通過(guò)在MettL5過(guò)表達(dá)體系中敲除ACSL4,以及添加β氧化阻斷劑的方式,證實(shí)了MettL5在肝癌中的致癌作用需要依賴(lài)ACSL4對(duì)脂肪酸β-氧化的調(diào)節(jié)作用。最后作者在小鼠體內(nèi)同樣的驗(yàn)證了上述現(xiàn)象。
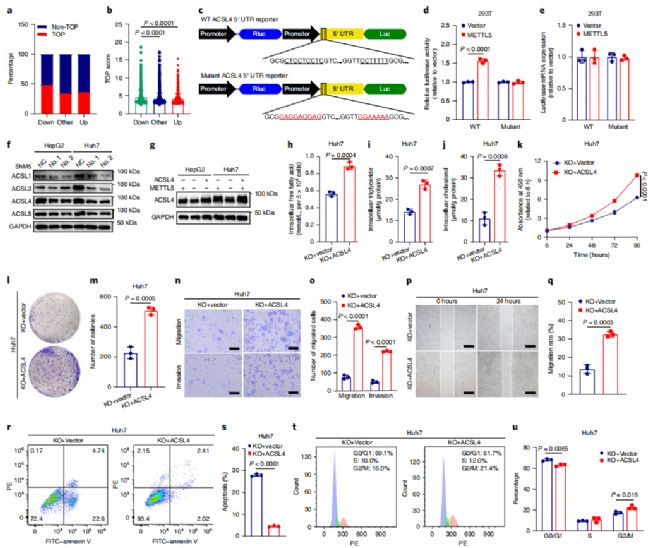
圖5. ACSL4介導(dǎo)MettL5在脂肪酸代謝和肝癌進(jìn)展中的功能
研究小結(jié)
總的來(lái)說(shuō),本研究提供了強(qiáng)有力的體外和體內(nèi)證據(jù),支持METTL5介導(dǎo)的18S rRNA m6A修飾在肝癌中的致癌作用。此外,作者還進(jìn)一步證明了rRNA表觀遺傳修飾、mRNA翻譯和脂肪酸代謝之間的交聯(lián),為在轉(zhuǎn)化水平上開(kāi)發(fā)肝癌治療的靶向治療提供了有力的證據(jù)。
科研延伸
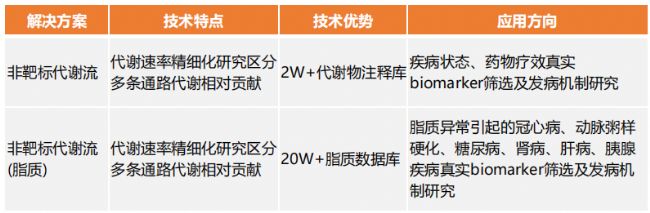
BIOTREE非靶代謝流解決方案:無(wú)偏向性的檢測(cè)所有帶同位素標(biāo)記的代謝物,廣泛篩選同位素標(biāo)記的代謝物參與的代謝途徑或基因敲除前、后代謝速率變化。
文/阿趣代謝組學(xué)
- Target-BS技術(shù)揭示糖尿病引發(fā)勃起功能障礙的DNA甲基化調(diào)控機(jī)制
- 合成生物學(xué)底盤(pán)細(xì)胞之畢赤酵母常用表達(dá)載體及基因改造技術(shù)
- 深度解析CRISPR文庫(kù)篩選流程及應(yīng)用案例
- 可溫和條件下高分辨率檢測(cè)m6A修飾的新m6A測(cè)序方法開(kāi)發(fā)研究
- AI人工智能在蛋白質(zhì)結(jié)構(gòu)預(yù)測(cè)、功能預(yù)測(cè)及設(shè)計(jì)中的作用
- m5C MeRIP-seq等揭示m5C修飾在癌癥耐藥中的關(guān)鍵調(diào)控機(jī)制中的應(yīng)用
- ChIP技術(shù)揭示NURR1在前列腺癌從基因轉(zhuǎn)錄到腫瘤進(jìn)展中的調(diào)控機(jī)制
- 兩種轉(zhuǎn)錄因子在介導(dǎo)番茄果實(shí)成熟的表觀遺傳調(diào)控中發(fā)揮的關(guān)鍵作用
- 2025伯豪生物春季全國(guó)巡講開(kāi)啟,早鳥(niǎo)報(bào)名搶占先機(jī)
- 華大智造副總裁中國(guó)區(qū)總經(jīng)理彭歡歡一行到訪(fǎng)伯豪生物
- 伯豪董事長(zhǎng)出席專(zhuān)精特新中小企業(yè)發(fā)展壯大論壇并發(fā)言
- 伯豪生物雙11狂歡特惠活動(dòng)來(lái)襲,限時(shí)限量搶
- 怡美通德推出成本價(jià)體驗(yàn)單細(xì)胞測(cè)序(FFPE或全血)
- 伯豪生物2024系列培訓(xùn)班(陜西站)報(bào)名開(kāi)啟
- 伯豪單細(xì)胞Flex年中巨惠,1.1W/樣本活動(dòng)價(jià)即將截止
- 藍(lán)景科信DAP-seq技術(shù)相關(guān)文章6連發(fā),總IF 95.2





