生物反應器在生物工程肝臟器官體外培養研究中的應用
急性和慢性肝功能衰竭肝臟移植是唯一治療方法,供體器官卻面臨持續短缺的情況。器官生物工程技術有希望利用生物反應器體外培養制造人體器官來解決這一困境。然而,該技術在臨床上的應用目前還受到功能血管網絡重建、特定功能細胞移植、細胞系培養條件不同等重重阻礙。
Functional characterization of a bioengineered liver after heterotopic implantation in pigs報告了一種將HUVECs(人臍靜脈內皮細胞)重新內皮化后,原代豬肝細胞植入生物工程肝臟(BEL)支架,利用生物反應器進行體外培養增殖器官細胞獲得生物工程肝臟的方法。
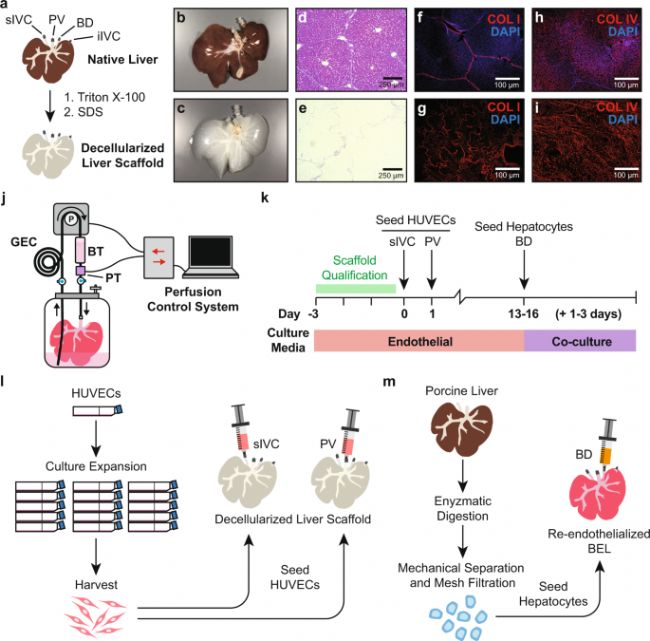
去細胞支架制備
首先,使用Triton X-100和SDS洗滌劑溶液分別灌注豬肝臟以獲得無細胞支架。組織學染色驗證去細胞化支架中完全去除細胞物質并只保留細胞外基質(ECM)蛋白膠原I和膠原IV。隨即將去細胞化的肝臟安裝在生物反應器中,并用不含抗生素的內皮培養基灌注72小時(37°C,5%二氧化碳)。
人臍靜脈內皮細胞培養與支架接種
人臍靜脈內皮細胞同樣在不含抗生素內皮細胞生長培養基中進行預處理(37°C,5%二氧化碳),隨即接種進行培養。首先靜態培養1小時,使得細胞先附著在支架上,隨后灌注補充含青霉素和鏈霉素的培養基。每天更換培養基,確保生物反應器內葡萄糖水平在24小時內保持在0.3 g/L以上。培養過程中培養基灌注壓力保持在12 mmHg。
豬肝細胞分離、培養與支架接種
新鮮豬肝臟去除殘留血液和經缺血性損傷預防性處理后,使用膠原酶和中性蛋白酶進行酶解。使用含10% FBS(胎牛血清)的Williams E溶液進行細胞分散,經過篩分離、離心富集得到肝細胞,并在2L培養基中進行高密度培養(1X106細胞/mL)。HUVEC接種至支架的13-16天后,以50 mL/min的速率利用蠕動泵將含有肝細胞的培養基灌注至反應器內。接種48h后,觀察到肝細胞在支架上呈簇狀分布。
反應器培養細胞代謝物與分泌因子分析
每天收集來自生物反應器的培養基樣品,進行離線分析確定培養基中葡萄糖,氨和乳酸脫氫酶活性的水平。測量葡萄糖濃度用于計算24小時內的消耗。使用ELISA試劑盒定量可溶性和白蛋白。
經組織學分析、氨清除動力學分析和尿素生產測定后,證實培養所得到的生物工程肝臟能夠產生白蛋白、氨解毒和尿素合成,具有肝臟器官類似的功能。實驗證實了肝細胞高密度培養的可行性,并在去細胞化肝支架中可以保持其器官功能。此外,數據顯示在支架中培養的內皮細胞在體外不會阻礙支架中肝細胞的功能。
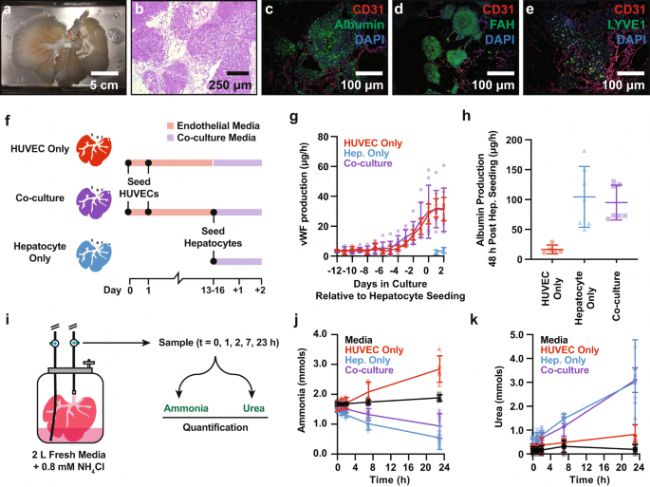
生物工程肝臟還可以用于減緩手術誘導的急性肝功能衰竭模型中氨的積累。該研究結果證實了設計生產臨床規模BEL可行性,并建立了一個優化肝臟特異性細胞接種和植入的生物培養平臺。
參考文獻:
1. Anderson, B.D., Nelson, E.D., Joo, D. et al. Functional characterization of a bioengineered liver after heterotopic implantation in pigs. Commun Biol 4, 1157 (2021). https://doi.org/10.1038/s42003-021-02665-2






