脂質體擠出器在新型納米藥物復合物中的應用
湖南大學與湘雅醫院在The Royal Society of Chemistry上聯合發表文章《A hybrid membrane coating nanodrug system against gastric cancer via the VEGFR2/STAT3 signaling pathway》。Liposome Extruder(脂質體擠出器)在文章中得到多次應用。

圖1.發表文章首頁
血管內皮生長因子(VEGF)在許多胃癌患者中是一個重要的致癌基因。越來越多的證據表明,VEGF/VEGFR2通路的異常激活不僅可以促進新血管的生成,還可以加速細胞增殖和遷移,誘發血管通透性加重,加劇腫瘤微環境缺氧和酸中毒,顯著抑制腫瘤免疫功能,多層次促進惡性發展。癌細胞中的STAT3可立即調節包括連續激活后的VEGF在內的多種癌基因的表達。VEGF可以激活STAT3以在癌細胞中產生信號前饋回路。因此,抑制VEGFR2被認為是重要的抗癌策略。
作為小分子VEGFR2抑制劑,通過特異性靶向細胞內激酶ATP結合位點以抑制磷酸化,阿帕替尼(AP)發揮了強大的抗血管生成功能。
華蟾素 (CS-1) 是具有良好抗腫瘤和抗炎活性的化合物。據研究表明,它可以通過靶向幾個重要的腫瘤信號通路來發揮抗癌作用。
紅細胞膜 (RBC)可以穩定抵抗體內納米顆粒(NPs)的清除機制以延長體循環半衰期。而癌細胞膜 (CCM)包裹的納米顆粒可以增強藥物在腫瘤部位的富集。因此,包覆了紅細胞和癌細胞雜化膜(R/C)的納米顆粒可以同時延長半衰期并提高藥物作用于腫瘤部位的靶向性。
基于AP 和 CS-1水溶性差,體內半衰期短與生物利用度低的缺陷,結合納米藥物載體的獨特優勢,文章研究了以pH響應型脂質體納米顆粒作為藥物載體共同遞送藥物AP和CS-1(LP@AC)。納米粒子進一步包覆于源自紅細胞(RBC)和癌細胞(CCM)的雜化膜(R/C),最終獲得納米藥物復合物(LP-R/C@AC NPs)。
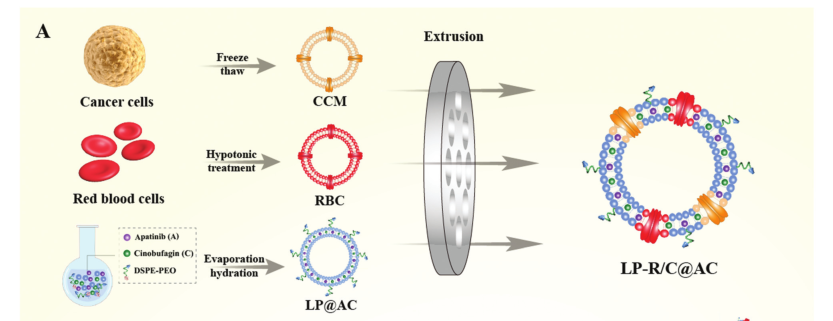
圖2. 納米藥物復合物(LP-R/C@AC NPs)制備概圖
研究結果表明,構建的納米藥物復合物(LP-R/C@AC NPs)不僅能通過誘導細胞凋亡、自噬和細胞焦亡來有效殺死腫瘤,還顯著抑制腫瘤通過 VEGFR2/STAT3 通路侵襲和轉移。
新開發的納米藥物復合物有望應用于晚期胃癌的臨床治療。

圖3. Liposome Extruder(脂質體擠出器)在文章中的應用
Liposome Extruder(脂質體擠出器)分別在雜化膜(R/C),載藥脂質體(LP@AC)與納米藥物復合物(LP-R/C@AC NPs)的制備過程中得到應用。目的均為獲得均一的顆粒。

圖4. Liposome Extruder(脂質體擠出器)
Liposome Extruder(脂質體擠出器)具有操作簡便,濾膜規格選擇多樣性等特點,其應用領域包括但不限于醫藥,化妝品等科研實驗。





