SPR與LSPR在儀器相關設計和檢測細節的區別
介紹
當涉及到用于生物傳感、環境監測、臨床診斷或闡明蛋白-蛋白相互作用的實時、無標記光學技術時,大多數研究人員通常會想到表面等離子體共振(SPR)技術。一般來說,SPR信號產生于薄金屬表面生物分子相互作用導致的局部折射率變化,因此不需要標記,數據可以實時收集。傳統的SPR已經建立了幾十年,局域表面等離子體共振 (LSPR)技術也走向了商業化。這兩種技術在儀器相關設計和檢測細節的區別將在下面進行概述。
傳統SPR的優勢
Affinite的SPR儀器的核心技術使用了Kretschmann配置,其中入射光與連接到玻璃棱鏡的薄金膜上的表面等離子體相互作用(圖1)。消逝波垂直于金屬表面傳播到周圍的樣品介質中。這些消逝波對金屬薄膜表面[1]到200-300nm范圍內的任何折射率變化都很敏感。這是SPR檢測靈敏度的關鍵,只有在這個區域內的折射率變化才會影響SPR的響應。例如,與表面受體結合的蛋白質的存在會引起表面等離子體條件的變化,從而改變SPR的響應,這在我們的儀器中是用波長測量的(可以很容易地轉換為共振單位)。
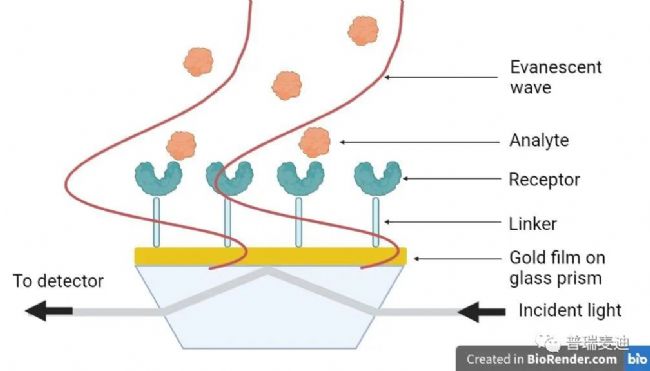
圖1所示 基于Kretschmann結構的SPR設計圖像
是什么使Affinite的儀器成為大多數應用、質量控制和檢測開發的首選平臺?
棱鏡上的金膜厚度為50nm,已被證明能提供高靈敏的測量[2]。這也是市場上大多數SPR儀器的標準和首選配置。此外,我們的SPR儀器使用波長模式,而不是角度。因此,光學組件使我們的平臺保持緊湊和穩健,并減少受到物理振動或擾動產生的噪聲的影響。最重要的是,由于這種技術的折射特性,光線不需穿透樣本,可以使用血清和血漿等復雜的基質。自從幾十年前傳統的SPR出現以來,已經有無數的文獻對金表面鈍化以減少非特異性吸附進行了研究。Affinite同時也優化了一種名為Afficoat的獨特試劑,可以降低生物樣本與芯片表面的非特異結合。最重要的是,由于我們易于使用的SPR平臺、直觀的軟件和創新的KNX2泵模塊,獲得感興趣的生物分子相互作用的動力學和親和力信息非常簡單。
傳統SPR在生物傳感、分析開發和其他應用方面的主要優勢
*最少的樣品準備
*對表面的結合作用引起的表面折射率變化具有高靈敏度
*在表面化學、分析開發、親和力和動力學測定和應用方面有許多文獻參考
*可用于復雜的樣品,如臨床樣本
局域表面等離子體共振技術LSPR呢?
LSPR使用的不是金屬薄膜,而是圓形的納米顆粒以及其他形狀的納米顆粒,比如直徑通常小于100nm的納米圓盤、納米棒和納米三角形[3],它們要么用于溶液中,要么固定在透明的基底上。對于固定的LSPR, SPR信號依賴于介質的局部折射率。當入射光激發納米顆粒時,表面等離子體激元(或自由電子振蕩)被限制在納米顆粒的邊界內(圖2)。LSPR采用透射模式,峰值吸收波長的偏移將對應于納米顆粒表面局部折射率的變化。
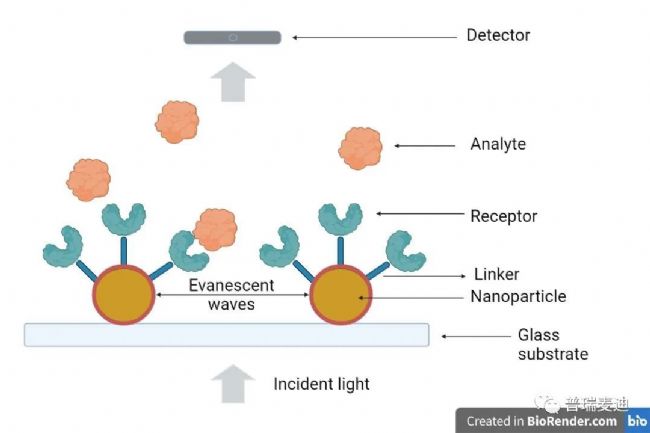
圖2 局域表面等離子體共振技術LSPR光路示意圖
雖然LSPR看起來是一個更簡單的過程,但在信號重復性、靈敏度和信噪比方面面臨一系列問題。由于LSPR等離子體激元峰增寬,傳感器性能等問題,檢測時可能會發生結果重復性低的問題。這可能與納米顆粒的輻射阻尼,以及這些納米顆粒的尺寸、形狀、表面粗糙度和材料不均勻性的組合有關[4,5]。如果納米顆粒表面與聚集體不一致,則固定蛋白的密度可能會發生變化,這會影響靈敏度。此外,LSPR實驗的噪聲也高于傳統的SPR[7,8]。當低濃度的分析物被檢測時可能會遇到信噪比問題。眾所周知,隨著實驗的進行,納米顆粒的量會相應減少[7,9]。
雖然自21世紀初[6]以來,關于LSPR的文獻數量開始增加,但在納米粒子表面化學的優化方面仍有差距。而納米顆粒的非特異性結合一直是一個難以克服的問題[6,9]。當涉及臨床樣本這樣的復雜基質時,尤其如此[9]。
結論
傳統的SPR和LSPR通過不同的光路設計提供信號。然而,平面金屬薄膜的表面化學性質更加穩定,而且SPR信號不像LSPR那樣嚴重依賴于納米顆粒的性能和質量。納米顆粒的表面化學必須精細控制,其性能才得以保障。進一步探索LSPR現象和其應用依然需要一個過程。
總之,傳統的SPR工具,如Affinite instruments提供:
*金薄膜的均勻性,檢測重復性好
*基于波長檢測的儀器設計,運行穩定
*對于復雜的生物樣品,亦能提供優良的檢測效果
*完善的表面修飾策略,臨床應用的案例,以及著名的期刊文獻
考慮到以上所有觀點,Affinite的SPR儀器基于傳統的SPR技術設計,因為它是一種更可靠的方法,可以為研究人員提供高質量的數據,沒有任何不確定性。
Affinite優勢
✓Affinite Instruments的P4SPR、qSPR是一種非常友好的檢測儀器。
✓與傳統的ELISA免疫分析相比,Affinite Instruments的SPR儀器提供快速、實時的親和力和動力學數據。
✓簡單----輕松易學,快速取得試驗結果。
✓多功能性----生物制藥,生物傳感,分析方法開發及應用。
✓經濟----實惠,方便。
Affinite Instruments公司的SPR儀器使用性價比高,實驗耗材傳感芯片價格友好,是一款真正普通實驗室即可買得起用得起的互作檢測儀器,同時免于維護的負擔。
文獻參考
[1] Maxime Couture, Ludovic S. Live, Anuj Dhawan and Jean-Francois Masson. EOT or Kretschmann configuration? Comparative study of the plasmonic modes in gold nanohole arrays. Analyst, 2012, 137, 4162.
[2] Gwon, H.R.; Lee, S.H. Spectral and angular responses of surface plasmon resonance based on the Kretschmann prism configuration. Mater. Trans. 2010, 51, 1150–1155.
[3] Amanda J. Haes, Richard P. Van Duyne. A unified view of propagating and localized surface plasmon resonance biosensors. Anal Bioanal Chem, 2004, 379, 920–930.
[4] Mikael Svedendahl, Si Chen, Alexandre Dmitriev, and Mikael Kall. Refractometric Sensing Using Propagating versus Localized Surface Plasmons: A Direct Comparison. Nano Lett., 9, 2009, 4428-4433.
[5] K, Takemura. Surface Plasmon Resonance (SPR)- and Localized SPR (LSPR)-Based Virus Sensing Systems: Optical Vibration of Nano- and Micro-Metallic Materials for the Development of Next-Generation Virus Detection Technology. Biosensors, 2021, 11, 250.
[6] M.-Carmen Estevez, Marinus A. Otte, Borja Sepulveda, Laura M. Lechuga. Trends and challenges of refractometric nanoplasmonic biosensors: A review. Anal. Chim. Acta, 2014, 806, 55–73.
[7] Jacqueline Jatschka, André Dathe, Andrea Csáki, Wolfgang Fritzsche, Ondrej Stranik. Propagating and localized surface plasmon resonance sensing — A critical comparison based on measurements and theory. Sens. Bio-Sens. Res., 2016, 7 62–70.
[8] Chanda Ranjit Yonzon, Eunhee Jeoung, Shengli Zou, George C. Schatz, Milan Mrksich, and Richard P. Van Duyne. A Comparative Analysis of Localized and Propagating Surface Plasmon Resonance Sensors: The Binding of Concanavalin A to a Monosaccharide Functionalized Self-Assembled Monolayer. J. Am. Chem. Soc., 2004, 126, 12669-12676.
[9] Andreas Dahlin. Biochemical Sensing with Nanoplasmonic Architectures: We Know How but Do We Know Why? Annu. Rev. Anal. Chem., 2021, 14, 281–9.





