單細胞多組學揭示非小細胞肺癌ICI治療反應的預測性生物標志物
近年來,雖然癌癥免疫療法進展驚人,但如何準確預測針對患者特定腫瘤的治療方法依舊是一個挑戰。當前數據表明只有不到一半的癌癥患者會對免疫治療產生反應。此外,考慮到該療法的潛在危險副作用,對最佳患者候選人的選擇也尤為重要。
本期推送為大家帶來一項來自紐約西奈山伊坎醫學院的研究,該研究可能為非小細胞肺癌 (NSCLC) 的免疫檢查點治療反應提供新的預測性生物標志物。這些發現可以通過根據腫瘤的免疫成分更精確地對患者進行分層,與其他腫瘤特征(例如腫瘤突變負擔)協調工作,從而幫助更好地為治療決策提供信息。
// 免疫治療反應的生物標記物
腫瘤學家為了做出這種治療決策會使用一些不同的參數。單一生物標志物測試可用于評估癌細胞表面PD-L1的表達水平,從而了解抗PD-1/PD-L1藥物臨床獲益的可能性。免疫治療效果的另一個生物標志物被稱為腫瘤突變負荷 (TMB),即癌細胞中突變數量的讀數。當觀察到高TMB時,假設這些癌細胞更有可能產生被患者免疫系統識別為外來物質的蛋白質,從而使癌癥更容易受到免疫檢查點抑制劑 (ICI) 療法增強的免疫反應的影響。然而,TMB作為一種獨立的生物標志物仍存在爭議,因為TMB可能因癌癥類型而異,所以需要一致的疾病特異性標準來準確量化腫瘤的TMB是高還是低。
此外,越來越多的臨床研究顯示,在確定免疫治療的反應時,綜合考慮多種生物標志物可能是十分必要的。一項在轉移性尿路上皮癌患者中使用阿特殊單抗(一種治療性抗PD-L1抗體)的II期試驗結果表明,生物標志物如PD-L1表達和TMB等提供了腫瘤對治療反應的獨立和互補的信息[1]。這暗示了想要更好地預測患者的反應需要結合多種標記物進行評估。當前需要找到新的腫瘤生物標志物,與TMB或PD-L1結合,從而為改善腫瘤分類并為免疫治療的關鍵決策過程提供信息。
// 非小細胞肺癌免疫人群的定義
腫瘤生物學中一種相對未探索的關系是腫瘤的免疫成分與隨后對免疫治療的反應之間的關系。盡管T細胞浸潤是一種普遍陽性反應的新興標志,但尚不清楚治療前的腫瘤免疫微環境如何驅動這種反應,以及哪些特定的免疫細胞群或細胞狀態可能是對ICI治療反應的預測因子。此外,在腫瘤學家尋求免疫治療的基礎上,有必要了解這些免疫特征與腫瘤突變負擔之間的聯系。它們是免疫治療反應的冗余參數,還是作為補充的預測性生物標志物?
來自紐約西奈山伊坎醫學院的科學家進行了一項研究,以在非小細胞肺癌 (NSCLC) 中探索上述問題的真相[2]。為了研究NSCLC中免疫細胞的組成和分子狀態,該研究聚焦于單細胞RNA測序 (scRNA-seq),通過CITE-seq和T細胞受體測序 (TCR-seq)進行表面蛋白分析和免疫組庫分析。對27個未經處理的匹配患者樣本進行了scRNA-seq,包括癌癥和非癌癥的肺組織。還通過CITE-seq對8個患者匹配的樣本進行了多組學分析,然后對3個患者匹配的樣本進行了組合scRNA-seq和TCR-seq。共計分析來自35個腫瘤的361,929個單細胞,這是迄今為止最大的早期肺癌免疫反應單細胞圖譜。
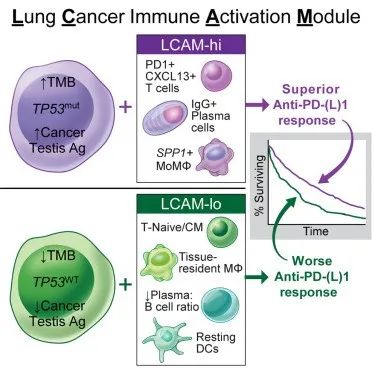 所有腫瘤的譜系歸一化單細胞數據揭示了6大類細胞中的49個免疫簇:T細胞、B細胞、漿細胞、肥大細胞、漿細胞樣樹突狀細胞和單核吞噬細胞。結合scRNA-seq和表面蛋白數據揭示了T細胞的多樣化組合,解析了CD4+和CD8+T細胞簇內獨特的種群和活動狀態。其中一個被稱為Tactivated的簇富含IFNG、GZMB、LAG3、CXCL13和HAVCR2轉錄本,并增加了PD-1、ICOS和CD39蛋白表達,這其中一些與ICI治療的潛在機制直接相關。這組Tactivated細胞連同調節性T細胞 (Treg) 是在一組被研究者稱為Tcycle的T細胞群中最為普遍的。Tcycle是一種共享循環狀態的多種T細胞表型的混合物,其特征是細胞循環基因MKI67和STMN1的表達,以及表面蛋白HLA-DR和CD38的表達。
所有腫瘤的譜系歸一化單細胞數據揭示了6大類細胞中的49個免疫簇:T細胞、B細胞、漿細胞、肥大細胞、漿細胞樣樹突狀細胞和單核吞噬細胞。結合scRNA-seq和表面蛋白數據揭示了T細胞的多樣化組合,解析了CD4+和CD8+T細胞簇內獨特的種群和活動狀態。其中一個被稱為Tactivated的簇富含IFNG、GZMB、LAG3、CXCL13和HAVCR2轉錄本,并增加了PD-1、ICOS和CD39蛋白表達,這其中一些與ICI治療的潛在機制直接相關。這組Tactivated細胞連同調節性T細胞 (Treg) 是在一組被研究者稱為Tcycle的T細胞群中最為普遍的。Tcycle是一種共享循環狀態的多種T細胞表型的混合物,其特征是細胞循環基因MKI67和STMN1的表達,以及表面蛋白HLA-DR和CD38的表達。
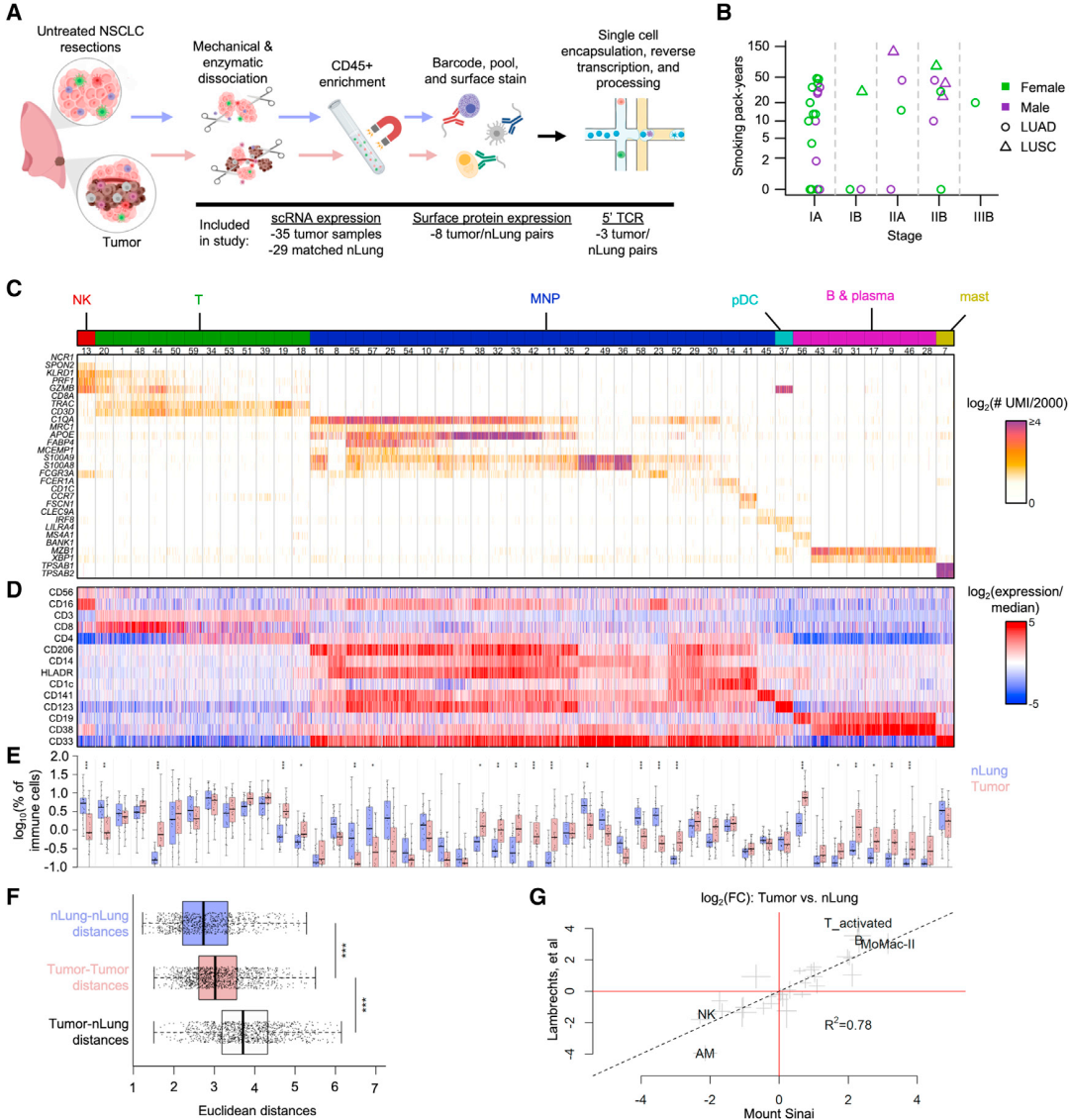
scRNA-seq和CITE-seq建立了腫瘤微環境中轉錄狀態的多樣性
// 腫瘤免疫激活的一種新的細胞特征
通過對未經治療的腫瘤微環境的免疫成分的詳細了解,研究人員注意到腫瘤中某些免疫群體之間細胞類型頻率的相關性。在Tactivated細胞、IgG+漿細胞和其他單核細胞群之間觀察到高度相關性,它們共同形成了肺癌激活模塊 (LCAMhi)。在B細胞、TCentral Memory (CM)/naive-like-II和樹突狀細胞等之間觀察到了反相關,這些細胞組成了LCAMlo細胞特征,并且類似于在非癌癥的肺組織中看到的免疫成分。重要的是,根據這些模塊中代表的細胞類型的平均值對患者進行了很好的分層,這表明不同的細胞特征可能代表了對患者多樣性的新參數。
為了探索LCAM評分更廣泛的潛在意義,研究小組使用代表LCAMhi和LCAMlo模塊中細胞類型的特定基因特征,對癌癥基因組圖譜中記錄的512例肺腺癌的大量轉錄組數據進行了重新評分。這些分數與已發表的總免疫含量數據相關。對大量數據的回顧性分析還表明,記錄的腫瘤突變負荷也與相應肺腫瘤的LCAM評分相關,量化突變癌癥新抗原表達的評分也是如此。這些相關性表明,LCAM細胞模塊反映了對突變腫瘤抗原的適應性免疫反應,該反應與總免疫浸潤無關。
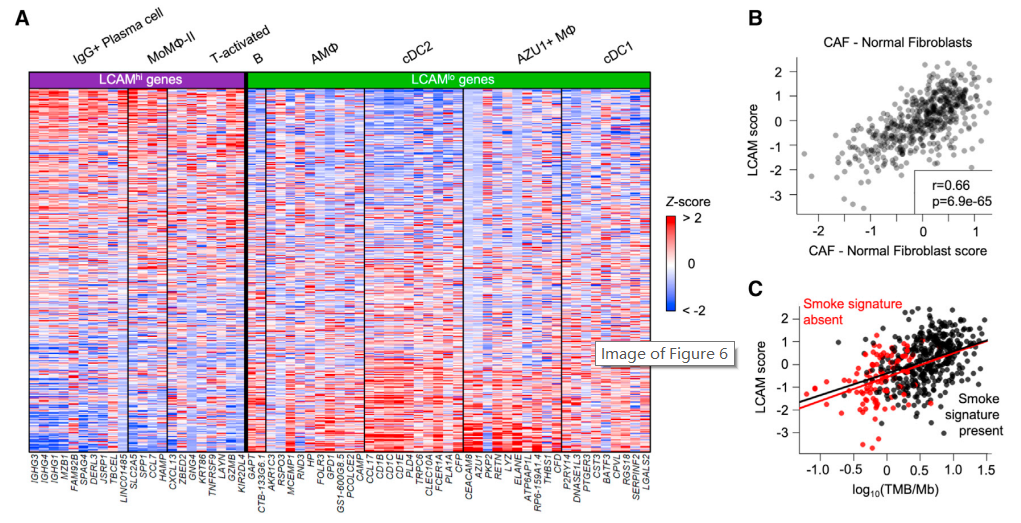
與LCAM免疫反應相關的腫瘤特征
臨床數據進一步鞏固了LCAM評分作為免疫治療反應指標的潛在意義。研究分析了2016年NSCLC患者接受阿特殊單抗或化療治療的臨床試驗結果,發現LCAM評分和TMB與接受治療的患者的無進展生存期改善相關。這一生存益處的證據,連同構成肺癌激活模塊的活性免疫細胞的質量,可能表明LCAMhi患者經歷了更強的抗原特異性抗腫瘤適應性免疫反應。這也將LCAM定位為免疫治療對檢查點封鎖反應的可行補充預測生物標志物。
// 單細胞多組學分析改善免疫治療預測
研究通過對腫瘤微環境細胞組成的單細胞多組學圖譜進行分析,能夠識別與免疫激活相關的特定細胞和分子特征,可以在更大范圍內進一步測試和確認腫瘤隊列。有了LCAM生物標志物,以及揭示其他未發現的預測性生物標志物的工具,我們有望開始了解決定免疫治療反應的所有多維腫瘤免疫特征。
參考文獻:
[1] Decoding the signs of response to cancerimmunotherapy. Nature Research Custom Media and Illumina.
[2] Leader AM, Grout JA, Maier BB, et al. Single-cellanalysis of human non-small cell lung cancer lesions refines tumorclassification and patient stratification. Cancer Cell.2021;39(12):1594-1609.e12. doi:10.1016/j.ccell.2021.10.009





