ЙъОп·ҙ‘ӘЖчФЪ»щУЪјҡ°ыЖ¬өДЙъОп№ӨіМЯMРРРДјЎјҡ°ы‘ТёЎЕарBјјРgЙПөД‘ӘУГ
ЙъОп№ӨіМөД№ҰДЬРФРДЕKҪMҝ—УРНыҙЩЯMКЬ“pРДЕKҪMҝ—өДРЮҸНЎЈСРҫҝХЯФшК№УГЙъОп·ҙ‘ӘЖчНЁЯ^РЎКуЕЯМҘёЙ (mES) јҡ°ыСЬЙъөДРДјЎјҡ°ый_°lБЛРДЕKјҡ°ыЖ¬Ј¬Я@КЗТ»·NҸД ES јҡ°ы®aЙъЯm®””өБҝөДРДјЎјҡ°ыөДПөҪyЈ¬Ждқ“ФЪҷCЦЖИФИ»лyТФЧҪГюЎЈ
ФЪСРҫҝҢҚтһЦРЈ¬СРҫҝХЯК№УГИэҫSЙъОп·ҙ‘ӘЖчНЁЯ^ЕЯ оуwРОіЙҪЁБўБЛҫЯУРЯmәПmESјҡ°ы”UФцәНРДЕK·Ц»Ҝ—lјюөДЕарBПөҪyЎЈГҝИХіЈТҺЕарB»щёь“QОҙДЬ·АЦ№ЕарB»щЦРИйЛб·eАЫәН pH ЦөҪөөНЈ¬ҸД¶шҢ§ЦВјҡ°ы”UФцәНРДЕK·Ц»ҜІ»ЧгЎЈ·ҙЯ^ҒнЈ¬ЯBАm№аЧўПөҪyұЈіЦБЛИйЛбқв¶ИәН pH ЦөөД·Җ¶ЁРФЈ¬ІўК№јҡ°ы”өБҝФцјУБЛ¶аЯ_ 300 ұ¶өДҪУ·Nјҡ°ы”өБҝЈ¬ІўФЪ·Ц»Ҝ 10 МмәуҙЩЯMБЛРДЕK·Ц»ҜЎЈҪӣЯ^ 8 МмөДЕарBәНјғ»ҜІҪуEЈ¬ҙујs 1×10ФЪ 1-L ЙъОп·ҙ‘ӘЖчЕарBОпЦРКХјҜБЛ8ӮҖРДјЎјҡ°ыЈ¬ІўУГо^ө°°ЧәНБЈјҡ°ыјҜВдҙМјӨТтЧУЯMРРо~НвМҺАнЈ¬К№РДјЎјҡ°ы”өБҝФцјУөҪјs 5.5×10 8ЎЈmES јҡ°ыСЬЙъөДРДјЎјҡ°ыЕcЯm®””өБҝөДФӯҙъЕарBіЙАwҫSјҡ°ыФЪңШ¶Ин‘‘ӘЕарBГуЙП№ІЕарBЈ¬ДЬүтРОіЙРДЕKјҡ°ыЖ¬ІўРОіЙ·ЦҢУЦВГЬөДРДЕKҪMҝ—ЎЈЯ@Р©°l¬FұнГчЈ¬Я@·NҫЯУРЯm®”ЕарB»щөДЙъОп·ҙ‘ӘЖчПөҪyҝЙДЬДЬүтһй»щУЪјҡ°ыЖ¬өДРДЕKҪMҝ—ЦЖӮдРДјЎјҡ°ыЎЈ

ФЪҝмЛЩ°lХ№өДФЩЙъбtҢWоIУтЦРЈ¬»щУЪјҡ°ыөДҜҹ·ЁТСіЙһйРДЕKТЖЦІЦОҜҹКЬ“pРДЕKҪMҝ—өДУРПЈНыөДМжҙъ·Ҫ°ёЎЈСРҫҝХЯЦ®З°й_°lБЛТ»·NФӯКјөДҹoЦ§јЬҪMҝ—№ӨіМјјРgЈ¬·Qһй“»щУЪјҡ°ыЖ¬өДҪMҝ—№ӨіМ”Ј¬К№УГЕcңШ¶Ин‘‘ӘРФҫЫәПОпҫЫЈЁ N-®җұы»щұыП©хЈ°·Ј©№ІғrҪYәПөДңШ¶Ин‘‘ӘРФЕарBГуЎЈҪөөНЕарBңШ¶ИҝЙҙЩЯMұнГжҸДКиЛ®РФҝмЛЩЮDЧғһйУHЛ®РФЈ¬Я@К№СРҫҝХЯДЬүтКХјҜҝЙРРөДҶОҢУјҡ°ыЖ¬Ј¬ІўНкИ«ұЈҙжјҡ°ы-јҡ°ыҪУУ|әНјҡ°ыНв»щЩ|. ФS¶аСРҫҝҲуөАЈ¬К№УГёч·NоҗРНөДјҡ°ыЯMРР»щУЪјҡ°ыЖ¬өДТЖЦІҝЙТФёДЙЖКЬ“pРДЕKөДРДЕK№ҰДЬЎЈИ»¶шЈ¬ЧоҪьөДЧC“юұнГчЈ¬ҒнЧФТЖЦІјҡ°ыөД·ЦГЪТтЧУҪйҢ§өДЕФ·ЦГЪЧчУГЎўСӘ№ЬЙъіЙәНРДЕKұЈЧoҝЙДЬКЗјҡ°ыТЖЦІҪйҢ§өДРДЕK№ҰДЬёДЙЖөДЦчТӘҷCЦЖЎЈКВҢҚЙПЈ¬Я@Р©У°н‘ҝЙДЬКЗ„“ФмҝЙТЖЦІөДЙъОп№ӨіМФцәсРДЕKҪMҝ—өДПИӣQ—lјюЈ¬ЦұҪУҢ§ЦВКХҝsЎЈ
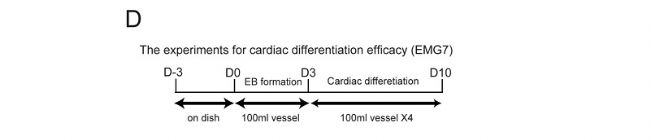
„“ҪЁЙъОп№ӨіМРДЕKҪMҝ—ТЖЦІОпөД·Ҫ·ЁТСҪӣҪЁБўБЛ”өК®ДкЈ¬СРҫҝХЯЦ®З°ФшҲуөАЈ¬ҢўИэҢУРВЙъҙуКуРДЕKТЖЦІОпЦШҸНТЖЦІөҪуwғИЖӨПВҪMҝ—ЙПЈ¬ҝЙТФ®aЙъјs 1 әБГЧәсөДРДЕKҪMҝ—ЎЈИ»¶шЈ¬ІёИй„УОпРДјЎјҡ°ыФЪіцЙъәуІ»ҫГҫНК§ИҘБЛФцЦіДЬБҰЈ»ТтҙЛЈ¬ЕЯМҘёЙјҡ°ыЈЁESЈ©әНХTҢ§¶аДЬёЙјҡ°ыЈЁiPSЈ©өИ¶аДЬёЙјҡ°ыКЗУРЗ°НҫөДРДјЎјҡ°ыҒнФҙЎЈ
ТСҪӣй_°lБЛёч·N·Ҫ·ЁУГУЪ ES әН iPS јҡ°ыөД”UФцәНРДЕK·Ц»ҜЈ¬ЕЯ оуwЈЁEBЈ©‘ТёЎЕарBТСұ»ҸV·әУГЧчТ»·NТЧУЪ”UХ№өД·Ҫ·ЁЎЈZandstra өИИЛҲуөАБЛК№УГЮDЖҝЕарBУГУЪРДјЎјҡ°ыЙъ®aөДРЎКу ES (mES) јҡ°ыөДҝЙ”UХ№ЕарB Ј¬Wang өИИЛҲуөАБЛК№УГРэЮDјҡ°ыЕарBПөҪyЯMРРРДјЎ·Ц»ҜөД mES ЕарBЎЈСРҫҝХЯҲуөАБЛ mES јҡ°ыФЪЮDЖҝЦРФцЦіІў·Ц»ҜһйРДјЎјҡ°ыЈ¬ІўЗТФҙЧФ mES јҡ°ыөДРДјЎјҡ°ыЖ¬ҫЯУРФЪјҡ°ыЖ¬ЙПӮчІҘөДлҠЙъАн№ҰДЬ . И»¶шЈ¬®”mESјҡ°ыФЪЮDЖҝЦРЕарB•rЈ¬лSЦшјҡ°ыФцЦіЈ¬јҡ°ыЕарB—lјюлyТФ·Җ¶ЁҫSіЦЈ¬Я@ҝЙДЬ•юУ°н‘јҡ°ыөДЙъйLЎў·Ц»ҜәН»оБҰЎЈЧоҪьөДҲуёжұнГчЈ¬ҫЯУРСхҡвҝШЦЖәНЧФ„УМоідәНійИЎЕарB»щёь“QөД ЙъОп·ҙ‘ӘЖчПөҪyҝЙТФМбёЯРДјЎјҡ°ыөД®aБҝЎЈИ»¶шЈ¬ЙРІ»ЗеіюҒнЧФЙъОп·ҙ‘ӘЖчПөҪyөДРДјЎјҡ°ыКЗ·сЯmәПЦЖФмРДЕKјҡ°ыЖ¬ЎЈ
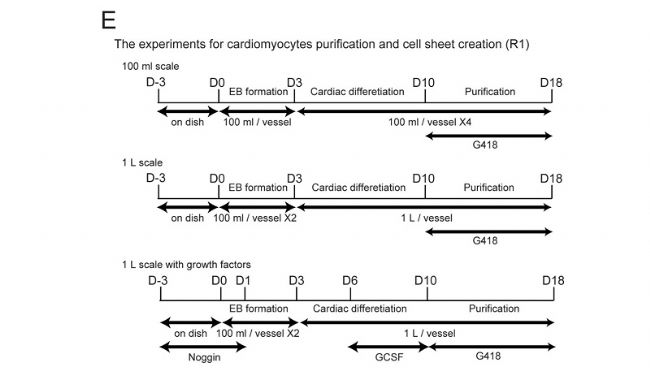
ФЪұҫСРҫҝЦРЈ¬СРҫҝХЯК№УГ»щУЪИэҫSЙъОп·ҙ‘ӘЖчөД‘ТёЎЕарBПөҪy„“ҪЁБЛ·ЦҢУөДРДЕKјҡ°ыЖ¬Ј¬УГУЪ”UФц mES јҡ°ыәНРДјЎјҡ°ыЎЈ
ФЪСРҫҝҢҚтһЦРЈ¬СРҫҝХЯК№УГИэҫSЙъОп·ҙ‘ӘЖчНЁЯ^ЕЯ оуwРОіЙҪЁБўБЛҫЯУРЯmәПmESјҡ°ы”UФцәНРДЕK·Ц»Ҝ—lјюөДЕарBПөҪyЎЈГҝИХіЈТҺЕарB»щёь“QОҙДЬ·АЦ№ЕарB»щЦРИйЛб·eАЫәН pH ЦөҪөөНЈ¬ҸД¶шҢ§ЦВјҡ°ы”UФцәНРДЕK·Ц»ҜІ»ЧгЎЈ·ҙЯ^ҒнЈ¬ЯBАm№аЧўПөҪyұЈіЦБЛИйЛбқв¶ИәН pH ЦөөД·Җ¶ЁРФЈ¬ІўК№јҡ°ы”өБҝФцјУБЛ¶аЯ_ 300 ұ¶өДҪУ·Nјҡ°ы”өБҝЈ¬ІўФЪ·Ц»Ҝ 10 МмәуҙЩЯMБЛРДЕK·Ц»ҜЎЈҪӣЯ^ 8 МмөДЕарBәНјғ»ҜІҪуEЈ¬ҙујs 1×10ФЪ 1-L ЙъОп·ҙ‘ӘЖчЕарBОпЦРКХјҜБЛ8ӮҖРДјЎјҡ°ыЈ¬ІўУГо^ө°°ЧәНБЈјҡ°ыјҜВдҙМјӨТтЧУЯMРРо~НвМҺАнЈ¬К№РДјЎјҡ°ы”өБҝФцјУөҪјs 5.5×10 8ЎЈmES јҡ°ыСЬЙъөДРДјЎјҡ°ыЕcЯm®””өБҝөДФӯҙъЕарBіЙАwҫSјҡ°ыФЪңШ¶Ин‘‘ӘЕарBГуЙП№ІЕарBЈ¬ДЬүтРОіЙРДЕKјҡ°ыЖ¬ІўРОіЙ·ЦҢУЦВГЬөДРДЕKҪMҝ—ЎЈЯ@Р©°l¬FұнГчЈ¬Я@·NҫЯУРЯm®”ЕарB»щөДЙъОп·ҙ‘ӘЖчПөҪyҝЙДЬДЬүтһй»щУЪјҡ°ыЖ¬өДРДЕKҪMҝ—ЦЖӮдРДјЎјҡ°ыЎЈ

ФЪҝмЛЩ°lХ№өДФЩЙъбtҢWоIУтЦРЈ¬»щУЪјҡ°ыөДҜҹ·ЁТСіЙһйРДЕKТЖЦІЦОҜҹКЬ“pРДЕKҪMҝ—өДУРПЈНыөДМжҙъ·Ҫ°ёЎЈСРҫҝХЯЦ®З°й_°lБЛТ»·NФӯКјөДҹoЦ§јЬҪMҝ—№ӨіМјјРgЈ¬·Qһй“»щУЪјҡ°ыЖ¬өДҪMҝ—№ӨіМ”Ј¬К№УГЕcңШ¶Ин‘‘ӘРФҫЫәПОпҫЫЈЁ N-®җұы»щұыП©хЈ°·Ј©№ІғrҪYәПөДңШ¶Ин‘‘ӘРФЕарBГуЎЈҪөөНЕарBңШ¶ИҝЙҙЩЯMұнГжҸДКиЛ®РФҝмЛЩЮDЧғһйУHЛ®РФЈ¬Я@К№СРҫҝХЯДЬүтКХјҜҝЙРРөДҶОҢУјҡ°ыЖ¬Ј¬ІўНкИ«ұЈҙжјҡ°ы-јҡ°ыҪУУ|әНјҡ°ыНв»щЩ|. ФS¶аСРҫҝҲуөАЈ¬К№УГёч·NоҗРНөДјҡ°ыЯMРР»щУЪјҡ°ыЖ¬өДТЖЦІҝЙТФёДЙЖКЬ“pРДЕKөДРДЕK№ҰДЬЎЈИ»¶шЈ¬ЧоҪьөДЧC“юұнГчЈ¬ҒнЧФТЖЦІјҡ°ыөД·ЦГЪТтЧУҪйҢ§өДЕФ·ЦГЪЧчУГЎўСӘ№ЬЙъіЙәНРДЕKұЈЧoҝЙДЬКЗјҡ°ыТЖЦІҪйҢ§өДРДЕK№ҰДЬёДЙЖөДЦчТӘҷCЦЖЎЈКВҢҚЙПЈ¬Я@Р©У°н‘ҝЙДЬКЗ„“ФмҝЙТЖЦІөДЙъОп№ӨіМФцәсРДЕKҪMҝ—өДПИӣQ—lјюЈ¬ЦұҪУҢ§ЦВКХҝsЎЈ

„“ҪЁЙъОп№ӨіМРДЕKҪMҝ—ТЖЦІОпөД·Ҫ·ЁТСҪӣҪЁБўБЛ”өК®ДкЈ¬СРҫҝХЯЦ®З°ФшҲуөАЈ¬ҢўИэҢУРВЙъҙуКуРДЕKТЖЦІОпЦШҸНТЖЦІөҪуwғИЖӨПВҪMҝ—ЙПЈ¬ҝЙТФ®aЙъјs 1 әБГЧәсөДРДЕKҪMҝ—ЎЈИ»¶шЈ¬ІёИй„УОпРДјЎјҡ°ыФЪіцЙъәуІ»ҫГҫНК§ИҘБЛФцЦіДЬБҰЈ»ТтҙЛЈ¬ЕЯМҘёЙјҡ°ыЈЁESЈ©әНХTҢ§¶аДЬёЙјҡ°ыЈЁiPSЈ©өИ¶аДЬёЙјҡ°ыКЗУРЗ°НҫөДРДјЎјҡ°ыҒнФҙЎЈ
ТСҪӣй_°lБЛёч·N·Ҫ·ЁУГУЪ ES әН iPS јҡ°ыөД”UФцәНРДЕK·Ц»ҜЈ¬ЕЯ оуwЈЁEBЈ©‘ТёЎЕарBТСұ»ҸV·әУГЧчТ»·NТЧУЪ”UХ№өД·Ҫ·ЁЎЈZandstra өИИЛҲуөАБЛК№УГЮDЖҝЕарBУГУЪРДјЎјҡ°ыЙъ®aөДРЎКу ES (mES) јҡ°ыөДҝЙ”UХ№ЕарB Ј¬Wang өИИЛҲуөАБЛК№УГРэЮDјҡ°ыЕарBПөҪyЯMРРРДјЎ·Ц»ҜөД mES ЕарBЎЈСРҫҝХЯҲуөАБЛ mES јҡ°ыФЪЮDЖҝЦРФцЦіІў·Ц»ҜһйРДјЎјҡ°ыЈ¬ІўЗТФҙЧФ mES јҡ°ыөДРДјЎјҡ°ыЖ¬ҫЯУРФЪјҡ°ыЖ¬ЙПӮчІҘөДлҠЙъАн№ҰДЬ . И»¶шЈ¬®”mESјҡ°ыФЪЮDЖҝЦРЕарB•rЈ¬лSЦшјҡ°ыФцЦіЈ¬јҡ°ыЕарB—lјюлyТФ·Җ¶ЁҫSіЦЈ¬Я@ҝЙДЬ•юУ°н‘јҡ°ыөДЙъйLЎў·Ц»ҜәН»оБҰЎЈЧоҪьөДҲуёжұнГчЈ¬ҫЯУРСхҡвҝШЦЖәНЧФ„УМоідәНійИЎЕарB»щёь“QөД ЙъОп·ҙ‘ӘЖчПөҪyҝЙТФМбёЯРДјЎјҡ°ыөД®aБҝЎЈИ»¶шЈ¬ЙРІ»ЗеіюҒнЧФЙъОп·ҙ‘ӘЖчПөҪyөДРДјЎјҡ°ыКЗ·сЯmәПЦЖФмРДЕKјҡ°ыЖ¬ЎЈ

ФЪұҫСРҫҝЦРЈ¬СРҫҝХЯК№УГ»щУЪИэҫSЙъОп·ҙ‘ӘЖчөД‘ТёЎЕарBПөҪy„“ҪЁБЛ·ЦҢУөДРДЕKјҡ°ыЖ¬Ј¬УГУЪ”UФц mES јҡ°ыәНРДјЎјҡ°ыЎЈ
ҳЛәһЈә
‘ТёЎЕарB
- ЙъОп·ҙ‘ӘЖчЦъБҰ7.6ұ¶®aБҝМбЙэөДОrЗаЛШЙъ®a№ӨЛҮҝмЛЩғһ»Ҝ
- јҡ°ыЕарBОўЭdуwЈәІ»Н¬ІДБПөДғһИұьcј°‘ӘУГЦёДП
- ЙъОпЦЖЛҺРРҳIЦР№ӨЛҮЮDТЖ»щұҫФӯ„tј°кPЧўЦШьc
- І»Н¬јҡ°ыЕарBҸҠ»Ҝ№ӨЛҮөДЙъОп·ҙ‘ӘЖчЙъ®aВКәНЕарB»щіЙұҫұИЭ^
- ЙъОп·ҙ‘ӘЖчЦъБҰӮчҪyЕарBПтҸҠ»Ҝ№ӨЛҮөДөьҙъЮDРН
- ОўЭdуwөДФӯАнЕc·Цоҗ
- ФәКҝҪвЧxСлТ•јoдӣЖ¬Ў¶ПтРВіц°lЎ·ЙъОпЦЖФм®aҳI¬F ој°З°ҫ°
- ОўЦШБҰјҡ°ыЕарBФOӮдҫCКцЈәғxЖчЯxРНЎўК№УГЎўІЩЧчЕcҫSРЮ
- °¬ШҗМ©”yЙъОп·ҙ‘ӘЖчөИББПаөЪ¶юК®ЛДҢГЙъОпЦЖЖ·ҙу•ю
- CytivaЛјНШ·І:“P·«УӢ„қ-ЧЯИл¶ҰҝөЙъОп»о„УҲAқMЕeРР
- DHSЈЁ¶Ұк»ФҙЈ©Х\СыДъ…ўјУөЪ24ҢГЦРҮшЙъОпЦЖЖ·ҙу•ю
- °¬ШҗМ©Х\Ңў”yЙъОп·ҙ‘ӘЖчөИ…ўјУЦРҮшЙъОпЦЖЖ·ҙу•ю
- °¬ШҗМ©”yЙъОп·ҙ‘ӘЖчөИББПаSBCәПіЙЙъОпҢW®aҳIІ©У[•ю
- °¬ШҗМ©СыДъ…ўјУSBC2025өЪИэҢГәПіЙЙъОпҢW®aҳIІ©У[•ю
- °¬ШҗМ©”yЧФСРЙъОп·ҙ‘ӘЖчөИ®aЖ·ББПа2025ЙъОп°lҪНХ№
- °¬ШҗМ©Х\СыДъ…ўјУ2025қъДПҮшлHЙъОп°lҪНПөБРХ№
Copyright(C) 1998-2025 ЙъОпЖчІДҫW лҠФ’Јә021-64166852;13621656896 E-mailЈәinfo@bio-equip.com





