缺血性卒中治療的新方向|肢體電刺激的效應與神經血管耦聯機制
在卒中的康復中,施加一定強度和頻率的電刺激是常用的治療手段。而電刺激引發去極化、動作電位的傳遞、到最終產生相應的效果,整個過程涉及多種機制參與。其中,神經信號與血管功能之間的相互作用以及其中的機制,對于恢復腦血流灌注,改善疾病轉歸都有著重要價值。
肢體電刺激的效應
在腦缺血的治療領域,電刺激技術對于神經功能的保護作用,以及梗死的改善都有一定的效果。為了探明電刺激和血管變化之間的效應,通過肢體電刺激技術來提高梗死區的血流量一直是缺血性卒中研究的熱門方向。如2019年發表在Lancet的文章¹表明,采用翼腭神經節的電刺激療法,對于急性缺血性卒中的腦血流恢復、防止梗死灶擴大、穩定血腦屏障功能有很好的治療效果。
²研究人員將外周肢體電刺激技術應用于缺血性卒中的SD大鼠,并在肢體電刺激后同時監測皮層腦電及血流灌注情況,以監測神經血管耦聯(neurovascular coupling,NVC)機制的表現。
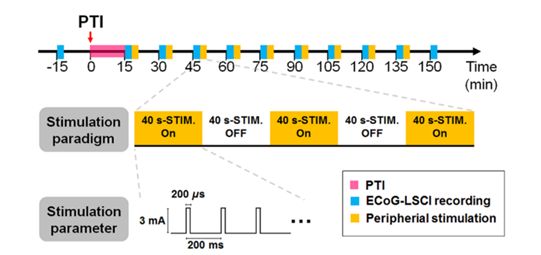
肢體電刺激模式及采集模式時間線
備注:藍色代表皮層腦電記錄及腦皮層血流灌注量記錄;PTI代表光栓法制造缺血性卒中模型;黃色代表電刺激的時間。
在使用該治療方法后,研究人員發現前肢電刺激后對于缺血區域周邊的側支循環血流灌注情況有明顯改善。其效果要優于對于后肢給予電刺激后的效果。
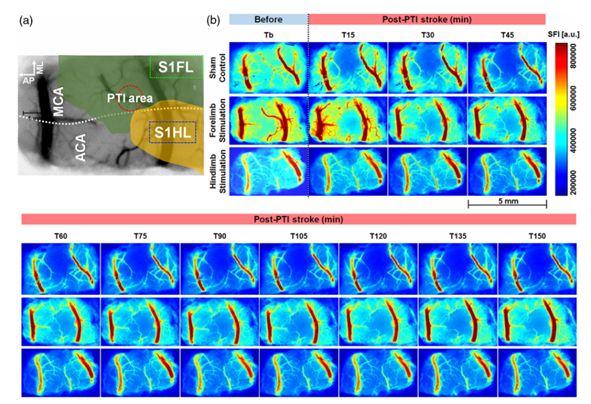
缺血性卒中后,在不同的肢體電刺激模式下通過激光散斑成像設備獲得的腦血流灌注量彩圖。
備注:在缺血性卒中發生以后,分別對于前肢和后肢進行電刺激,并觀察皮層側支循環區域血流的變化情況。通過灌注量圖像可見前肢電刺激后血流灌注情況的恢復要明顯優于對后肢進行電刺激的結果。
Abbr.S1-somatosensory cortex;S1FL- somatosensory cortex forelimb cortex;S1HL- somatosensory cortex hindlimb cortex;PTI- photothrombotic ischemic;MCA- middle cerebral artery;ACA- arteria cerebri anterior
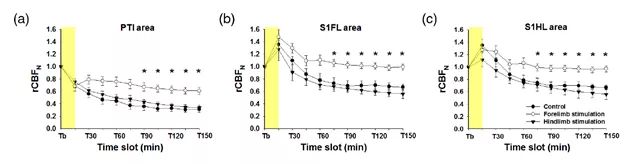
不同的側支循環區域內的灌注量量化數據情況。
備注:與血流灌注彩圖對應的,不同側支循環區域血流灌注量的恢復情況。可見前肢電刺激后的血流灌注量數據要明顯高于后肢電刺激后的血流灌注量數據。
研究發現通過電刺激前肢,可以改善缺血性卒中后側支循環的血流灌注情況,但這其中的神經血管耦聯機制仍待探索。
神經血管耦聯機制
大腦生理功能的實現依賴于神經活動與血流之間的相互配合,這種機制稱為神經血管耦合(Neurovascular Coupling,NVC)。
盡管大腦本身僅占體重的2%,但腦血流量仍占心輸出量的15%、靜止總耗氧量的20%。因此,腦血流量必須不斷地與當前活躍的大腦區域相匹配。而NVC是負責此復雜操作的機制,這種機制對于神經元興奮所致的大腦局部血流的分配具有重要意義。
NVC功能的完成需要由血管平滑肌細胞、周細胞、神經元、星形膠質細胞等細胞的參與。腦實質內的小動脈主要通過平滑肌細胞實現血管的舒縮功能,而毛細血管的舒縮功能更多依賴于周細胞。二者被星形膠質細胞終足包裹,且周圍存在豐富的神經元突觸。當神經元活動時,神經遞質被釋放出來,與星形膠質細胞上的受體結合,并激活鈣信號,傳遞至終足附近的血管上,激活對應的信號通路后,引發血管活性物質的釋放從而引起血管反應,這一系列復雜結構通過協同或拮抗作用參與基本NVC功能的維持與調節。
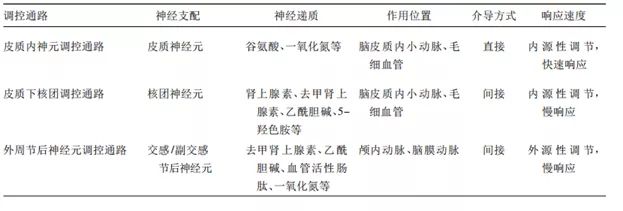
³依據不同神經支配來源分類的三種不同的腦血流神經血管調控機制。
如Anna Csiszar⁴等人通過老年小鼠的觸碰胡須刺激等系列實驗,結合血流灌注量的情況,得出靶向于線粒體的過氧化氫酶過表達改善了老年小鼠的神經血管耦合反應,并改善了行為表現。
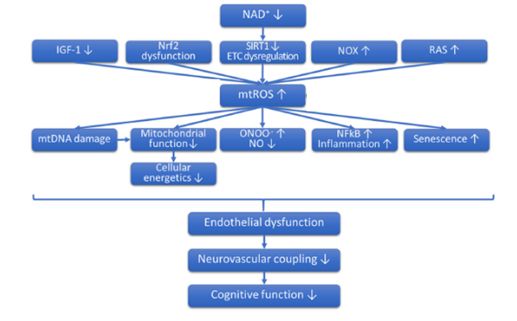
在線粒體活性氧的研究方向上與NVC相關的關鍵研究機制。
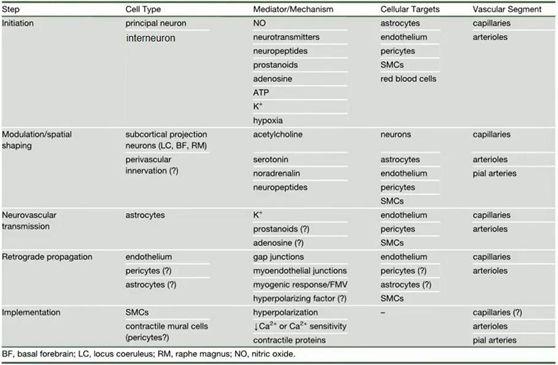
⁵NVC中不同類型細胞的機制及研究方向,不同的研究靶點所帶來的效應都能在血管層面體現。通過對組織血管效應的分析,對于完善NVC相關機制及效應研究有很大幫助。

NVC機理中相關的研究方向眾多,作為使大腦血流量不斷適應大腦活動的重要機制⁶,NVC與維持不斷變化血壓的大腦自動調節(cerebral autoregulation)共同維護大腦血循環系統動態平衡。探索神經血管耦聯機制及其生理功能,也可以為病理狀態下腦血流的恢復提供可能干預的靶點,為缺血性卒中的研究提供新的切入點。
【參考文獻】
¹ Bornstein NM, Saver JL, et al. An injectable implant to stimulate the sphenopalatine ganglion for treatment of acute ischaemic stroke up to 24 h from onset (ImpACT-24B): an international, randomised, double-blind, sham-controlled, pivotal trial. Lancet. 2019 Jul 20;394(10194):219-229.
² Pan HC, Liao LD, et al. Neurovascular function recovery after focal ischemic stroke by enhancing cerebral collateral circulation via peripheral stimulation-mediated interarterial anastomosis. Neurophotonics. 2017 Jul;4(3):035003.
³ 馬思明,汪露,楊靜雯,曹燕,蘇鑫童,劉存志.腦內神經血管耦合功能調控機制的研究進展[J].中國腦血管病雜志,2019,16(12):667-672.
⁴ Csiszar A, Yabluchanskiy A, et al. Overexpression of catalase targeted to mitochondria improves neurovascular coupling responses in aged mice. Geroscience. 2019 Oct;41(5):609-617.
⁵ https://www.youtube.com/watch?v=x4FEw61rIxM
⁶ Spronck B, Martens EG, et al. A lumped parameter model of cerebral blood flow control combining cerebral autoregulation and neurovascular coupling. Am J Physiol Heart Circ Physiol. 2012 Nov 1;303(9):H1143-53.





