三維潮汐式生物反應(yīng)器于間充質(zhì)干細胞的應(yīng)用
前 言
未來的細胞治療需要大量的間充質(zhì)干細胞(MSCs),每個劑量從1000萬到2億多個細胞不等。當需要超過5000萬個細胞的大劑量使用時,傳統(tǒng)的平板培養(yǎng)是不切實際的。而利用生物反應(yīng)器并結(jié)合線性放大、過程控制和自動化,是解決這一需求的主要方法。然而許多生物反應(yīng)器在MSCs培養(yǎng)方面都面臨技術(shù)難題,比如如何控制培養(yǎng)基充分混合的同時將剪切力最小化,以及如何從具有高產(chǎn)量和高活性的片狀載體中分離得到細胞等諸多難點。
潮汐式生物反應(yīng)器,利用3D片狀載體(BioNOC II)建立了一個強大的、可擴展的平臺,以滿足未來臨床治療的需求。在整個培養(yǎng)期間,監(jiān)測細胞培養(yǎng)條件,并測量生長過程參數(shù),如葡萄糖消耗量和pH值,以確保適當?shù)姆糯蟆M瑫r研究優(yōu)化干細胞培養(yǎng)系統(tǒng)所需的細胞接種密度、培養(yǎng)基培養(yǎng)條件和改進的生物工藝參數(shù)等關(guān)鍵問題。總的來說,Esco將提供過程優(yōu)化與質(zhì)量控制以及放大生產(chǎn)過程中的相關(guān)標準,以便協(xié)助用戶將學(xué)術(shù)或工業(yè)研發(fā)轉(zhuǎn)化為面向未來的臨床試驗和商業(yè)化銷售。

各組織來源MSCs的生長情況
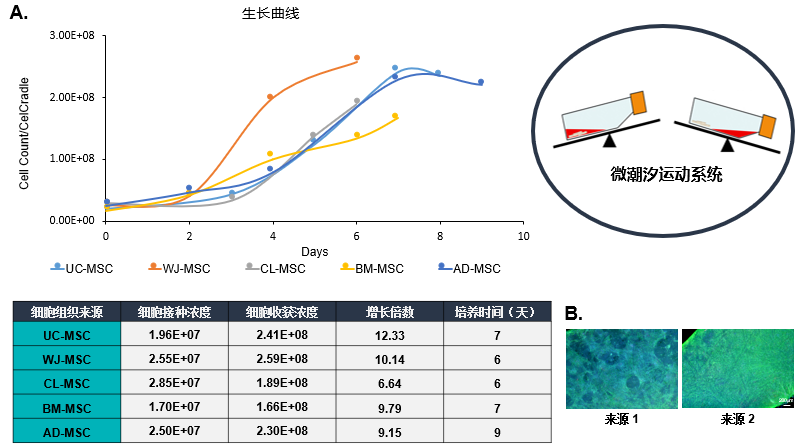
(A)用潮汐式生物反應(yīng)器系統(tǒng)成功擴增了不同組織來源的MSCs。MSCs的常見組織來源,如臍帶間充質(zhì)干細胞(UC-MSC)、沃頓膠間充質(zhì)干細胞(WJ-MSC)、骨髓間充質(zhì)干細胞(BM-MSC)和脂肪間充質(zhì)干細胞(AD-MSC),在培養(yǎng)后7天內(nèi)普遍可擴增10倍。上表列出了使用商業(yè)細胞來源進行優(yōu)化的不同組織來源MSCs的接種密度。
(B)將同類型(相同組織來源)但細胞來源不同的MSCs,從低播種密度進行擴增能力測試。結(jié)果顯示,來源2的BM-MSCs與來源1的BM-MSCs生長情況存在明顯差異,因此在進行線性放大擴增之前,需要對每個來源MSCs進行播種密度、培養(yǎng)基變化規(guī)律等參數(shù)進行優(yōu)化。
MSCs在不同培養(yǎng)基中的擴增情況
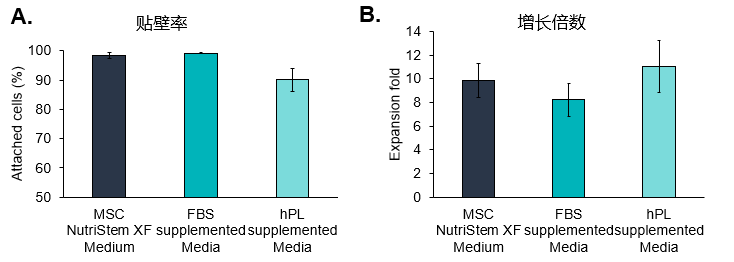
(A) 將UC-MSCs接種于含血清代替物(hPL)的培養(yǎng)基中,觀察到其對載體的貼壁效率較低。
(B) 盡管觀察到的附著效率較低,但使用血清代替物補充培養(yǎng)基,使不同組織來源MSCs的細胞擴增倍數(shù)增大。
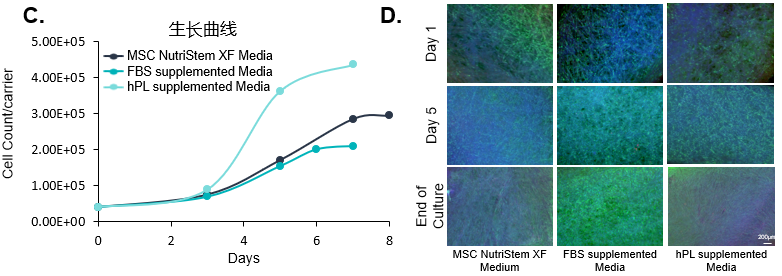
(C) 在將UC-MSCs接種到BioNOC II載體之前,對不同培養(yǎng)基類型培養(yǎng)的細胞進行2次以上傳代,以監(jiān)測其增殖速率。結(jié)果顯示含血清代替物(hPL)培養(yǎng)基培養(yǎng)的細胞增長最快。
(D) 熒光圖像顯示細胞在培養(yǎng)期間在載體上的擴增情況,結(jié)果顯示含胎牛血清(FBS)培養(yǎng)基的細胞生長較好,含血清代替物(hPL)的次之。綜合考量,使用含血清代替物培養(yǎng)基是更優(yōu)的選擇。
綠色:熒光素二乙酸酯(活細胞細胞質(zhì))
藍色:Hoechst 33342(細胞核)
紅色:碘化丙啶(死細胞)
細胞收集工藝優(yōu)化
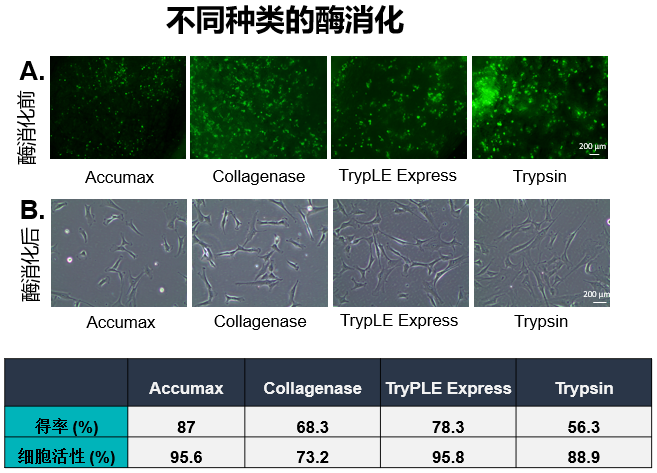
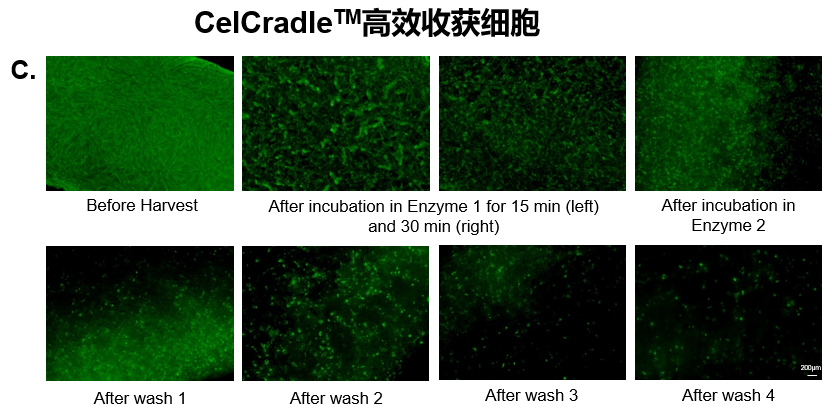
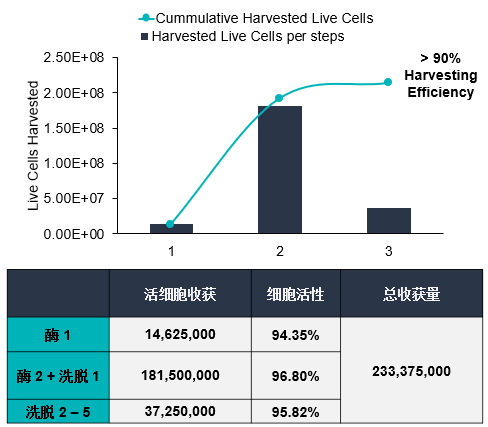
通過優(yōu)化參數(shù),開發(fā)了一種從BioNOC II載體高效收獲UC-MSCs的方法。在整個實驗過程中,使用熒光素二乙酸酯(FDA)對BioNOC II載體上的活細胞進行染色。
質(zhì)量控制
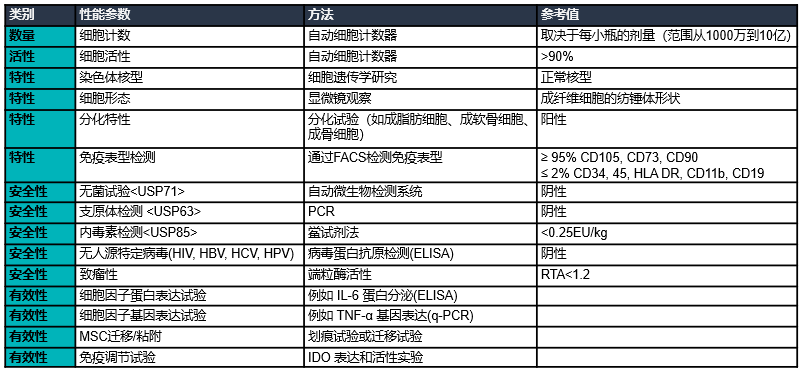
結(jié) 論
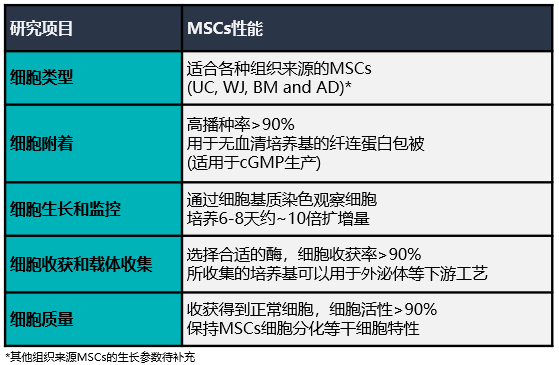
*潮汐式生物反應(yīng)器是由無菌一次性CelCradle細胞培養(yǎng)瓶和波紋管壓縮平臺組成,可線性放大,且在培養(yǎng)過程中支持取樣監(jiān)測。
*小規(guī)模系統(tǒng)支持MSCs早期研發(fā)階段,可以低成本高效率進行參數(shù)優(yōu)化。
*為大批量生產(chǎn)MSCs提供一個很好的平臺。

- 生物反應(yīng)器助力7.6倍產(chǎn)量提升的蝦青素生產(chǎn)工藝快速優(yōu)化
- 細胞培養(yǎng)微載體:不同材料的優(yōu)缺點及應(yīng)用指南
- 生物制藥行業(yè)中工藝轉(zhuǎn)移基本原則及關(guān)注重點
- 不同細胞培養(yǎng)強化工藝的生物反應(yīng)器生產(chǎn)率和培養(yǎng)基成本比較
- 生物反應(yīng)器助力傳統(tǒng)培養(yǎng)向強化工藝的迭代轉(zhuǎn)型
- 微載體的原理與分類
- 院士解讀央視紀錄片《向新出發(fā)》生物制造產(chǎn)業(yè)現(xiàn)狀及前景
- 微重力細胞培養(yǎng)設(shè)備綜述:儀器選型、使用、操作與維修





