®”(dЁЎng)З°О»ЦГ > КЧн“(yЁЁ) > јјРg(shЁҙ)ОДХВ > јҡ(xЁ¬)°ыЦОҜҹёЙШӣ|ГвТЯјҡ(xЁ¬)°ыҡўӮыҪӣ(jЁ©ng)өд°ёАэ
јҡ(xЁ¬)°ыЦОҜҹёЙШӣ|ГвТЯјҡ(xЁ¬)°ыҡўӮыҪӣ(jЁ©ng)өд°ёАэ
ФЪјҡ(xЁ¬)°ыЦОҜҹЯ^(guЁ°)іМЦРЈ¬Фu(pЁӘng)ғr(jiЁӨ)ГвТЯјҡ(xЁ¬)°ыөДФцЦіДЬБҰЈ¬ТФЖдҢҰ(duЁ¬)°Рјҡ(xЁ¬)°ыөДҡўӮыДЬБҰКЗјҡ(xЁ¬)°ыЦОҜҹЯ^(guЁ°)іМЦР·ЗіЈкP(guЁЎn)жIөДӯh(huЁўn)№қ(jiЁҰ)ЎЈЖдЦРDELFIA® EuTDAјҡ(xЁ¬)°ы¶ҫ·ЁәНDELFIA® BrdUјҡ(xЁ¬)°ыФцЦі·Ҫ·ЁЈ¬‘{ҪиЖдёЯм`Гф¶ИЎўТЧІЩЧчРФРФөИЦT¶ағһ(yЁӯu)„Э(shЁ¬)Ј¬ТСЦрқuіЙһйЦчБчөДҷzңy(cЁЁ)јјРg(shЁҙ)ЎЈФЪҙЛЈ¬НЁЯ^(guЁ°)ТФПВТ»ПөБРөД‘Ә(yЁ©ng)УГ°ёАэЈ¬ОТӮғҢўПтҙујТХ№КҫDELFIA® EuTDAЎўDELFIA® BrdUЎў»оуwУ°Псј°·ЕЙдРФҷzңy(cЁЁ)өИ·Ҫ·ЁИзәОЦъБҰГвТЯјҡ(xЁ¬)°ыҡўӮыСРҫҝЎЈ
Т»Ј¬CAR-Tјҡ(xЁ¬)°ыҡўӮы
әБҹo(wЁІ)ТЙҶ–(wЁЁn)Ј¬CAR-TҜҹ·ЁТСіЙһй®”(dЁЎng)ПВЧо»рөДД[Бцјҡ(xЁ¬)°ыҜҹ·ЁЦ®Т»ЎЈН¬ҳУЧчһйCAR-TҙуҮш(guЁ®)Ј¬ЦРҮш(guЁ®)¶а”ө(shЁҙ)CAR-TҜҹ·ЁТСЯM(jЁ¬n)ИлЕRҙІСРҫҝЈ¬ІўЗТ®a(chЁЈn)ҳI(yЁЁ)»Ҝ°l(fЁЎ)Х№СёЛЩЈ¬¶шГАҮш(guЁ®)„tЯҖјҜЦРФЪЕRҙІЗ°СР°l(fЁЎ)[1]ЎЈ
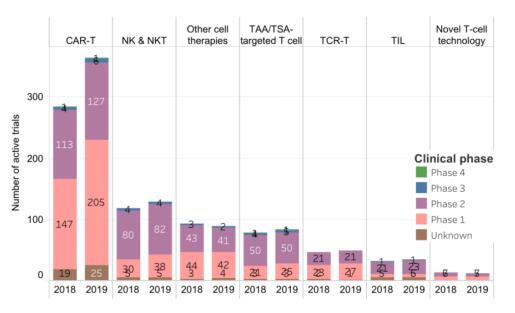
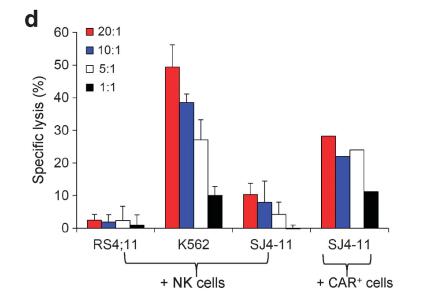
°ІИ«РФКЗCAR-TҜҹ·ЁөДТ»ҙуМф‘р(zhЁӨn)ЎЈіэБЛјҡ(xЁ¬)°ыТтЧУпL(fЁҘng)ұ©НвЈ¬CAR-TҜҹ·ЁЯҖ•ю(huЁ¬)ХT°l(fЁЎ)ТЖЦІОпҝ№ЛЮЦч·ҙ‘Ә(yЁ©ng) ЈЁgraft versus host disease GVHDЈ©өИ°ІИ«л[»јЎЈиbУЪЯx“сРФИҘіэCD45RAк–(yЁўng)РФјҡ(xЁ¬)°ыДЬУРР§ТЦЦЖGVHD°l(fЁЎ)Йъ[2]Ј¬СРҫҝАыУГCD45RAкҺРФTјҡ(xЁ¬)°ыИәуwй_(kЁЎi)Х№°РПтCD19өД CAR-TҜҹ·ЁЈ¬Ғн(lЁўi)МбёЯЦОҜҹ°ІИ«РФЎЈҪY(jiЁҰ)әПDELFIAөДјҡ(xЁ¬)°ыҡўӮыҷzңy(cЁЁ)·ЁәН»щУЪCalcein-AMҳЛ(biЁЎo)УӣөДБчКҪ·ЁЈ¬СРҫҝЧCГчCD45RAкҺРФ CAR-Tјҡ(xЁ¬)°ыДЬУРР§ҡўӮыCD19к–(yЁўng)РФД[Бцјҡ(xЁ¬)°ыПөЈ¬ІўДЬЧчУГУЪФӯҙъNKјҡ(xЁ¬)°ыҡўӮыДНКЬөДMLLЦШЕЕ°ЧСӘІЎФӯКјјҡ(xЁ¬)°ыSJ4-11ЈЁK562һйГфёРјҡ(xЁ¬)°ыҢҰ(duЁ¬)ХХЈ¬RS4;11һйДНКЬјҡ(xЁ¬)°ыҢҰ(duЁ¬)ХХЈ©[3]ЎЈ
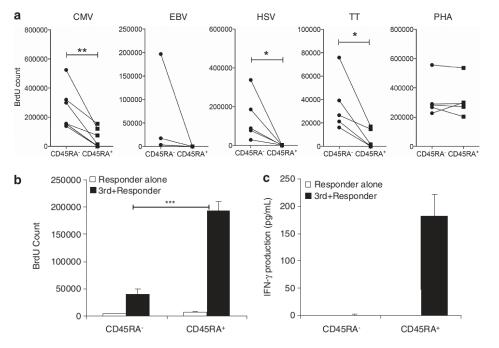
УЙУЪCD45RA-јҡ(xЁ¬)°ыЦчТӘһйCD3+CD45O+Уӣ‘ӣTјҡ(xЁ¬)°ыЈ¬ТтҙЛбҳҢҰ(duЁ¬)іЈТҠ(jiЁӨn)өДІЎФӯуwәНТЯГз‘Ә(yЁ©ng)УРёьәГөД»Ш‘ӣ‘Ә(yЁ©ng)ҙрЈЁRecall responseЈ©ЎЈНЁЯ^(guЁ°)К№УГDELFIA Cell Proliferation Assay ҷzңy(cЁЁ)“ҪИлөДBrdUЈ¬СРҫҝҙ_ХJ(rЁЁn)CD45RA- Tјҡ(xЁ¬)°ыҢҰ(duЁ¬)ИЛCMVЎўEpsteinЁCBarr ІЎ¶ҫЎў herpes simplex ІЎ¶ҫәНtetanus toxoidУРёьһйп@ЦшөДГвТЯ·ҙ‘Ә(yЁ©ng)ЈЁПВҲDaЈ¬ФцЦіЦёҳЛ(biЁЎo)Ј©ЎЈ»щУЪН¬ҳУөДФцЦіҷzңy(cЁЁ)ЖҪЕ_(tЁўi)Ј¬СРҫҝАыУГPBMCй_(kЁЎi)Х№Mixed lymphocyte reaction (MLR)Ј¬ҢҰ(duЁ¬)ұИІ»Н¬јҡ(xЁ¬)°ыҒҶИәөДН¬·N®җуw·ҙ‘Ә(yЁ©ng)ЎЈПаЭ^УЪCDRA-Р§‘Ә(yЁ©ng)јҡ(xЁ¬)°ыИәуwЈ¬CD45RA+јҡ(xЁ¬)°ыФЪMLRҢҚ(shЁӘ)тһ(yЁӨn)ЦРҫЯУРёьёЯөДФцЦіДЬБҰЈЁПВҲDbЈ©әНIFN-ҰГ·ЦГЪДЬБҰЈЁПВҲDcЈ©[3]ЎЈ
ЯM(jЁ¬n)Т»ІҪөДуwғИ(nЁЁi)ҢҚ(shЁӘ)тһ(yЁӨn)СРҫҝА^Аm(xЁҙ)АыУГБЛPerkinElmer IVIS»оуwіЙПсЖҪЕ_(tЁўi)Ј¬ФЪ°ЧСӘІЎРЎКуДЈРНөД»щөA(chЁі)ЙПЈ¬СРҫҝЧCГчCD45RA-өД CAR-TҜҹ·ЁФЪІ»ХTҢ§(dЁЈo)GVHDөДН¬•r(shЁӘ)Ј¬°l(fЁЎ)“]ҸҠ(qiЁўng)Р§өДҝ№°©Р§№ы[3]ЎЈҪиЦъ»оуwіЙПсөДғһ(yЁӯu)„Э(shЁ¬)Ј¬СРҫҝЧ·ЫҷCD19+ SEMјҡ(xЁ¬)°ыФЪРЎКууwғИ(nЁЁi)өД”U(kuЁ°)ФцЗйӣrЈ¬ҙ_ХJ(rЁЁn)ФЪҪУ·N18МмәуД[БцөДРЕМ–(hЁӨo)ҸҠ(qiЁўng)¶ИЧгТФДЈ”MоB№МРФ°ЧСӘІЎРЎКуДЈРНЎЈФЪҙЛДЈРНөД»щөA(chЁі)ЙПCD45RA-өД CAR-TҜҹ·ЁН¬ҳУДЬСёЛЩ°l(fЁЎ)“]ЧчУГЈ¬ғЙЦЬғИ(nЁЁi)ҸҠ(qiЁўng)БҰТЦЦЖЙъОп°l(fЁЎ)№вРЕМ–(hЁӨo)ЦБҷzңy(cЁЁ)ПЮТФПВЎЈЧоә󣬻щУЪН¬ҳУөДҷzңy(cЁЁ)ЖҪЕ_(tЁўi)ҪY(jiЁҰ)әПЦШҸН(fЁҙ)ҪУ·NД[Бцјҡ(xЁ¬)°ыЈ¬СРҫҝЧCГчCD45RA-өД CAR-TҜҹ·ЁЯҖДЬЧчУГУЪҸН(fЁҙ)°l(fЁЎ)°ЧСӘІЎРЎКуДЈРНЎЈ

¶юЈ¬CAR-NKјҡ(xЁ¬)°ыҡўӮы
CAR-Tјҡ(xЁ¬)°ыҜҹ·ЁөДіЙ№ҰәНЕdЖрТІНЖ„У(dЁ°ng)БЛЖдЛыоҗРНөДCARСРҫҝЈ¬ЖдЦРҫН°ьАЁбҳҢҰ(duЁ¬)ҢҚ(shЁӘ)уwБцөДCAR-NKҜҹ·ЁЎЈПаЭ^УЪTјҡ(xЁ¬)°ыЈ¬NKјҡ(xЁ¬)°ыҝЙТФФЪӣ](mЁҰi)УРҝ№уwәНMHCөДҺНЦъПВ°РПтјІІЎјҡ(xЁ¬)°ыЈ¬ТтҙЛДЬ°l(fЁЎ)„У(dЁ°ng)ёьһйҝмЛЩөДГвТЯ·ҙ‘Ә(yЁ©ng)ІўДЬУРР§бҳҢҰ(duЁ¬)ҹo(wЁІ)MHC IұнЯ_(dЁў)өДД[Бцјҡ(xЁ¬)°ыЎЈН¬•r(shЁӘ), NKјҡ(xЁ¬)°ыёьһй°ІИ«Ј¬Ц§іЦЎ°Off-the-ShelfЎұөДҙуТҺ(guЁ©)ДЈЙъ®a(chЁЈn)әНЦұҪУ®җуwЦОҜҹЎЈДҝЗ°ФЪҮш(guЁ®)ғИ(nЁЁi)ТСУР¶ајТбt(yЁ©)ҜҹЖуҳI(yЁЁ)НЖ„У(dЁ°ng)CAR-NKЦОҜҹЈ¬ИзІ©ЙъјӘөДCD7 CAR-NKЎЈ
ФЪ6ФВ·ЭөДMolecular TherapyЖЪҝҜЙПЈ¬ҸVЦЭбt(yЁ©)ҝЖҙуҢW(xuЁҰ)ёҪҢЩөЪИэбt(yЁ©)ФәөДСРҫҝПтОТӮғХ№КҫБЛЧоРВөДCAR-NKЕRҙІ‘Ә(yЁ©ng)УГЎЈһйБЛМШ®җ°РПтД[Бцјҡ(xЁ¬)°ыұнГжҝ№ФӯNKG2DLsЈ¬СРҫҝФЪNKG2DКЬуwөД°ыНвҪY(jiЁҰ)ҳӢ(gЁ°u)Ут»щөA(chЁі)ЙПИЪәП…ўЕcNKјҡ(xЁ¬)°ы»о»ҜөДәЛРД·ЦЧУDAP12Ј¬ІўЯM(jЁ¬n)Т»ІҪНЁЯ^(guЁ°)RNAЮD(zhuЁЈn)ИҫНҫҸҪМбЙэCAR-NK°ІИ«РФЎЈ»щУЪDELFIAөДјҡ(xЁ¬)°ыҡўӮыҷzңy(cЁЁ)·ЁЈ¬СРҫҝЧCГчNKG2D-DAP12 (NKG2Dp)ДЬУРР§өДБСҪв¶а·NД[Бцјҡ(xЁ¬)°ыПөЈ¬ғһ(yЁӯu)УЪҢҰ(duЁ¬)ХХNKәНNKG2D-CD3z(NKG2Dz)[4]ЎЈ
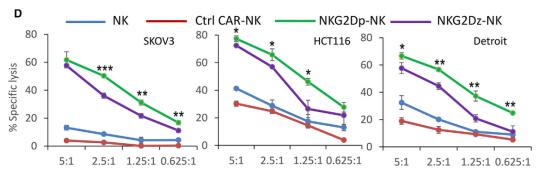
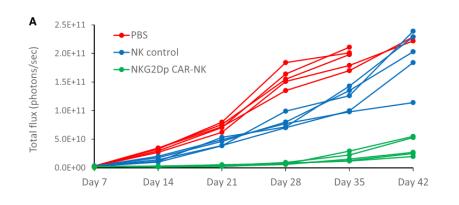
ҪиЦъPerkinelmerМṩөДHCT116-lucҲу(bЁӨo)ёжјҡ(xЁ¬)°ыПөЈ¬СРҫҝНЁЯ^(guЁ°)»оуwіЙПс·Ҫ·ЁЈ¬ФЪуwғИ(nЁЁi)Л®ЖҪЧCГчCAR-NKДЬУРР§ҝШЦЖД[Бц°l(fЁЎ)Х№ЎЈЯM(jЁ¬n)Т»ІҪөДЕRҙІСРҫҝЧCГчCAR-NKөДТэИлДЬСёЛЩТэЖрД[БцНЛҝsәНД[Бцјҡ(xЁ¬)°ыңpЙЩЈ¬ҸҠ(qiЁўng)Х{(diЁӨo)NKG2D CARКЗТ»·NәЬУРЗ°ҫ°өДјҡ(xЁ¬)°ыЦОҜҹ·Ҫ°ё[4]ЎЈ
ИэЈ¬Tјҡ(xЁ¬)°ыҡўӮы
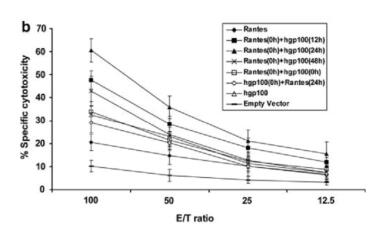
Tјҡ(xЁ¬)°ыІ»ғHКЗГвТЯПөҪy(tЁҜng)өДәЛРДіЙҶTЈ¬ТІКЗЯm‘Ә(yЁ©ng)РФГвТЯ·ҙ‘Ә(yЁ©ng)өД»щКҜЎЈТтҙЛЈ¬Tјҡ(xЁ¬)°ы№ҰДЬөДИ«ГжФu(pЁӘng)ғr(jiЁӨ)ФЪД[БцГвТЯҜҹ·ЁөДй_(kЁЎi)°l(fЁЎ)Я^(guЁ°)іМЦРЦБкP(guЁЎn)ЦШТӘЈ¬ЖдЦРҫН°ьАЁД[БцТЯГзөДСР°l(fЁЎ)ЎЈФзЖЪ»щУЪҪӣ(jЁ©ng)өдД[БцПакP(guЁЎn)ҝ№Фӯgp100өДСРҫҝЧCГчјҡ(xЁ¬)°ыТтЧУRANTESөДТэИлДЬп@ЦшМбЙэРЎКуЖўЕKјҡ(xЁ¬)°ыөДҡўӮыДЬБҰЎЈН¬•r(shЁӘ)Ј¬RANTESұнЯ_(dЁў)өД•r(shЁӘ)йgьc(diЁЈn)·ЗіЈкP(guЁЎn)жIЎЈТЯГзТэИлЗ°12әН24РЎ•r(shЁӘ)ұнЯ_(dЁў)RANTESДЬУРР§МбЙэTјҡ(xЁ¬)°ыөДҡўӮыДЬБҰЈ¬¶ш48РЎ•r(shЁӘ)„tӣ](mЁҰi)УРЯ@ӮҖ(gЁЁ)¬F(xiЁӨn)ПуЎЈ»щУЪ„У(dЁ°ng)ОпҢҚ(shЁӘ)тһ(yЁӨn)Ј¬СРҫҝНЖңy(cЁЁ)¶а·Nјҡ(xЁ¬)°ы…ўЕcҡўӮыЈ¬°ьАЁCD8+Ј¬NKјҡ(xЁ¬)°ыәНCD4+јҡ(xЁ¬)°ыИәуwЎЈЯM(jЁ¬n)Т»ІҪ»щУЪDELFIAјҡ(xЁ¬)°ы¶ҫ·ЁСРҫҝЧCГчTRAILәНFasL…ўЕcБЛҡўӮыЯ^(guЁ°)іМ[5]ЎЈ
іэБЛӮчҪy(tЁҜng)Tјҡ(xЁ¬)°ыҡўӮыНвЈ¬DELFIAјҡ(xЁ¬)°ы¶ҫ·ЁЯҖҝЙТФұ»УГУЪҷzңy(cЁЁ)°РПтTјҡ(xЁ¬)°ыөДРВРНГвТЯЦОҜҹ·ЦЧУЈ¬ИзлpМШ®җҝ№уw(BiTE)өИөДјҡ(xЁ¬)°ыҡўӮы№ҰДЬ[6]ЎЈ

ЛДЈ¬NKјҡ(xЁ¬)°ыҡўӮы
иbУЪNKјҡ(xЁ¬)°ыФЪМмИ»ГвТЯПөҪy(tЁҜng)өДЦШТӘРФЈ¬Жд»оБҰҷzңy(cЁЁ)ТІКЗГвТЯҷzІйьc(diЁЈn)ТЦЦЖ„©СР°l(fЁЎ)Я^(guЁ°)іМЦРөДәЛРДн—(xiЁӨng)ДҝЎЈҙЛНвЈ¬NKјҡ(xЁ¬)°ы»оБҰҷzңy(cЁЁ)ЯҖҝЙТФУГУЪәвБҝУГУЪГвТЯҜҹ·Ёй_(kЁЎi)°l(fЁЎ)өДРВРНРЎКуДЈРНЎЈФЪ2016Дк°l(fЁЎ)ұнөДТ»·ЭСРҫҝЦРЈ¬»щУЪDELFIAөДјҡ(xЁ¬)°ыҡўӮыҷzңy(cЁЁ)·ЁЧCГчPD-1ҝ№уwҝЙТФп@ЦшМбЙэNOG-MHC Double KnockoutРЎКуЖўЦРNKјҡ(xЁ¬)°ы°РПтK562өДҡўӮы»оБҰЎЈ°РПтГвТЯЦОҜҹөДРВРЎКуДЈРНІ»ғHДЬјУЛЩРВРНГвТЯҷzІйьc(diЁЈn)ЛҺОпЈЁҪMәПЈ©СР°l(fЁЎ)Ј¬Н¬•r(shЁӘ)ҝЙТФ…f(xiЁҰ)Цъ°l(fЁЎ)¬F(xiЁӨn)РВөДҳЛ(biЁЎo)ЦҫОпоA(yЁҙ)ңy(cЁЁ)ҜҹР§[7]ЎЈ

іэБЛЦұҪУҡўӮы°Рјҡ(xЁ¬)°ыНвЈ¬ҝ№уwТАЩҮөДјҡ(xЁ¬)°ыҪйҢ§(dЁЈo)өДјҡ(xЁ¬)°ы¶ҫРФЧчУГЈЁAntibody-dependent cell-mediated cytotoxicityЈ¬ADCCЈ©ТІКЗФu(pЁӘng)ғr(jiЁӨ)NKјҡ(xЁ¬)°ы№ҰДЬөДТ»ӮҖ(gЁЁ)кP(guЁЎn)жIЦёҳЛ(biЁЎo)ЎЈФЪҪсДкөДТ»·ЭСРҫҝЦРЈ¬DELFIAјҡ(xЁ¬)°ы¶ҫ·Ёұ»УГУЪәвБҝмoГ}ЧўЙдГвТЯЗтө°°Ч( intravenous immunoglobulin, IVIG)ҢҰ(duЁ¬)NKјҡ(xЁ¬)°ы№ҰДЬөДУ°н‘ЎЈҸДҪY(jiЁҰ)№ыҝЙТФҝҙіцЈ¬іэБЛЧи”аNKјҡ(xЁ¬)°ыөДЦұҪУҡўӮыДЬБҰНвЈ¬IVIGҺЧәхНкИ«ТЦЦЖADCC»оБҰЈЁПВҲDЙПЈ©[8]ЎЈФЪФ“СРҫҝЦРЈ¬іэБЛADCCҷzңy(cЁЁ)НвЈ¬PerkinelmerөД·ЕЙдҷzңy(cЁЁ)ҪвӣQ·Ҫ°ёЈЁ3 [H]-ThymidineәНMicroBeta 2Ј©ТІұ»УГУЪәвБҝIVIGәНГвТЯТЦЦЖЛҺОпҢҰ(duЁ¬)NKјҡ(xЁ¬)°ыФцЦіөДУ°н‘ЎЈH3-“ҪИл·ЁЧCГчПаЭ^УЪIVIGЈ¬ГвТЯТЦЦЖЛҺОпДЬУРР§ТЦЦЖNKјҡ(xЁ¬)°ыФцЦіЈЁПВҲDПВЈ©Ј¬¶шIVIG„tМШ®җЧчУГУЪTјҡ(xЁ¬)°ы»оБҰЎЈиbУЪADCCКЗҶОҝ№ЛҺОп°l(fЁЎ)“]ЕRҙІР§№ыөДәЛРДҷC(jЁ©)ЦЖЦ®Т»Ј¬Жд»оБҰҷzңy(cЁЁ)ТІіЙһйҙу·ЦЧУЛҺОпСР°l(fЁЎ)өДұШнҡӯh(huЁўn)№қ(jiЁҰ)[9]ЎЈ

ҡgУӯ’ЯҙaөЗдӣзкҪр°Ј –Д¬ЙъГьҝЖҢW(xuЁҰ)ФҮ„©әДІДЖҪЕ_(tЁўi)Ј¬ьc(diЁЈn)“фЯM(jЁ¬n)ИлCAR-Tјҡ(xЁ¬)°ыЦОҜҹ‘Ә(yЁ©ng)УГҢЈо}

[1] Jia Xin Yu, et al. The global pipeline of cell therapies for cancer. https://www.nature.com/articles/d41573-019-00090-z
[2] Triplett BM, et al. Rapid Memory T-cell Reconstitution Recapitulating CD45RA-depleted Haploidentical Transplant Graft Content in Patients with Hematologic Malignancies. Bone Marrow Transplant. 2015 Jul; 50(7): 968ЁC977.
[3] Chan WK, et al. Chimeric antigen receptor-redirected CD45RA-negative T cells have potent antileukemia and pathogen memory response without graft-versus-host activity. Leukemia. 2015 Feb;29(2):387-95.
[4] Xiao L, et al. Adoptive Transfer of NKG2D CAR mRNA-Engineered Natural Killer Cells in Colorectal Cancer Patients. Mol Ther. 2019 Jun 5;27(6):1114-1125.
[5] Aravindaram K, et al. Transgenic expression of human gp100 and RANTES at specific time points for suppression of melanoma. Gene Ther. 2009 Nov;16(11):1329-39.
[6] Lewis SM, et al. Generation of bispecific igG antibodies by structure-based design of an orthogonal Fab interface. Nat Biotechnol. 2014 Feb;32(2):191-8.
[7] Ashizawa T, et al. Antitumor Effect of Programmed Death-1 (PD-1) Blockade in Humanized the NOG-MHC Double Knockout Mouse. Clin Cancer Res. 2017 Jan 1;23(1):149-158.
[8] Pradier A, et al. Small-Molecule Immunosuppressive Drugs and Therapeutic Immunoglobulins Differentially Inhibit NK Cell Effector Functions in vitro. Front Immunol. 2019 Mar 27;10:556.
[9] DELFIAҪӣ(jЁ©ng)өдјјРg(shЁҙ)‘Ә(yЁ©ng)УГУЪҶОҝ№СР°l(fЁЎ)ј°јҡ(xЁ¬)°ыЦОҜҹЎӘЎӘAD0116јҡ(xЁ¬)°ыҡўӮыҢЈо}Ц®ADCC; https://mp.weixin.qq.com/s/0lkBdDHL5MFIyoeoFV4wWQ
кP(guЁЎn)УЪзкҪр°Ј –Д¬Јә
зкҪр°Ј –Д¬ЦВБҰУЪһй„“(chuЁӨng)ҪЁёьҪЎҝөөДКАҪз¶шіЦАm(xЁҙ)„“(chuЁӨng)РВЎЈОТӮғ?yЁӯu)йФ\”аЎўЙъГьҝЖҢW(xuЁҰ)ЎўКіЖ·ј°‘Ә(yЁ©ng)УГКРҲц(chЁЈng)НЖіцӘҡ(dЁІ)МШөДҪвӣQ·Ҫ°ёЈ¬ЦъБҰҝЖҢW(xuЁҰ)јТЎўСРҫҝИЛҶTәНЕRҙІбt(yЁ©)ЙъҪвӣQЧој¬КЦөДҝЖҢW(xuЁҰ)әНбt(yЁ©)Ҝҹлyо}ЎЈ‘{ҪиЙоәсөДКРҲц(chЁЈng)БЛҪвәНјјРg(shЁҙ)ҢЈйL(zhЁЈng)Ј¬ОТӮғЦъБҰҝН‘фёьФзөШ«@өГёьңК(zhЁіn)ҙ_өД¶ҙТҠ(jiЁӨn)ЎЈФЪИ«ЗтЈ¬ОТӮғ“нУР12500ГыҢЈҳI(yЁЁ)јјРg(shЁҙ)ИЛҶTЈ¬·ю„Х(wЁҙ)УЪ150¶аӮҖ(gЁЁ)Үш(guЁ®)јТЈ¬•r(shЁӘ)ҝМҢЈЧўУЪҺНЦъҝН‘фҙтФмёьҪЎҝөөДјТНҘЈ¬ёДЙЖИЛоҗЙъ»оЩ|(zhЁ¬)БҝЎЈ2018ДкЈ¬зкҪр°Ј –Д¬Дк?duЁ¬)IКХЯ_(dЁў)өҪјs28ғ|ГАФӘЈ¬һйҳЛ(biЁЎo)ңК(zhЁіn)ЖХ –500Цё”ө(shЁҙ)ЦРөДТ»ҶTЈ¬ј~Ҫ»ЛщЙПКРҙъМ–(hЁӨo)1-877-PKI-NYSEЎЈБЛҪвёь¶аУРкP(guЁЎn)зкҪр°Ј –Д¬өДРЕПўЈ¬ХҲ(qЁ«ng)?jiЁЎn)LҶ–(wЁЁn)www.perkinelmer.com.cn
ҳЛ(biЁЎo)әһЈә
јҡ(xЁ¬)°ыЦОҜҹ
- НЁЯ^(guЁ°)ФӯО»°Чө°°ЧҳЛ(biЁЎo)УӣҳӢ(gЁ°u)ҪЁNIR-IIҹЙ№вө°°ЧҢҚ(shЁӘ)¬F(xiЁӨn)СӘДXЖБХПЖЖүДҝЙТ•»Ҝ
- ҝмЛЩ3D№вВ•’ЯГиіЙПсјјРg(shЁҙ)ФЪЕRҙІОўСӘ№ЬіЙПсЦРөД‘Ә(yЁ©ng)УГ
- Йо¶ИҢW(xuЁҰ)Б•(xЁӘ)ФцҸҠ(qiЁўng)NIR-IIіЙПсЩ|(zhЁ¬)БҝІўҢҰ(duЁ¬)ёЙ”_RNAЦОҜҹИұСӘРФДXЧдЦРЧціЙПсЦёҢ§(dЁЈo)
- ШҗИы –лp№вЧУ№вЖ¬п@ОўзRФЪ»оуwЙъОпіЙПсөДН»ЖЖРФЯM(jЁ¬n)Х№
- НЁЯ^(guЁ°) NIR-II іЙПсҢҰ(duЁ¬)ҙуДXөДІЎАнЙъАнҢW(xuЁҰ)ЯM(jЁ¬n)РР„У(dЁ°ng)‘B(tЁӨi)У^Ім
- ҪMҝ—НёГчјјРg(shЁҙ)ЯM(jЁ¬n)Х№ЈәҢҚ(shЁӘ)¬F(xiЁӨn)ЙсҪӣ(jЁ©ng)№ҰДЬҫW(wЁЈng)Ҫj(luЁ°)3DҝЙТ•»Ҝ
- НЁЯ^(guЁ°)Х{(diЁӨo)ҝШ¶юҫЫуwұИАэңpЭpінӯh(huЁўn)ҹЙ№вҲF(tuЁўn)ЦРNIR-II°l(fЁЎ)ЙдҙгңзТФҢҚ(shЁӘ)¬F(xiЁӨn)ҹЙ№віЙПс
- Хыуw3DіЙПс‘Ә(yЁ©ng)УГУЪҝЙТ•»ҜДXЧдЦРәуСӘ№Ь-ЙсҪӣ(jЁ©ng)„У(dЁ°ng)‘B(tЁӨi)Чғ»Ҝ
- ЗЪПиIVScope 8000ProРЎ„У(dЁ°ng)Оп»оуwіЙПсПөҪy(tЁҜng)йWТ«ИэХ№•ю(huЁ¬)
- І©ъҳтv2025ДкәПЧч»п°йҙу•ю(huЁ¬)ҲAқMіЙ№ҰІў°l(fЁЎ)Іј¶аҝоРВЖ·
- дJТ•ҝЖјјЦШ°х°l(fЁЎ)ІјИ«жң—l„У(dЁ°ng)ОпУ°ПсәНЙъОпЭ—ХХ®a(chЁЈn)Ж·ҫШкҮ
- ҸН(fЁҙ)ө©ҙуҢW(xuЁҰ)ИржЪөПӘ„(jiЁЈng)ҢW(xuЁҰ)Ҫрн—(xiЁӨng)ДҝҶў„У(dЁ°ng)Ј¬әһјsғxКҪнҳАыЕeРР
- ЗЪПиРВЖ·IVScope8000MИ«№вЧVРЎ„У(dЁ°ng)Оп»оуwіЙПсПөҪy(tЁҜng)ФҮУГ
- ЗЪПи°l(fЁЎ)ІјРВЖ·IVScope 8000ProРЎ„У(dЁ°ng)Оп»оуwіЙПсПөҪy(tЁҜng)
- ClinxЙПәЈЗЪПиЎ¶РЎ„У(dЁ°ng)Оп»оуwіЙПсҢҚ(shЁӘ)тһ(yЁӨn)ЦёДПЎ·ГвЩM(fЁЁi)ПВЭd
- 2025ИржЪөПИ«ЗтдNКЫҶў„У(dЁ°ng)ҙу•ю(huЁ¬)ФЪАӯЛ№ҫSјУЛ№ҲAқMЕeРР
Copyright(C) 1998-2025 ЙъОпЖчІДҫW(wЁЈng) лҠФ’Јә021-64166852;13621656896 E-mailЈәinfo@bio-equip.com