SMAD2/3ЕcTGF-ҰВНЁВ·…fН¬У°н‘ЮDдӣТтЧУ°lЙъm6A RNAјЧ»щ»ҜХ{ҝШёЙјҡ°ы°lУэ
ЕЯМҘёЙјҡ°ыЧчһйТ»·NИ«ДЬРФјҡ°ыЈ¬НЁЯ^ФцЦіәН·Ц»ҜЈ¬®aЙъ„УОпуwЛщУРҪMҝ—әНЖч№ЩөДјҡ°ыЎЈТСУРСРҫҝұнГчЈ¬ЕЯМҘёЙјҡ°ы°lЙъm6A RNAјЧ»щ»ҜЈ¬ҙу¶аЕcјҡ°ыФцЦі[1-2]Ј¬ГвТЯ‘Әҙр[4]кPПөГЬЗРЎЈИ»¶шЈ¬ҢҰУЪm6AРЮп—ФЪЕЯМҘёЙјҡ°ыПтЙсҪӣғИЕЯҢУјҡ°ы·Ц»ҜЯ^іМЦРөД·ЦЧУҷCЦЖДҝЗ°Іўӣ]УРПакPҲуөАЎЈҪсМмЈ¬·ЦПнТ»ЖӘУўҮш„ҰҳтҙуҢWСРҫҝҲFк УЪ2018Дк8ФВ°lұнФЪNatureЈЁУ°н‘ТтЧУЈә40.14Ј©ОДХВЈ¬БДТ»БДRNAјЧ»щ»ҜФЪХ{ҝШЕЯМҘёЙјҡ°ы·Ц»ҜЯ^іМЦРөДЧчУГҷCЦЖЎЈЯ@ЖӘОДХВөДй_о^әЬЦұҪУЈ¬КЧПИНЁЯ^йҶЧxОД«Iҙ_¶ЁБЛёРЕdИӨөД»щТтSMAD2/3Ј¬ҢҰЖдЯMРРCo-IPәНЩ|ЧVәуЈ¬ҪY№ып@КҫЖдДЬүтЕcјЧ»щ»ҜЮDТЖГёMETTL3Ј¬METTL14әНWTAPЦұҪУ»ҘЧчЎЈЛыӮғКЗГчРЗЈ¬әНЛыӮғҪYәПөД·ЦЧУТІКЗГчРЗ·ЦЧУЈ¬Я@І»Ј¬ФЪЕЯМҘёЙјҡ°ы®”ЦРУРСРҫҝХЯҫН°l¬FSMAD2/3ҫНәНMETTL3Ј¬METTL14ҪYәПЈ¬І»іцЛщБПЈ¬Я@Т»ҪYәПФЪЕЯМҘёЙјҡ°ы®”ЦРЖрөҪБЛЦШТӘЧчУГЎЈ

1.SMAD2/3ө°°ЧЕcMETTL3-METTL14-WTAPҸНәПОпҪYәП
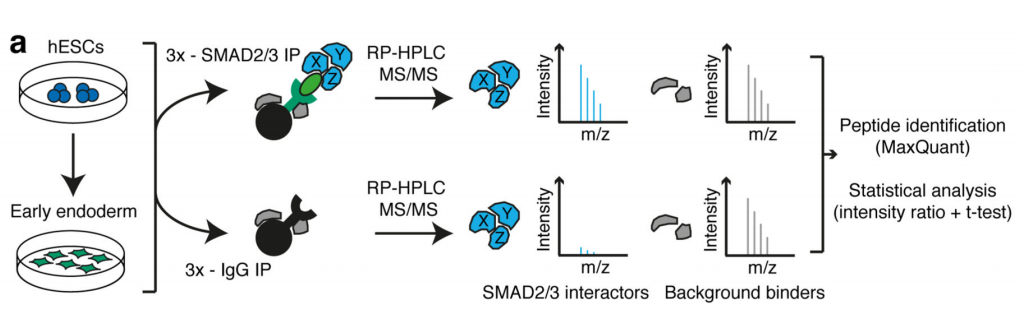
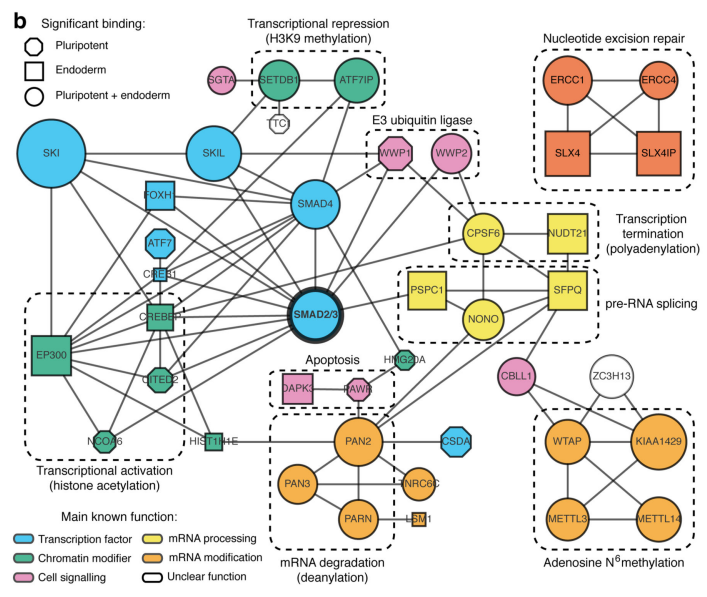
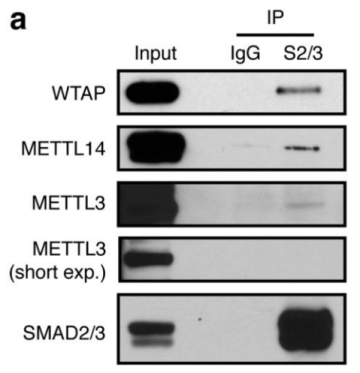
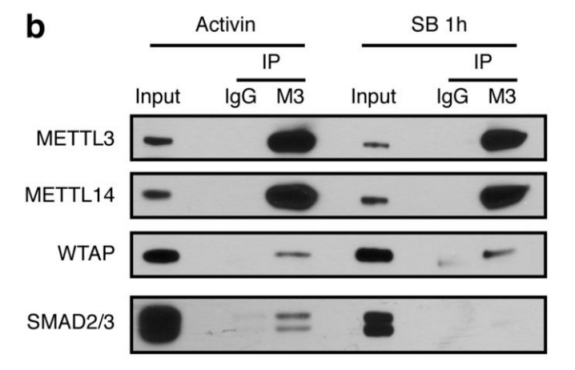
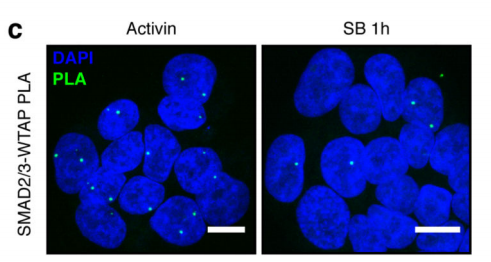
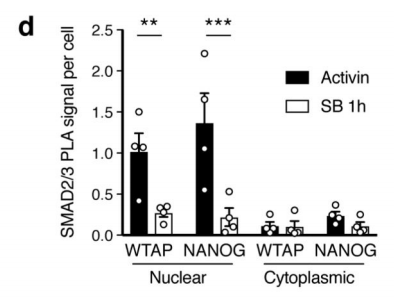
ЧчХЯКЧПИНЁЯ^уwНвҙМјӨЈ¬ХTҢ§ИЛоҗЕЯМҘёЙјҡ°ы·Ц»ҜһйЙсҪӣНвЕЯҢУјҡ°ыЈ¬ІўНЁЯ^Co-IPјјРgВ“әПЩ|ЧVЈЁФЖРтЙъОпМṩҙЛн—ҢҚтһЈ©јјРgЈ¬ҢҰұИғЙ·Nјҡ°ыЦРЈ¬ДЬүтЕcSMAD2/3ҝ№уwЦұҪУҪYәПөДө°°ЧЎЈҪY№ып@КҫЈ¬Т»№ІХТөҪ89ӮҖө°°ЧЈ¬ИЎҪ»јҜәуЈ¬өГөҪ78ӮҖ№ІУРө°°ЧЈ¬АLЦЖіЙҫWҪjҲDЈ¬°l¬FЯ@Р©ө°°Чіэ…ўЕcTGF-βРЕМ–НЁВ·Ј¬mRNAЙъОпҢWЯ^іМЦ®НвЈ¬ЯҖЕcҮшЧФИ»ҙуҹбьcRNAјЧ»щ»ҜЦРөДјЧ»щ»ҜЮDТЖГё-------METTL3-METTL14-WTAPҸНәПОпЦұҪУ»ҘЧчЎЈҙЛҪY№ыЕcәуЖЪWBтһЧCәНТЦЦЖSMAD2/3БЧЛб»ҜО»ьcәуCo-IPҪY№ыОЗәПЎЈPLAҢҚтһЧCҢҚғЙХЯйgөДҪYәПЦчТӘ°lЙъФЪјҡ°ыәЛғИЈ¬ІўЗТКЬActivinҙМјӨәуЈ¬У°н‘әЛғИЮDдӣТтЧУNANOGұнЯ_ЎЈ
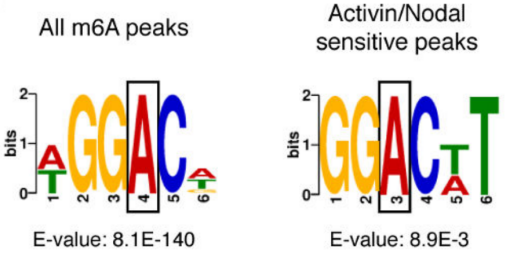
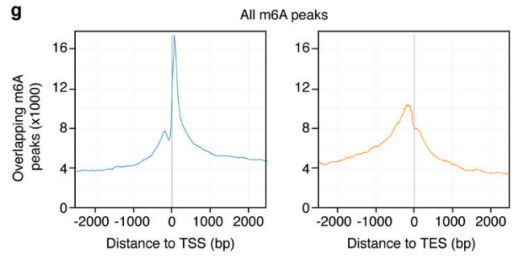
ЧчХЯТФActivin/NodalЗГҪөҪMЕЯМҘёЙјҡ°ыһйҢҚтһҪMЈ¬ОҙЗГҪөҪMһйҢҰХХЈ¬ГҝҪMИэӮҖЙъОпҢWЦШҸНЈ¬ЯMРРm6A RNAјЧ»щ»ҜңyРт(ФЖРтЙъОпМṩҙЛн—ҢҚтһЈ©ЎЈҪY№ып@КҫЈ¬motif…^УтұЈКШРтБРһйGGACЈ¬ЗТҙу¶аФЪЮDдӣЖрКј…^әНЮDдӣҪKЦ№…^ё»јҜЈ¬Activin/NodalМШУРјЧ»щ»ҜО»ьcФЪЮDдӣЖрКј…^өНё»јҜЎЈҝЙТ•»ҜҪY№ып@КҫЈ¬NANOGәНLEFTY1өДmRNA·ЦЧУЙПҙжФЪm6AјЧ»щ»ҜРЕМ–ЈЁИзјtҝтЛщКҫЈ©,ІўЗТНЁЯ^SMAD2/3өДChIPңyРтЈЁФЖРтЙъОпМṩҙЛн—ҢҚтһЈ©ҪY№ыЈ¬УРТ»Іҝ·Ц…^УтЕcјЧ»щ»ҜРЕМ–ЦШҜBЈЁИзҫGҝтЛщКҫЈ©ЎЈWTAP»тSMAD2/3ө°°ЧRIPҢҚтһЈЁФЖРтЙъОпМṩҙЛн—ҢҚтһЈ©ЧCҢҚЈ¬ФЪКЬActin·ЦЧУҙМјӨПВЈ¬WTAPЕcNANOGЈ¬LEFTЈ¬FZD8әНNOC2LҪYәПФцҸҠЈ¬¶шФЪSMAD2/3·ЦЧУҙМјӨПВЈ¬ДЬүтҙЩЯMЖдҪөҪвЎЈ
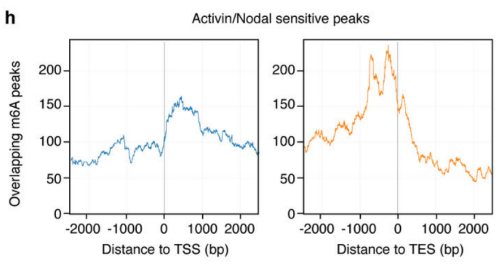
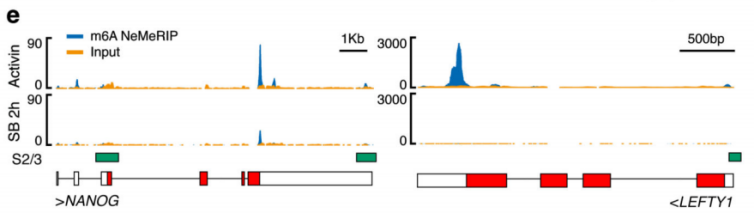
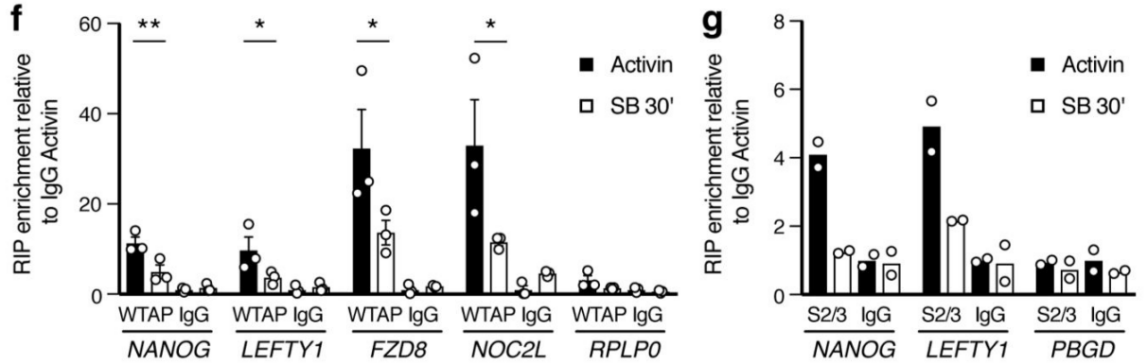
З°ИЛСРҫҝЧCҢҚm6A¶аФЪјҡ°ыәЛғИҙЩЯMpre-RNAөДәПіЙЈ¬УЙУЪұҫҢҚтһөДSMAD2/3НЁЯ^Еcm6A јЧ»щ»ҜГёҸНәПОпҪYәПЈ¬У°н‘°Р»щТтәПіЙөДО»ЦГН¬ҳУТІФЪәЛғИЈ¬ІўЗТSMAD2/3өДЮDдӣәНјЧ»щ»ҜКЬActivin/NodalХ{ҝШЈ¬ТтҙЛЈ¬ЧчХЯІВңySMAD2/3ҝЙДЬ…ўЕcpre-mRNAөДәПіЙЎЈНЁЯ^ТЦЦЖActivin/Nodalәуҷzңym6A RNAјЧ»щ»ҜЛ®ЖҪЈ¬°l¬FІо®җјЧ»щ»ҜөДЗйӣrІ»ҶОҶОФЪНвп@ЧУЙППВХ{Ј¬Н¬•rФЪНвп@ЧУәНғИә¬ЧУҪ»ҪзМҺКЬТЦЦЖЎЈҫCЙПЈ¬ActinНЁЯ^ҙЩЯMБЧЛб»ҜөДSMAD2/3ө°°ЧЕcПВУОЮDдӣТтЧУҪYәПЈ¬Х{ҝШ°Р»щТт°lЙъm6A RNAјЧ»щ»ҜЎЈ
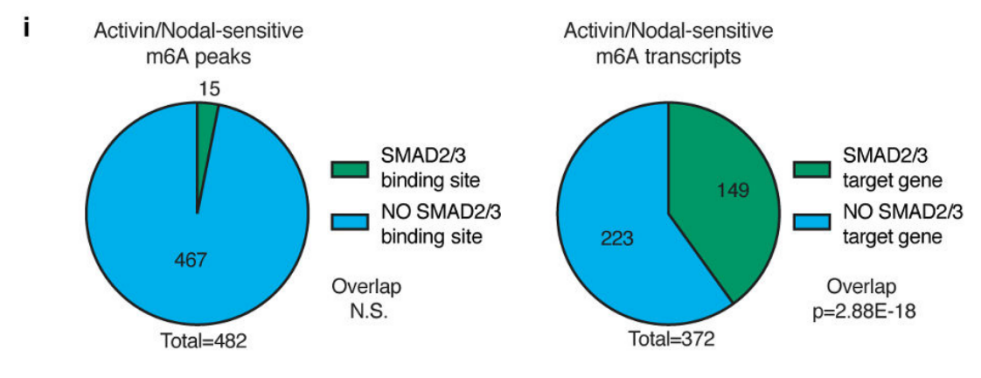
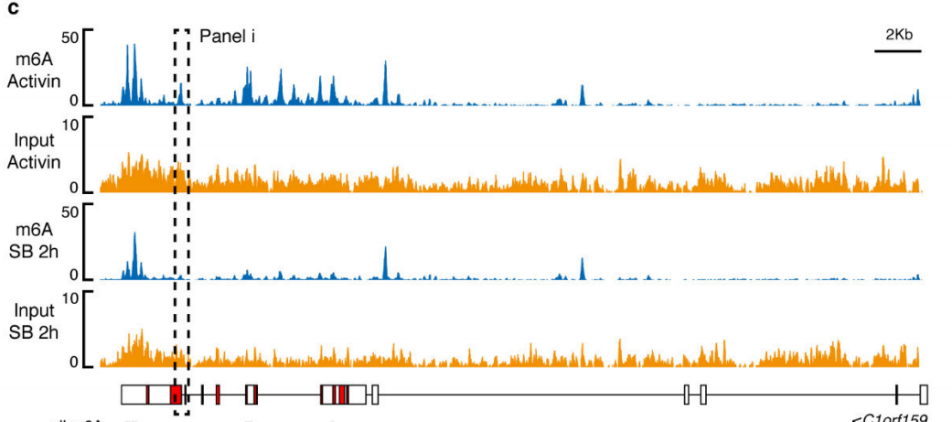
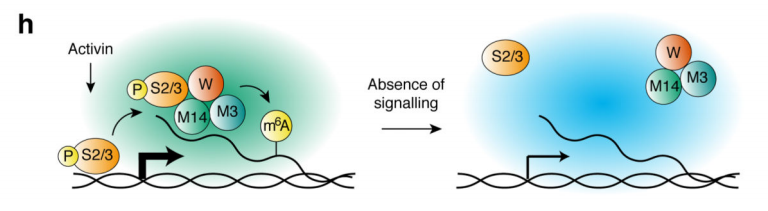
НЁіЈҒнХfЈ¬RNAјЧ»щ»ҜЕc»щТтөДұнЯ_кPПөГЬЗРЎЈЧчХЯҪУПВҒн·ЦОцБЛјЧ»щ»ҜЕcЮDдӣЛ®ЖҪөДғЙҪMҢWВ“әП·ЦОцЈ¬°l¬FПВХ{Activin/NodalНЁВ·әуЈ¬NNANOGЙПөДm6AјЧ»щ»ҜЛ®ЖҪЕcұнЯ_БҝіЙ·ҙұИЈ¬ІўҢҰЙсҪӣғИЕЯҢУ·Ц»ҜЖрҙЩЯMЧчУГЎЈ
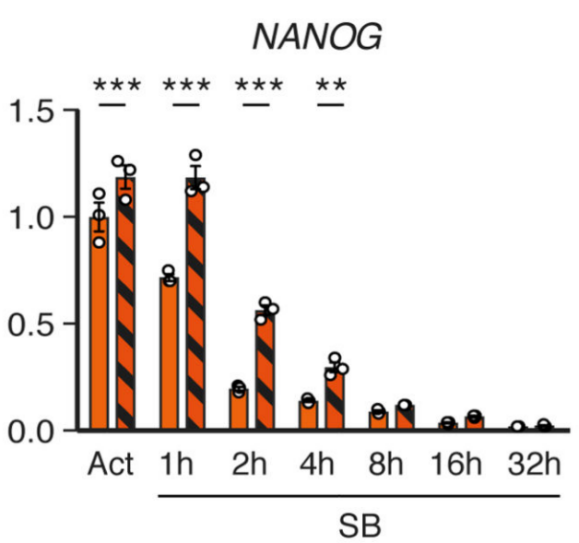
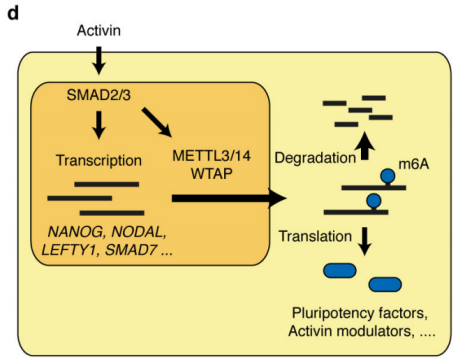
ұҫЖӘОДХВКЧҙОСРҫҝБЛSMAD2/3ө°°ЧЕcTGF-βНЁВ·йgҸНлsөДјҡ°ығИЙъОпҢWЯ^іМЎЈұҫОДҪY№ыХ№КҫБЛSMAD2/3ФЪmRNAЙП°l“]БЛХ{ҝШЈ¬өтНцЈ¬DNAРЮҸНәНЮDдӣәуХ{ҝШөДЙъОпҢW№ҰДЬЈ¬ІўкUКцБЛҙЛЯ^іМКЬActivin/NodalөДm6AјЧ»щ»ҜХ{ҝШЈ¬ІўЕcјЧ»щ»ҜЮDТЖГёйgөДкPВ“ЎЈұҫОДһйТФәуСРҫҝRNAјЧ»щ»Ҝ·ЗҪӣөдҷCЦЖЈ¬ИзЕcИҫЙ«Щ|ұнУ^ЯzӮчЎўЮDдӣәНұнО»Х{ҝШөм¶Ё»щөAЎЈ
И«ОДжңҪУ
https://www.nature.com/articles/nature25784
1.Yang D, Qiao J, Wang G, et al. N6-Methyladenosine modification of lincRNA 1281 is critically required for mESC differentiation potential[J]. Nucleic Acids Research, 2018, 46. У°н‘ТтЧУЈә11.561
2.Wen J, Lv R, Ma H, et al. Zc3h13 Regulates Nuclear RNA m6A Methylation and Mouse Embryonic Stem Cell Self-Renewal.[J]. Molecular Cell, 2018, 69(6):1028. ?У°н‘ТтЧУ: 14.248
3.Li H B, Tong J, Zhu S, et al. m6A mRNA methylation controls T cell homeostasis by targeting the IL-7/STAT5/SOCS pathways[J]. Nature, 2017, 548(7667):338-342. У°н‘ТтЧУ: 41.577?
ФЖРтЙъОпRNAјЧ»щ»Ҝ®aЖ·БРұн
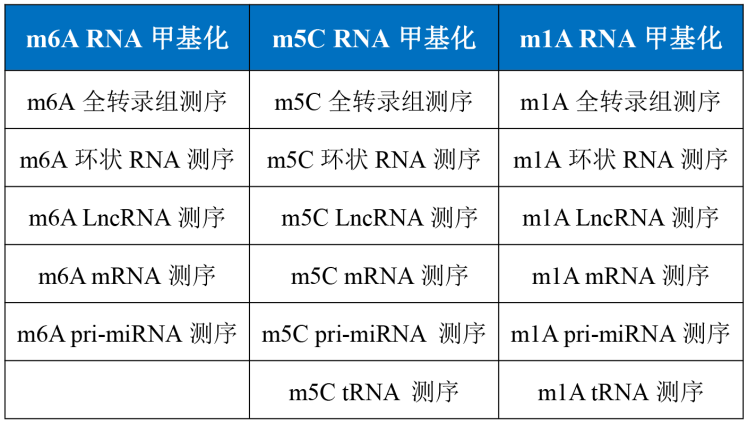
ФЖРтПакP®aЖ·НЖЛ]
НщЖЪ»Шоҷ
Nat. commun|Mettl3ҪйҢ§өДm6A RNAјЧ»щ»ҜХ{ҝШ№ЗЛийgідЩ|ёЙјҡ°ыәН№ЗЩ|КиЛЙ°Y
Nature|m6A RNAјЧ»щ»ҜЧR„eө°°ЧYTHDF1…ўЕcУӣ‘ӣөДРОіЙ
І»өГБЛЈ¬ҙуЕЈёжФVДгlncRNAјЧ»щ»ҜИзәОСРҫҝ
10·ЦТФЙПm6A RNAјЧ»щ»ҜңyРтОДХВ----ФЖРтЙъОпЦъБҰ
20·ЦОДХВЦРөДRNAјЧ»щ»ҜЈ¬ҹб¶ИЕcҢҚБҰІўҙж
ФЖРтЙъОпЧоРВm6A“RNAјЧ»щ»Ҝ”СРҫҝ…RҝӮ—·ЗҫҺҙaRNAЖӘ
ФЖРтЙъОпЧоРВ“RNA јЧ»щ»Ҝ”СРҫҝ…RҝӮ-”MДПҪжЖӘ
ФЖРтЙъОпЧоРВm6A“RNAјЧ»щ»Ҝ”СРҫҝ…RҝӮ—ІЎ¶ҫЖӘ
Plant CellЈә”MДПҪж°l¬FИ«РВm6A RNAИҘјЧ»щ»ҜРЮп—Гё
ФЖРтҝН‘ф12·Цн”јүОДХВЈ¬ҪМДгИзәОЗЙУГRIPңyРтНжЮD·ЦЧУҷCЦЖЈЎ
2018ДкNatureлsЦҫЦШ°хјүН»ЖЖРФСРҫҝіЙ№ы--m5C RNAјЧ»щ»Ҝ ФЖРтЙъОп
NatureН»ЖЖРФСРҫҝ—RNAјЧ»щ»ҜРВРЮп—m1A ФЖРтЙъОп
NatureЦШ°хЈәm6A RNAјЧ»щ»Ҝ…ўЕcФмСӘёЙјҡ°ы°lУэкPжIӯh№қЈЎ
Cancer Cell: әОҙЁҪМКЪФЪ°l¬Fm6A RNAјЧ»щ»ҜЦШТӘ№ҰДЬ
РЎ°ЧұШҝҙЈЎRNAјЧ»щ»ҜХыуwЛ®ЖҪиb¶ЁөД·Ҫ·Ё…RҝӮ
HepatologyЈәm6A RNAјЧ»щ»ҜГёMETTL3ҙЩёО°©°lХ№РВРюҷC
Shanghai Cloud-seq Biotech Co., Ltd.
өШЦ·ЈәЙПәЈКРЛЙҪӯ…^Э·ҙu№«В·518М–20М–ҳЗ3ҳЗ

лҠФ’Јә021-64878766
ӮчХжЈә021-64878766
ҫWЦ·Јәwww.cloud-seq.com.cn
а]ПдЈәmarket@cloud-seq.com.cn
- Target-BSјјРgҪТКҫМЗДтІЎТэ°lІӘЖр№ҰДЬХПөKөДDNAјЧ»щ»ҜХ{ҝШҷCЦЖ
- әПіЙЙъОпҢWөЧұPјҡ°ыЦ®®…іаҪНДёіЈУГұнЯ_Эdуwј°»щТтёДФмјјРg
- Йо¶ИҪвОцCRISPRОДҺмәYЯxБчіМј°‘ӘУГ°ёАэ
- ҝЙңШәН—lјюПВёЯ·ЦұжВКҷzңym6AРЮп—өДРВm6AңyРт·Ҫ·Ёй_°lСРҫҝ
- AIИЛ№ӨЦЗДЬФЪө°°ЧЩ|ҪYҳӢоAңyЎў№ҰДЬоAңyј°ФOУӢЦРөДЧчУГ
- m5C MeRIP-seqөИҪТКҫm5CРЮп—ФЪ°©°YДНЛҺЦРөДкPжIХ{ҝШҷCЦЖЦРөД‘ӘУГ
- ChIPјјРgҪТКҫNURR1ФЪЗ°БРПЩ°©ҸД»щТтЮDдӣөҪД[БцЯMХ№ЦРөДХ{ҝШҷCЦЖ
- ғЙ·NЮDдӣТтЧУФЪҪйҢ§·¬ЗС№ыҢҚіЙКмөДұнУ^ЯzӮчХ{ҝШЦР°l“]өДкPжIЧчУГ
- 2025І®әАЙъОпҙәјҫИ«ҮшСІЦvй_ҶўЈ¬ФзшBҲуГы“ҢХјПИҷC
- ИAҙуЦЗФмёұҝӮІГЦРҮш…^ҝӮҪӣАнЕнҡgҡgТ»РРөҪФLІ®әАЙъОп
- І®әА¶ӯКВйLіцПҜҢЈҫ«МШРВЦРРЎЖуҳI°lХ№үСҙуХ“үҜІў°lСФ
- І®әАЙъОплp11ҝсҡgМШ»Э»о„УҒнТuЈ¬ПЮ•rПЮБҝ“Ң
- вщГАНЁөВНЖіціЙұҫғrуwтһҶОјҡ°ыңyРтЈЁFFPE»тИ«СӘЈ©
- І®әАЙъОп2024ПөБРЕаУ–°аЈЁкғОчХҫЈ©ҲуГый_Ҷў
- І®әАҶОјҡ°ыFlexДкЦРҫЮ»ЭЈ¬1.1W/ҳУұҫ»о„УғrјҙҢўҪШЦ№
- Л{ҫ°ҝЖРЕDAP-seqјјРgПакPОДХВ6ЯB°lЈ¬ҝӮIF 95.2





