細胞不貼壁、生長緩慢,怎么破?

在細胞培養過程中會出現這樣或那樣的問題,這些問題從細胞生長角度來說,針對細胞不貼壁、生長緩慢、生長不好,甚至死亡的原因,我們做以下分析并提出相對應的解決方法。
一、培養細胞不貼壁
可能原因:
•胰蛋白酶消化過度;
•支原體污染;
•培養基pH值過堿(NaHCO3分解);
•細胞老化;
•接種細胞起始濃度太低或太高。
解決方法:
•縮短胰蛋白酶消化時間或降低胰蛋白酶濃度;
•分離培養物,檢測支原體。清潔支架或培養箱。如發現支原體污染,丟棄培養物;
•使用無菌醋酸溶液調整pH值或充入無菌CO2;
•啟用新的保種細胞;
•調節接種細胞濃度。
二、培養細胞生長緩慢
可能原因:
•由于更換不同培養液或血清;
•培養液中一些細胞生長必需成分如谷氨酰胺或生長因子耗盡或缺乏或已被破壞;
•培養物中有少量細菌或真菌污染;
•試劑保存不當;
•接種細胞起始濃度太低;
•細胞已老化;
•支原體污染 。
解決方法:
•比較新培養液與原培養液成分,比較新血清與舊血清支持細胞生長實驗,讓細胞逐漸適應新培養液;
•換入新鮮配置培養液,或補加谷氨酰胺及生長因子;
•用無抗生素培養液培養,如發現污染,丟棄培養物;
•血清需保存在-10到-20℃。培養液需在2-8℃避光保存。含血清完全培養液在2-8℃保存,需在1周內用完;
•增加接種細胞起始濃度;
•換用新的保種細胞;
•分離培養物,檢測支原體。清潔支架和培養箱。如發現支原體污染,丟棄培養物。
三、培養細胞生長不好
可能原因:
•細胞本身的狀態
細胞傳代次數多,細胞老化;
細胞的接種量:接種量過低,細胞生長緩慢;
細胞傳代時間過晚:細胞中毒,影響傳代后的細胞生長;
胰酶消化時間過長或過短:時間過長,細胞死亡;時間過短,細胞未完全分離而成團,細胞死亡;
細胞的凍存與復蘇:慢凍速融。
•污染
支原體污染;
霉菌污染。
•培養基或血清
更換血清或培養基之前未進行驗證;
選擇的培養基是否合適;
培養基配制是否準確無誤。
•培養環境
CO2供應是否正常;
培養箱或搖床溫度控制是否正確。
解決方法:
根據以上四個方面的可能原因,做出針對性的解決方案
•注意細胞的本身狀態:如傳代次數、接種量等;
•避免產生污染(用正規、合法、可溯源的血清);
•要用合適的血清或培養基,經過驗證;
•注意實驗室的環境。
四、培養細胞死亡
可能原因:
•培養箱內無CO2;
•培養箱內溫度波動太大;
•細胞凍存或復蘇過程中損傷;
•培養液滲透壓不正確;
•培養液中有毒代謝產物堆積 。
解決方法:
•檢測培養箱內CO2;
•檢查培養箱內溫度;
•取新的保存細胞種;
•檢測培養液滲透壓;
•換入新鮮培養液。
下面為您推薦Esco產品——CelCradle系列生物反應器—高密度細胞培養的搖籃
一、什么是CelCradle生物反應器

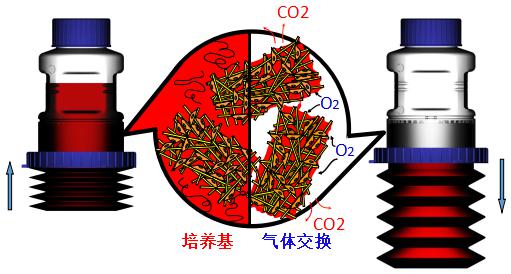
CelCradle生物反應器根據潮汐漲落原理設計而成,其中波紋管的壓縮和解壓可使細胞不斷接觸培養基的營養與空氣,提供了一個低細胞撕裂、無泡沫、高氧氣飽和度以及高營養濃度的細胞培養環境。
CelCradle是用于高密度細胞培養的一款易于使用的經濟型臺式生物反應器,既可以高密度培養細胞,也可以收集細胞分泌產物。
二、CelCradle潮汐式工作原理
通過CelCradle細胞培養瓶底部的波紋管壓縮和解壓,細胞間歇的暴露在空氣和培養基中,使細胞充分與培養基和氧氣接觸,和滾瓶的原理類似。
三、CelCradle生物反應器產品特點
•大面積高密度貼壁細胞培養空間
•預先滅菌、隨時可用
•一次性使用CelCradle培養瓶,操作簡單
•低剪切力、低細胞撕裂、無泡沫以及無氧氣限制高營養的細胞培養環境
•兼容大多數無血清培養基
•全細胞、細胞組分或細胞產物的培養和采集功能
四、為什么選擇CelCradle生物反應器
1. 簡便易用的設計,一次性使用可以節約空間和人力資源
CelCradle生物反應器是一款隨時可用的一次性生物反應系統,無需啟動時間及復雜的學習過程。
CelCradle生物反應器可放置在6立方英尺CO2培養箱內,并且可同時運行4個細胞培養瓶。 一個標準CelCradle細胞培養瓶帶有5.5g BioNoc II載體,可提供15000平方厘米的細胞培養總面積,培養細胞數可達到4~5x109/瓶,相當于18至20個滾動式細胞培養瓶的培養量。
可以通過增加CelCradle培養瓶數或者使用同為潮汐原理的TideCell生物反應器實現細胞規模的擴大化生產,從而簡化了培養系統規模擴大的過程以及節省了開發過程中所需的支出。
2. 高細胞產量,特殊的B_H功能促進蛋白表達
一臺CelCradle生物反應器可取代數百個培養皿、傳統細胞培養瓶以及多組細胞培養滾瓶等等,從而大大縮減生產成本。
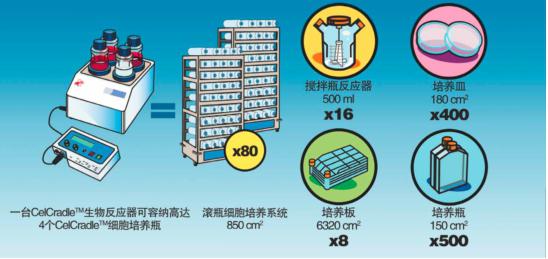
該系統不僅可實現較高的細胞產量,且這種特殊的B_H功能(增加底部保持時間)不僅限制了細胞的過度生長而且增加了超過3倍的蛋白表達,同時還可實現更高的蛋白濃度并在培養過程中節省培養基。
五、應用領域
•哺乳動物和昆蟲細胞培養
•蛋白質和病毒生產
•單克隆抗體生產
•蛋白質組研究
•藥物研發
•藥物代謝動力學研究
•基因和細胞治療研究
專業論文支持
以下是一些現有支持CelCradle細胞培養系統的科學研究應用的學術論文
[1]Akiyama, M., Nakayama, D., Takeda, S., Kokame, K., Takagi, J., & Miyata, T. (n.d.). Crystal structure and enzymatic activity of an ADAMTS-13 mutant with the East Asian-specific P475S polymorphism. J Thromb Haemost Journal of Thrombosis and Haemostasis, 1399-1406.
[2]Asaoka, Y., Tanaka, T., Tsumoto, K., Tomita, M., & Ide, T. (n.d.). Efficient expression of recombinant soluble human FcγRI in mammalian cells and its characterization. Protein Expression and Purification, 155-161.
[3]Brown, A., Mcsharry, J., Adams, J., Kulawy, R., Barnard, R., Newhard, W., . . . Drusano, G. (2011). Pharmacodynamic Analysis of a Serine Protease Inhibitor, MK-4519, against Hepatitis C Virus Using a Novel In Vitro Pharmacodynamic System. Antimicrobial Agents and Chemotherapy, 1170-1181.
[4]Chen, Y., Wu, J., Wang, K., Chiang, Y., Lai, C., Chung, Y., & Hu, Y. (n.d.). Baculovirus-mediated production of HDV-like particles in BHK cells using a novel oscillating bioreactor. Journal of Biotechnology, 135-147.
[5]Drugmand, J., J.-F., J., Agathos, S., & Schneider, Y. (n.d.). Growth of Mammalian and Lepidopteran Cells on BioNOC II Disks, a Novel Macroporous Microcarrier. Cell Technology for Cell Products, 781-784.
[6]Hammonds, J., Chen, X., Zhang, X., Lee, F., & Spearman, P. (n.d.). Advances in methods for the production, purification, and characterization of HIV-1 Gag–Env pseudovirion vaccines. Vaccine, 8036-8048.
[7]Haredy, A., Takenaka, N., Yamada, H., Sakoda, Y., Okamatsu, M., Yamamoto, N., . . . Okamoto, S. (2013). An MDCK Cell Culture-Derived Formalin-Inactivated Influenza Virus Whole-Virion Vaccine from an Influenza Virus Library Confers Cross-Protective Immunity by Intranasal Administration in Mice. Clinical and Vaccine Immunology, 998-1007.
[8]Haredy, A., Yamada, H., Sakoda, Y., Okamatsu, M., Yamamoto, N., Omasa, T., . . . Yamanishi, K. (2014). Neuraminidase gene homology contributes to the protective activity of influenza vaccines prepared from the influenza virus library. Journal of General Virology, 2365-2371.
[9]Ho, L., Greene, C., Schmidt, A., & Huang, L. (n.d.). Cultivation of HEK 293 cell line and production of a member of the superfamily of G-protein coupled receptors for drug discovery applications using a highly efficient novel bioreactor. Cytotechnology, 117-123.
[10]Hu, Y., Lu, J., & Chung, Y. (n.d.). High-density cultivation of insect cells and production of recombinant baculovirus using a novel oscillating bioreactor. Cytotechnology, 145-153.
有興趣進一步了解我們CelCradle系列生物反應器的顧客可以通過以下聯系方式咨詢我們:
Mobile:010-5823 6368/5823 6468
Email:mail@escolifesciences.cn
Website: www.escolifesciences.cn
本文轉載自CellMax胎牛血清,進行了一定的改編與排版,如有異議請聯系我們。





