最新生物標志物biomarker檢測技術進展(一)
生物標志物的概念早在1983年被首次提出,它是指可以標記系統、器官、組織、細胞及亞細胞結構或功能的改變的生化指標,具有非常廣泛的用途。由于生物標志物可用于疾病診斷、判斷疾病分期或用于評價新藥或新療法在目標人群中的安全性及有效性,展示出在藥物研發領域的重要作用。
2010年10月,美國FDA出臺文件討論生物標志物指導原則草案,預示著生物標志物已成為新藥臨床研究的評價工具之一(圖1)。美國NIH給生物標志物以更實用的詮釋:用以評價和衡量被試個體生物學過程,病理學過程以及對治療干預藥理學反應的特征指標,包括核酸,蛋白,代謝衍生物在內的諸多分子都可以成為潛在的生物標志物。蛋白是生物學功能的執行者,位于中心法則的功能一端,能夠為基礎醫學、轉化醫學和精準醫學提供最直接的判定依據,因而是研究和應用最為廣泛的標志物。因而對蛋白標志物的檢測技術也最為重要。迄今為止,抗體仍然是蛋白生物標志物檢測最根本的基礎,眾多方法以抗體為核心建立,并且不斷更新和發展,本綜述擬從應用視角出發,較為系統地分析和比較現有蛋白生物標志物的檢測技術,并結合全新技術的發展,對生物標志物的前景進行展望。

圖1. 生物標志物應用的轉化醫學研究領域

圖2. 生物標志物在藥物研發領域的應用
蛋白生物標志物可以幫助人們了解生物學過程,能運用于疾病的高危評估,早期診斷,檢測定位,預后判斷,治療反應,復發監測全過程。在早期診斷方面,以腫瘤研究為例,生物標志物可以提供預測,診斷和預后信息。特別是近年來興起的個性化治療和差異化診斷技術方面,生物標志物發揮的作用也日漸重要。因此不論對于科學研究還是制藥企業,生物標志物都是關注的焦點。生物標志物既可以為藥物的作用機制,如何影響靶點,以及下游的效應提供關鍵的洞見(圖2),也可在藥物早期研究中鑒定藥物或治療手段的毒性和副作用(例如肝毒性,腎毒性,心臟毒性,肌肉毒性等等。)這對于藥物研發有非常重要的意義,據統計,藥物研發過程中止的最重要原因來自藥物安全性評價或毒理學測試失敗(圖3,約占33%),而藥效不足僅排在第二的位置(26%)。
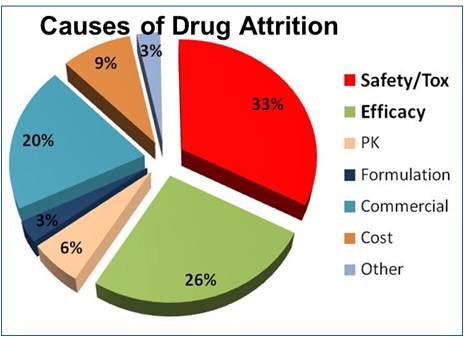
圖3. 藥物研發失敗原因分析
近年來興起的全新治療策略,例如嵌合抗原受體T細胞(即CAR-T)治療急性淋巴細胞白血病也對生物標志物的應用有了新的啟示。由于CAR-T細胞本身是具備免疫源性的物質,當輸入患者體內時,在治療效果之外,常會產生非常嚴重的副反應,例如細胞因子釋放綜合癥(Cytokine Releasing Syndrome, CRS)。人們對于CRS的認識與一位叫做Emily Whitehead的明星患者有很重要的聯系。Emily在治療史上的重要地位在于,在她之前的數位治療患者,出現過連續的病例死亡的情況,而她本身也發生了嚴重的炎癥反應。幸運的是,治療團隊利用抗炎性藥物幫助Emily挺過了讓人絕望的高燒。最終Emily成功活了下來。至此,Michel Sadelain(CAR-T技術的命名人,現供職于JUNO公司)等先驅開始應用蛋白多因子檢測技術對細胞因子生物標志物在治療過程中進行監控,并發現治療后關鍵的細胞因子CRP表達水平可以很好地判定CRS的風險(圖4,參考文獻2)。僅當CRP因子的表達量超過20mg/dl時,才會出現嚴重的細胞因子釋放綜合癥。來自中國的成功CAR-T治療案例里,蛋白多因子檢測技術也被成功應用(數據未展示)。
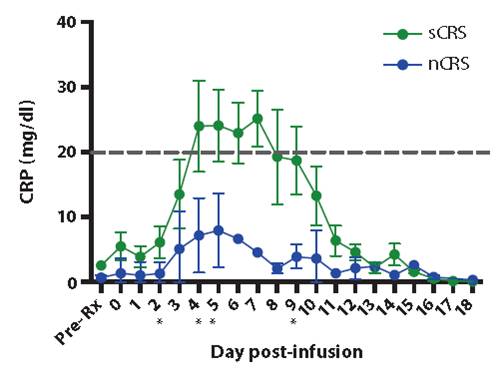
圖4. CRP標志物監測細胞因子釋放綜合癥





